Бактерия фрагилис что это
Бактерия фрагилис что это
Бактерии группы Bacteroides fragilis. Включают 9 видов неподвижных бактерий, образующих капсулу. Наиболее часто вызывают внутри-брюшинные и тазовые абсцессы, бактериемию, инфекции пролежней, артриты и остеомиелиты (основные возбудители В. thetalotaomicron, В. ovatus, В. vulgatus, В. distasonis). В мазках из клинического материала представлены бледными полиморфными палочками с закруглёнными концами.
Бактероиды часто неравномерно окрашиваются по Граму. На 5-7-е сутки образуют серовато-белые, прозрачные или мутноватые негемолизирующие S-колонии 1-3 мм в диаметре. На бульонах дают гомогенное помутнение. Ключевые признаки группы — способность расти на средах с 20% содержанием желчных солей; резистентность к канамицину (100 мкг), ванкомицину (5 мкг) и колистину (10 мкг). Чувствительны к действию производных имидазола.
Бактерии группы Bacteroides ureolytсus Группу образуют Bacteroides ureolyticus и Bacteroides gracilis; основное их отличие — инертность к углеводам. Вызывают инфекции женских половых органов, поражения дыхательных путей, костей и мягких тканей. В мазках из клинического материала представлены тонкими палочками с закруглёнными концами. На КА образуют мелкие полупрозрачные колонии, у некоторых штаммов — распластанные на поверхности. Часто вызывают позеленение и коррозию сред, содержащих кровь. Ключевые признаки группы — неспособность к росту на средах с 20% содержанием жёлчных солей, резистентность к канамицину (100 мкг) и колистину (10 мкг), но чувствительность к ванкомицину (5 мкг).
Принципы микробиологической диагностики бактероидов
Принципы получения и транспортировки образцов аналогичны таковым при подозрении на анаэробную инфекцию — следует избегать контакта образца с атмосферным воздухом. Образование супероксид дисмутазы В. fragilis позволяет бактериям сохранять жизнеспособность при непродолжительном контакте с атмосферным воздухом.
Бактероиды культивируют на КА, тиогликолевой среде. Оптимальны для роста анаэробные условия при 10% содержании С02 в атмосфере, температура 37 °С, рН 7,6-7,8.
Лечение заражений бактероидами
Бактероиды резистентны к пенициллинам, клиндамицину, цефалоспоринам 1-го и 2-го поколений. Препараты выбора — левомицетин, метронидазол и имипенем.
Бактероиды
История обнаружения
Бактероиды (Bacteroides) были впервые обнаружены в 1898 году учеными Вейоном и Зюбером (A. Veillon, H. Zuber). Микроорганизмы выделены у больного с абдоминальным абсцессом и получили название Bacillus fragilis. Спустя 14 лет Дистазо (A. Distaso) обнаружил их у здоровых людей, а через семь лет Кастеллани (A. Castellani) и Чалмерс (A. J. Chalmers) дали этим палочкам название Бактероиды.
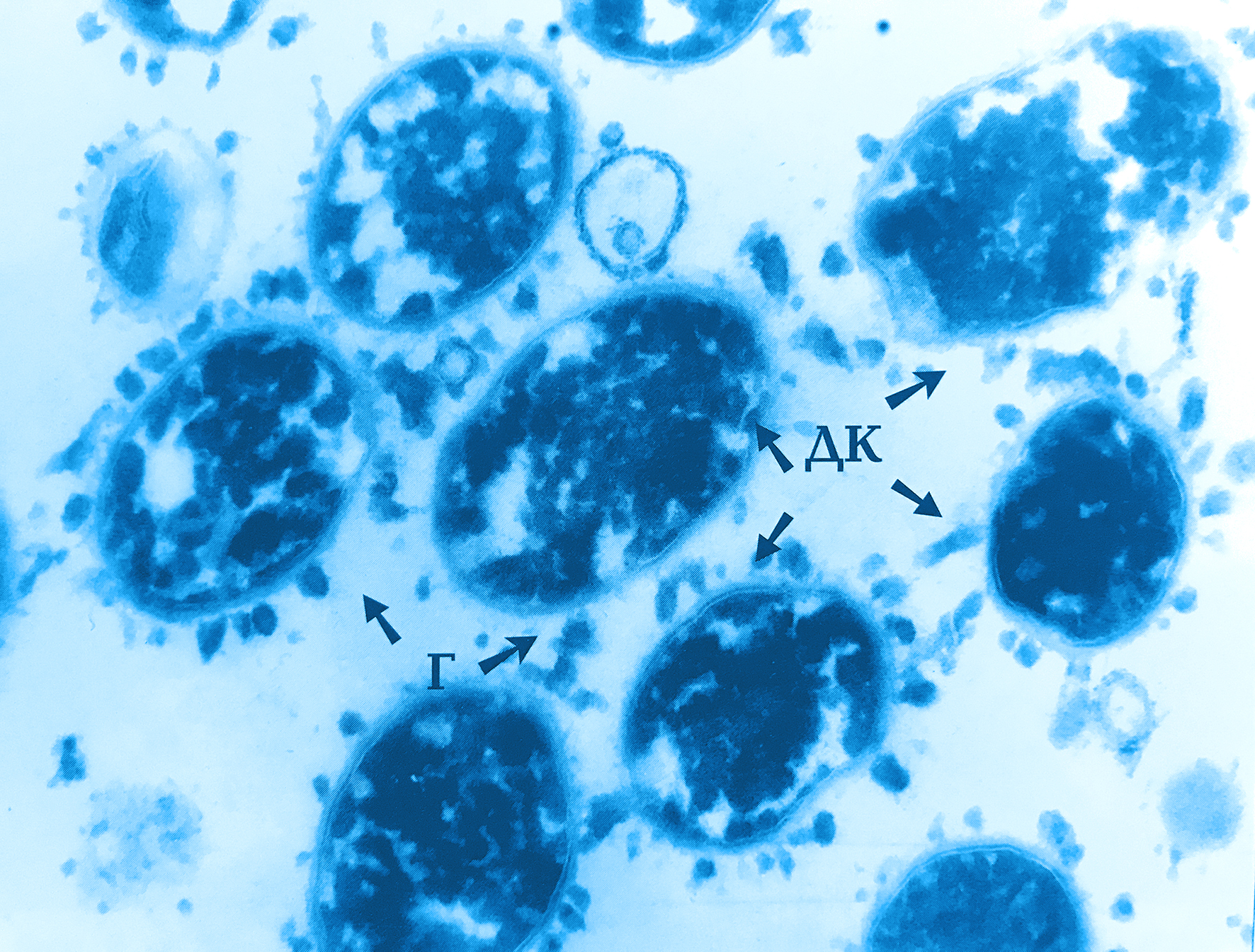
Внешний вид под микроскопом
Бактероиды при микроскопии могут иметь разную форму. Преимущественно это небольшие палочки, не окрашивающиеся по Граму. У отдельных видов эти палочки не обособляются при размножении, в результате чего получаются скопления бактерий, напоминающие ветви. Иногда у бактероидов имеются в одном из концов утолщенные вакуоли, за счет чего клетка приобретает форму кеглей или булавы. Поэтому их легко спутать с коринебактериями или спорообразующими бактериями. Бактероиды имеют жгутики и способны к образованию капсулы, позволяющей переждать неблагоприятные для жизни условия.
Где обитает
В норме представители Bacteroides у человека колонизируют толстую кишку и являются типичными представителями нормофлоры, наряду с лакто- и бифидобактериями. В фекалиях здорового человека около 40-50% всех микробных клеток составляют бактероиды.
Классификация
Царство
Bacteria
Тип
Bacteroidetes
Класс
Bacteroidia
Порядок
Bacteroidales
Семейство
Bacteroidaceae
Род
Bacteroides
Prevotella
Свойства
Бактероиды способны утилизировать сахарозу, мальтозу, глюкозу, рамнозу. Продуцируют янтарную, изовалериановую, уксусную и масляную кислоту. Вырабатывают вещества, способные инактивировать антибиотики пенициллового и цефалоспоринового ряда. Для роста необходим углекислый газ в концентрации 5-10% и температурный диапазон от +25 до +45°С. Оптимальная температура +37°С.
Функции
Биологическая роль бактероидов в толстом кишечнике изучена недостаточно. Однако доказана их антагонистическая активность по отношению к сальмонеллам, шигеллам и некоторым патологическим эшерихиям. Можно предположить, что, колонизируя толстый кишечник, представители Bacteroides защищают своего хозяина от инфекционных энтероколитов, вызванных патогенными микроорганизмами.
Вызываемые заболевания
В условиях нарушения иммунитета бактероиды проявляют свою патогенную активность. Они не вырабатывают эндотоксичные вещества, но, поскольку имеют полисахаридную капсулу, могут спровоцировать выработку антител в организме хозяина. В ассоциации с другими патогенными и условно-патогенными бактериями, Bacteroides способны вызывать перитонит, кольпит, пневмонию, пародонтоз, абсцессы, аппендицит, эндокардиты, заболевания слизистых оболочек и кожи.
Профилактика и лечение
Для подавления роста и размножения бактероидов используются антибиотики, в частности, ципрофлоксацин, офлоксацин, метронидазол, клиндамицин, левомицитин. Общеукрепляющие процедуры и элементарная гигиена, защита от стрессов и нормализация пищевого поведения (отказ от голодания и переедания), а также сбалансированный рацион питания способствуют защите от чрезмерного размножения бактероидов.
Bacteroides fragilis: злодейка или спасительница?
Данные об этой бактерии крайне противоречивы. С одной стороны, Bacteroides fragilis считают первопричиной целого ряда заболеваний, в том числе рака толстого кишечника. С другой — ей пророчат судьбу спасительницы от аутизма и воспаления кишечника. При этом B. fragilis является рядовой представительницей нормальной микрофлоры человека
В уютном жилище
B. fragilis — наиболее массовая анаэробная грамотрицательная палочковидная бактерия, обитающая в нижних отделах толстого кишечника. Основным местом ее локализации являются железистые крипты — мелкие углубления в слизистой оболочке. Здесь B. fragilis прекрасно себя чувствует при низких концентрациях кислорода и осуществляет утилизацию целлюлозы, азотсодержащих соединений, жирных кислот и стероидов. В кале здоровых людей около половины всех микробных клеток приходится на B. fragilis (1010–1011 клеток на 1 г сухих каловых масс), поэтому ее широко используют в качестве индикаторов фекального материала человека. Кроме того, эта бактерия входит в состав нормальной микрофлоры влагалища и вульвы, полости рта и гортани, а также верхних дыхательных путей человека. Однако в норме B. fragilis не должна содержаться во внутренних органах, не имеющих связи с окружающей средой. Если ее выделяют из крови, плевральной жидкости, жидкости брюшной полости или находят в ранах, то тогда речь уже идет о патологических процессах. Таким образом, B. fragilis относится к оппортунистическим патогенам, являясь обычным компонентом человеческой микрофлоры, но при определенных условиях может вызвать заболевание. Патогенность этой бактерии частично обусловлена ее способностью продуцировать капсульный полисахарид, который защищает от фагоцитоза и благоприятствует таким образом формированию абсцессов.
Темная сторона
B. fragilis известна в качестве основного возбудителя раневой септицемии. Как и другие бактероиды, она может вызывать различные гнойно-воспалительные заболевания после травм, оперативных вмешательств, инструментальных исследований, при онкопатологии или иммунодефицитных состояниях. B. fragilis может быть причиной внутрибрюшинных анаэробных инфекций, в частности вызывать перитонит и язвенный колит. Кроме того, с ней ассоциируют синовит, сальпингит, болезнь Рейтера, хронический тонзиллит, цервицит, эндометрит, аднексит, инфекции органов малого таза, а также простатит и хронический осложненный уретрит. Эта бактерия способна вызывать оппортунистические инфекции: синусит, воспаление среднего уха, инфекции ротовой полости, различные абсцессы и некротическую пневмонию, а также воспалительную диарею. Токсигенные штаммы B. fragilis, ассоциированные с воспалительной диареей, вырабатывают энтеротоксин, который стимулирует дегенерацию эпителиоцитов кишечника человека и разрезание Е-кадхерина.
Мозг и микробиом
Уже давно высказывались предположения о связи между деятельностью мозга и состоянием микробиома организма. Например, при «синдроме дырявой кишки» повышается проницаемость стенок кишечника, и в кровь выходят опасные токсины, негативно влияющие на работу всех систем организма, в том числе мозга. С помощью добавления B. fragilis в пищу мышам-аутистам удалось уменьшить выраженность таких симптомов аутизма, как повышенная тревожность, стереотипные движения и уменьшение голосовых контактов. Токсичные метаболиты бактерий (например, 4-этилфенилсульфат) усиливают симптомы аутизма, а восстановление баланса микрофлоры кишечника способствует их ослаблению. Кроме того, отходы жизнедеятельности бактерий могут непосредственно влиять на мозг, например, по меньшей мере два типа кишечной бактерии производят нейромедиатор γ-аминомасляную кислоту (ГАМК, GABA), который играет важнейшую роль в работе центральной нервной системы. Пока этот вопрос исследован плохо, но уже очевидно, что проблема заслуживает пристального внимания.
Лекарство от воспаления кишечника
Некоторые штаммы B. fragilis обусловливают воспаление тканей толстого кишечника. Кроме того, повышается активность гена по выработке фермента оксидазы. Это дает основание предположить, что определенные штаммы B. fragilis могут повышать чувствительность толстого кишечника к воздействию перекиси водорода, тем самым приводя к повреждению генетического материала и образованию злокачественных опухолей.
В других исследованиях было обнаружено, что B. fragilis вырабатывает вещество, названное полисахаридом А, которое стимулирует выработку лимфоцитами белка интерлейкина-10, известного также как фактор, ингибирующий синтез цитокинов. Благодаря этому в стенке кишечника угнетаются воспалительные процессы. Поэтому B. fragilis пророчат судьбу нового лекарства от таких воспалительных заболеваний кишечника, как неспецифический язвенный колит и болезнь Крона.
Очевидно, что жизнедеятельность B. fragilis вызывает много неоднозначных вопросов. Однако не остается сомнений, что дальнейшие исследования этой бактерии могут помочь при лечении многих сложных заболеваний
Состояние микробиоценоза влагалища, бактериальный вагиноз и возможности его лечения
Опубликовано в журнале:
«CONSILIUM MEDICUM», 2013, ТОМ 15, № 10, с. 22-24
А.В.Ледина, В.Н.Прилепская
ФГБУ Научный центр акушерства, гинекологии и перинатологии им. В.И.Кулакова Минздрава РФ
Бактериальный вагиноз (БВ) – широко распространенное патологическое состояние, встречающееся у женщин детородного возраста, которое включает комплекс изменений вагинального биотопа, характеризующегося снижением количества нормальной кислородпродуцирующей лактофлоры и повышением концентрации других микроорганизмов, особенно грамотрицательных анаэробов типа Prevotella Porphyromonas spp., Peptostreptococcus spp., Fusobacterium spp., Mobiluncus spp. и GV [5, 18].
Известно, что микрофлора влагалища здоровых женщин репродуктивного возраста представлена широким спектром микроаэрофилов, а также факультативных и облигатных анаэробов [4], присутствие которых не нарушает нормального состояния, не вызывает развития воспалительной реакции и патологических симптомов, характерных для вульвовагинита или БВ. В основном нормальная микрофлора представлена микроорганизмами рода Lactobacillus spp. – микроаэрофильными, продуцирующими перекись водорода палочками (71–100%), реже – анаэробными грамположительными палочками (5–30%).
Кроме лактобактерий, микроаэрофильная флора влагалища здоровых женщин представлена Gardnerella vaginalis (по данным разных авторов, в 6–60% случаев), а также включает облигатные анаэробы Peptostreptococcus spp. (30–90%), грамположительные анаэробные кокки, грамположительные палочки – строгие анаэробы Bifidobacterium spp. (у здоровых женщин примерно в 12% случаев), Clostridium spp. (10–25%), Propionibacterium spp. – P. acnes (до 25%), значительно реже выявляются Mobiluncus spp. (0–5%). Все эти микроорганизмы являются типичными представителями нормальной микрофлоры генитального тракта.
В нормальном биотопе также могут обнаруживаться грамотрицательные строго анаэробные палочковидные бактерии бактероиды Bacteroides spp.: B. urealyticum, B. fragilis, B. vulgatus, B. ovatus, B. distasonis, B. uniformis, B. coccae, B. multiacidus (9–13%), Fusobacterium spp. (14–40%), Porphyromonas spp. (31%), Prevotella spp. (60%) и генитальные микоплазмы M. hominis, U. urealyticum (у 2–15% сексуально активных женщин).
Из представителей факультативных анаэробных микроорганизмов часто выделяют каталазопозитивные, коагулазонегативные Staphylococcus epidermidis, новобиоцинрезистентные Staphylococcus saprophyticus, Streptococcus spp. Это стрептококки группы viridans – «зеленящие» (а или g), гемолитические, стрептококки серологической группы В (Streptococcus agalactie), стрептококки серологической группы D (энтерококки); непатогенные коринебактерии – Corynebacterium minutissimum, C. equi (новое название – Rhodococcus equi), C. aquaticum, C. xerosis; Escherichia coli.
Микробиоценоз влагалища при БВ характеризуется резким снижением уровня перекись продуцирующих лактобактерий, вплоть до их полного исчезновения, и замещением их гарднереллами, которые способствуют росту колоний аэробных и анаэробных микроорганизмов. Кроме G. vaginalis, характерными представителями микрофлоры при БВ являются Prevotella spp., Porphyromonas spp., Bacteroides spp., Peptostreptococcus spp., Mycoplasma hominis, Ureaplasma urealyticum, Mobiluncus spp., а также Fusobacterium spp. и Atopobium vaginae.
Концентрация микроаэрофильных бактерий (G. vaginalis) при БВ может повышаться в сотни раз, а анаэробных микроорганизмов Bacteroides spp., Peptococcus spp. – в тысячи раз и более [1, 9]. В некоторых случаях на фоне абсолютного преобладания микроорганизмов, ассоциированных с БВ, могут присутствовать и лактобактерии в низком титре, но, как правило, это анаэробные лактобактерии, неспособные продуцировать перекись водорода.
В сложной цепи патогенеза различных заболеваний женских половых органов существенная роль отводится иммунным реакциям организма. Снижение неспецифической резистентности у пациенток с БВ [2], а также то, что до 90% G. vaginalis находятся на поверхности вагинального эпителия в виде биопленок [21], способствует росту резистентности анаэробной вагинальной флоры [13] к современным лекарственным препаратам и длительному рецидивирующему течению патологического процесса.
Клиника
Основными клиническими проявлениями БВ являются гомогенные выделения из влагалища, пенистые, слегка тягучие, белого или серого цвета со специфическим «рыбным» запахом. Другие жалобы, такие как зуд, дизурические расстройства, диспареуния, встречаются реже, могут совсем отсутствовать или появляться периодически. Бессимптомное течение инфекционного процесса наблюдается более чем у 1/2 всех женщин с БВ, и у них какие-либо субъективные жалобы могут вообще отсутствовать [16]. При длительно текущем процессе выделения приобретают желтовато-зеленоватую окраску, становятся более густыми, нередко напоминают творожистую массу, равномерно распределяются по стенкам влагалища без выраженного его воспаления [8].
Наиболее опасны осложнения БВ, которые возникают при беременности, во время родоразрешения (преждевременный разрыв плодных оболочек, хориоамнионит, аномалии родовой деятельности), в послеродовом или послеоперационном периоде в случае оперативного родоразрешения (послеродовый эндометрит). БВ может оказывать неблагоприятное влияние на развитие плода (гипотрофия) или новорожденного (пневмония), поэтому чрезвычайно важным является лечение этого заболевания в период планирования и во время беременности [1].
Диагностика
С 1983 г. и по настоящее время для постановки диагноза БВ применяются критерии, предложенные R.Am-sel и соавт. (1983 г.), которые включают наличие обильных выделений из влагалища с неприятным запахом; появление запаха «гнилой рыбы» при проведении аминного теста; повышение значения pH вагинального содержимого до 4,5; присутствие «ключевых клеток» в мазках, окрашенных по Граму. Диагноз БВ можно поставить в случае выявления 3 из 4 указанных критериев.
Микроскопия вагинального мазка, окрашенного по Граму, – наиболее информативный, достоверный и доступный метод диагностики БВ, который дает возможность объективно оценить состояние вагинальной микроэкологии, причем позволяет оценить не только морфологические особенности и соотношение отдельных компонентов вагинальной микрофлоры, но и получить информацию о состоянии слизистой влагалища и наличии лейкоцитарной реакции [5]. Полимеразная цепная реакция позволяет провести не только типирование, но и количественное определение микроорганизмов в режиме реального времени и в последние годы широко применяется в клинической практике.
Лечение
Успешное лечение БВ, как и любого заболевания, зависит от правильной и своевременной постановки диагноза и проведения патогенетически обоснованной эффективной терапии.
Цель лечения БВ – восстановить нормальную микрофлору влагалища, задержать рост микроорганизмов, не свойственных этому микроценозу. Как правило, на первом этапе лечения для пациентки подбирается терапия, которая обеспечивает высокую концентрацию лекарственного вещества во влагалище, что обусловливает эффективность использования малых доз антимикробного препарата и быстрое купирование симптомов заболевания. Второй этап лечения включает стимуляцию нормальной лактофлоры влагалища за счет применения биологических бактерийных препаратов – эубиотиков и пробиотиков [6].
Основными препаратами для лечения БВ являются метронидазол, клиндамицин и тинидазол. Эти препараты могут применяться как в таблетированной форме для приема внутрь, так и в виде вагинальных таблеток, гелей, свечей. Хотя пероральный путь приема ассоциируется с большей частотой побочных эффектов, он является более приемлемым для большинства пациенток.
Метронидазол рекомендуется назначать в дозе 500 мг 2 раза в день в течение 7 дней или 1-кратно в дозе 2 г, но такой режим считается менее эффективным. При приеме метронидазола могут возникать побочные эффекты со стороны желудочно-кишечного тракта в виде металлического вкуса во рту и тошноты (до 10%), а также транзиторная нейтропения (7,5%), периферическая нейропатия. Тошнота, другие гастроинтестинальные эффекты менее выражены при интравагинальном пути введения метронидазола. Вагинальный гель в дозе 5 г, вводимый ежедневно в течение 5 дней, не уступает по эффективности пероральному пути введения и с успехом может применяться для лечения БВ [17].
Тинидазол – препарат нитроимидазольного ряда, применяется в таблетках по 1 г 1 раз в день в течение 5 дней или по 2 г в течение 2 дней.
Сравнимым по эффективности с метронидазолом, но имеющим меньшее количество побочных эффектов является клиндамицин (Клиндацин ® ) – антибиотик группы линкозамидов, обладающий широким спектром действия, оказывающим в основном бактериостатический эффект. Клиндамицин активен в отношении Staphylococcus spp. (в том числе Staphylococcus epidermidis, продуцирующих пенициллиназу), Streptococcus spp. (исключая Enterococcus spp.), Streptococcus pneu-moniae, Corynebacterium diphtheriae, в отношении споро- и неспорообразующих анаэробов и микроаэрофильных грамположительных кокков (включая Peptococcus spp. и Peptostreptococcus spp.), Clostridium perfringens, Clostridium tetani, Mycoplasma spp., Bacteroides spp. (включая Bacteroides fragilis и Prevotella melaninogenica), Fusobacterium spp., Propionibacterium spp., Eubacter spp., Actinomyces spp., т.е. против большинства микроорганизмов, вызывающих дисбиоз влагалища и БВ.
Предпочтительным режимом является местное применение препарата в течение 3–7 дней. При этом вагинальные суппозитории вводятся по 1 на ночь или 2% вагинальный крем при помощи аппликатора (5 г) на ночь 3–7 дней. Перорально клиндамицин назначается 2 раза в день по 300 мг в течение 7 дней.
Местный клиндамицин является наиболее эффективным по сравнению с метронидазолом препаратом при лечении рецидивирующего БВ, особенно ассоциированного с A. vaginae; клиническое излечение при его применении наступает в 83,3% случаев (рПобочные эффекты (псевдомембранозный колит, тошнота) при приеме клиндамицина встречаются редко, что значительно повышает комплаентность терапии.
Применение клиндамицина (Клиндацин ® ), что очень важно, возможно при беременности или в подготовительном к родам периоде (только местно) в обычных терапевтических дозировках.
Эффективность, быстрое достижение положительного результата лечения, хорошая переносимость клиндамицина при лечении, в том числе беременных женщин, доказана при проведении многочисленных рандомизированных плацебоконтролируемых сравнительных клинических исследований [1, 7, 14].
Вторым этапом лечения, а также с целью профилактики рецидивов БВ назначаются эубиотики, пробиотики, которые могут применяться в комплексе с антибактериальными препаратами или как основное средство лечения. В первом случае назначение пробиотиков целесообразно проводить не ранее чем через 3 дня после окончания антибактериальной терапии БВ в виде интравагинальных суппозиториев; длительность лечения должна составлять менее 7–10 дней [6, 12].
После проведенного лечения примерно у 1/3 пациенток возникает рецидив заболевания в течение первых 3 мес, а более чем у 1/2 симптоматика возобновляется в течение 12 мес [19, 20]. Это вероятнее всего происходит в связи с неэффективностью проведенного лечения, так как от 65 до 80% [15] патогенов находится в составе биопленок, матрикс которых может связывать или не пропускать, и/или инактивировать антибиотики [3, 10, 11] и приводить к снижению эффективности лечения. Другой возможной причиной частых рецидивов является то, что не происходит достаточно полного восстановления нормальной микрофлоры влагалища и на этом фоне вновь активизируется патогенная микрофлора [12, 23].
Вопрос о целесообразности назначения лечения партнерам женщин, получающих лечение по поводу БВ, не решен. Ряд исследователей считают, что лечение половых партнеров не влияет на успешность терапии, хотя доказана роль половых контактов в возникновении и рецидивировании БВ. Кроме того, показана эффективность использования презервативов в снижении частоты рецидивов БВ [22]. Но поскольку доказательная база для окончательных выводов остается недостаточной, для решения этой задачи необходимы новые исследования.
Таким образом, БВ, представляющий дисбиотическое состояние экосистемы влагалища, является достаточно распространенной в современной популяции патологией, требующей своевременной диагностики, комплексной адекватной терапии и профилактики. Препаратом, оказывающим быстрое положительное действие и обладающим хорошей переносимостью, а также разрешенным к применению во время беременности, является клиндамицин (Клиндацин ® ). Высокая эффективность, доказанная клиническими исследованиями, позволяет использовать Клиндацин ® в клинической практике как один из основных препаратов для лечения БВ.
Индекс лекарственного препарата: Клиндамицин: Клиндацин ® (Акрихин ОАО)
Bacteroides fragilis (бактероиды фрагилис)

Bacteroides fragilis — неподвижные, образующие капсулу бактерии. Капсулы обладают интенсивным свечением и значительной толщиной, превышая размер клетки в 3–6 раз.
Bacteroides fragilis — нормальная микрофлора человека
Основное место обитания Bacteroides fragilis в человеческом организме — толстая кишка. В кале здоровых людей Bacteroides fragilis составляют около половины всех микробных клеток. Bacteroides fragilis также входят в состав нормальной микрофлоры влагалища и вульвы, полости рта и гортани, верхних дыхательных путей человека. Bacteroides fragilis, как и другие бактероиды, во внутренних органах, не имеющих связанных с внешней средой полостей, и во внутрибрюшинном пространстве у здоровых людей отсутствуют.
Нарастание содержания Bacteroides fragilis в кишечнике человека коррелируется с выраженностью газообразования (Шульпекова Ю.О.).
Bacteroides fragilis — возбудители заболеваний
Bacteroides fragilis, как и другие бактероиды, могут вызывать различные гнойно-воспалительные заболевания после травм, оперативных вмешательств, инструментальных исследований, при онкопатологиях или иммунодефиците.
Bacteroides fragilis могут быть причиной как внутрибрюшинных инфекций, таких как перитонит, хронический язвенный колит, так и синовиита, сальпингита, болезни Рейтера, хронического тонзиллита, цервицита, эндометрита, аднексита, инфекции в малом тазу, а также простатита, хронически протекающего осложнённого мужского уретрита.
Антибактериальные средства (из имеющих описание в данном справочнике), активные в отношении Bacteroides fragilis: метронидазол, тинидазол, рифаксимин, джозамицин, линкомицин, клиндамицин, моксифлоксацин. Bacteroides fragilis резистентны к ципрофлоксацину, рокситромицину. Большинство штаммов Bacteroides fragilis устойчивы к доксициклину.
Bacteroides fragilis в МКБ-10
Bacteroides fragilis в систематике бактерий
Bacteroides fragilis относятся к роду бактероиды (лат. Bacteroides), входящему в семейство Bacteroidaceae, порядок Bacteroidales, класс Bacteroidia, тип Bacteroidetes, Bacteroidetes/Chlorobi group, Fibrobactere-Chlorobi-Bacteroidetes superphylum, царство Бактерии.
Синонимы (более ранние названия): Bacillus fragilis, Fusiformis fragilis, Ristella fragilis, Pseudobacterium fragilis, Bacteroides inaequalis, Sphaerophorus inaequalis, Pseudobacterium inaequalis, Bacteroides incommunis, Ristella incommunis, Pseudobacterium incommunis, Bacteroides uncatus, Ristella uncata, Pseudobacterium uncatum, Sphaerophorus intermedius.