усиление сосудистого рисунка печени что это значит
Университет
В редакции «Медицинского вестника» прошла прямая линия с доцентом 2-й кафедры детских болезней БГМУ, главным внештатным детским гастроэнтерологом Минздрава Ириной Саванович.
Таисия Тарасова, Минск: Ребенку 11 лет. Обнаружены 2 камня в желчном пузыре (5 и 6 мм в диаметре). Как понять, можно ли справиться с ними при помощи лекарств? Какое обследование пройти и где?
По результатам УЗИ усилен сосудистый рисунок печени. Что это означает?
— Желчнокаменная болезнь — одно из самых распространенных заболеваний у взрослых. 20–30 лет назад эту патологию у детей регистрировали нечасто, однако сейчас наблюдается четкая тенденция к ее омоложению (если есть заболевания органов ЖКТ, холелитиаз выявляют в 0,1–1% случаев).
Следует учитывать возраст ребенка, химический состав и особенности формирования желчных камней. Как правило, преобладают билирубиновые, и только в пубертатном возрасте имеет место холестериновый литиаз. У малышей часто встречаются смешанные по составу конкременты.
Необходимо динамическое наблюдение у детских гастроэнтеролога и хирурга, т. к. при однократном осмотре определить оптимальную тактику сложно. Требуется выяснить анамнез, проанализировать факторы риска: страдает ли ребенок ожирением; имеются ли эндокринные заболевания, сбой в работе других органов ЖКТ, почек, патология системы крови и т. д.
Успех медикаментозного лечения, дието- и физиотерапии зависит от продолжительности болезни. Чем дольше камни находятся в желчном пузыре, тем выше вероятность хирургического вмешательства.
Усиление сосудистого рисунка печени по данным УЗИ — маркер процессов, которые происходят в желчном пузыре.
Оксана Шусть, Минск: Как должен питаться ребенок второго и третьего года жизни?
— Меню — важный аспект, ведь до 2 лет закладывается пищевое поведение ребенка, формируются пристрастия в еде и вкусовые предпочтения.
Наиболее актуальный вопрос: переводить ли малыша на «взрослый» стол после года? Все зависит от того, как привыкли питаться родители.
Если рацион сбалансирован, в нем достаточно овощей, фруктов, мяса и рыбы, исключены фастфуд и острое, а у ребенка нет заболеваний ЖКТ, пищевой непереносимости, тогда постепенный переход к обычной еде возможен.
Но есть семьи, в которых блюда сильно солят, любят сосиски и колбасы, постоянно перекусывают, предпочитают углеводы, во все питье добавляют сахар. Так родные программируют у детей привычки, способные в будущем привести к патологии ЖКТ, ожирению, метаболическому синдрому и т. п.
Чем больше соли в еде — тем сильнее хочется пить. Жажду, как правило, предлагают утолять сахаросодержащими напитками. Избыточное потребление углеводов создает условия для детского ожирения. Получается порочный круг.
Наталья Заворотняя, Минск: Дочери 13 лет, с 6 беспокоят боли в желудке (3–4 раза в неделю). В детской больнице поставили диагноз «гастрит». Посоветовали спасаться смектой, она действительно помогает. Тревожат сильный запах изо рта, белый налет на языке, угревая сыпь, от которой не избавляют современные средства. Жирную и острую пищу не употребляем.
Посоветуйте, какое обследование и где пройти. Обслуживаемся в 23-й горполиклинике.
— Имеет значение, когда девочку госпитализировали и в каком возрасте ей поставили диагноз, лечилась ли по поводу хеликобактер пилори (угревая сыпь часто ассоциирована с наличием в желудке этого возбудителя). С моей точки зрения, требуется повторное обследование и, вероятно, госпитализация. Амбулаторную и стационарную помощь окажут в 4-й ГДКБ Минска. Может проконсультировать гастроэнтеролог РНПЦ «Мать и дитя». Нужно взять направление педиатра из поликлиники по месту жительства или обратиться самостоятельно.
Необходимы стандартные обследования: общие анализы крови и мочи, биохимический — крови, УЗИ органов ЖКТ, оценка параметров физического развития, копрограмма и т. д.
Наталья Родюкова, Комарин: Ребенку 2 года 10 месяцев. Диагноз «функциональный запор». В течение года ходит «по-большому» только после клизмы или в период приема фенибута, фитолакса и лацидофила. Какое обследование пройти? Как лечиться?
— Надо знать детали: вес при рождении, как ребенок набирал массу, питался грудным молоком или был на искусственном вскармливании, с какого возраста ввели прикорм, когда именно появились запоры, начались ли они на фоне благополучия, насколько часто приходится прибегать к клизмам?
Функциональные запоры могут скрывать врожденную патологию кишечника. Нередко проблему с дефекацией вызывают пищевая аллергия, патология щитовидной железы.
Если запоры прогрессируют, плохо контролируются диетотерапией, рекомендую госпитализацию в детское гастроэнтерологическое отделение Гомельской ОКБ. Возможно, там сделают ирригоскопию.
Надо запастись терпением. Лечение по продолжительности будет таким же, как и период формирования недуга.
Маргарита, Могилев: Дочери 5,5 года, весит всего 16 кг при росте 108 см. Стул неустойчивый, аппетит плохой. Нужно ли корректировать питание, физическое развитие? К какому специалисту обращаться и куда? Хотелось бы пройти обследование на республиканском уровне.
— Начать рекомендую с осмотра педиатром в поликлинике по месту жительства. Он решит, к каким докторам еще обратиться, достаточно ли будет содействия в условиях областной больницы.
Амбулаторную помощь детям из всей Беларуси оказывают в РНПЦ «Мать и дитя». При необходимости врачи могут направить на консультацию или для стационарного обследования и лечения в 3-ю ГДКБ Минска, где с 2008 года функционирует Республиканский детский центр целиакии.
Анна: Дочери 11 лет. Уже год ее беспокоит тошнота. Поначалу неприятное ощущение появлялось ближе к вечеру, сейчас — в разное время. С чем связан такой симптом?
— Тошнота относится к общим симптомам физического неблагополучия; может сигнализировать о неполадках любых органов и систем (не только ЖКТ, но и нервной, сердечно-сосудистой и др.).
Необходимо обратиться к педиатру по месту жительства. Врач решит, к какому специалисту направить ребенка и какие обследования назначить. Самолечение недопустимо!
Инна: Два месяца назад четырехлетняя дочь пила гельминтокс (кашляла по ночам, и педиатр назначил для профилактики от глистов). Сейчас в кале нашли цисты лямблий (низкая инвазия). Лечить лямблиоз (беспокоят боли в животе) или подождать какое-то время? Не короткий ли перерыв между приемами препаратов?
— Если после антигельминтной терапии обнаружили лямблии, нужен новый курс. Обследоваться надо всей семье и тем, кто ухаживает за девочкой.
Лекарство и методы контроля подберет педиатр, гастроэнтеролог или инфекционист по месту жительства.
Анна: Ребенку 4,5 года. Кал обычно очень плотный, сухой, фрагментированный; периодически — в виде «овечьего». Год назад делали УЗИ кишечника — все в норме. В туалет ходит ежедневно. Стараемся придерживаться диеты, молочные продукты не употребляем.
— Чаще всего причина сухого фрагментированного кала — недостаток жидкости. В таком возрасте ее нужно выпивать 11,5 литра в сутки. Желательно простую воду. Сахаросодержащие напитки исключить.
Татьяна В.: У четырехлетнего сына время от времени появляется запах селедки изо рта. Зубы в порядке…
— Такой признак иногда свидетельствует о проблемах в полости рта. Свободно ли ребенок дышит носом, храпит ли во сне? Вероятно, есть патология лор-органов или расстройство работы ЖКТ.
Необходимость в обследованиях и консультациях узких специалистов определит педиатр.
Валентина: У ребенка (5 лет) часто болел живот. УЗИ брюшной полости показало, что в подвздошных областях есть свободная жидкость; выявили преходящую илеоилеальную инвагинацию. Может ли это быть следствием плохого аппетита?
— Инвагинация, скорее всего, говорит о заболевании. Допустим, какая-либо врожденная патология (например, гуляющая брыжейка) проявила себя только сейчас.
Нужна консультация детских гастроэнтеролога и хирурга.
Плохой аппетит иногда указывает на проблемы с ЖКТ.
Дмитрий: У ребенка (6,5 года) в кале нашли яйца описторхоза. Какие лекарства наиболее эффективны для выведения этого паразита?
— Обследоваться и лечиться необходимо всей семье. За медпомощью обратиться к инфекционисту по месту жительства, он назначит препараты.
Ольга Н.: Ребенку 2 года. Даже после небольшого количества выпитого или съеденного появляется отрыжка. Порой донимает икота.
— Отрыжка и икота — симптомы патологии, в т. ч. со стороны ЖКТ. Требуется осмотр специалистом, который установит, нет ли заболевания. Вероятные причины отрыжки — малыш много разговаривает во время еды, пьет газированные напитки, заражен хеликобактер пилори.
Людмила: Какое увеличение печени у ребенка до года считается нормой?
— Увеличение печени не может быть нормой. Причины этого состояния нужно выяснить. Рекомендую посетить педиатра
Светлана Стаховская
Фото: Евгений Креч
Медицинский вестник, 22 октября 2015
Усиление сосудистого рисунка печени что это значит
Показаниями для исследования печени являются многие клинические симптомы и жалобы больного. Обследование проводится при болях в животе, отравлении, травме, желтушном синдроме, анемии, сахарном диабете, ожирении, изменении показателей биохимических проб, выявлении вирусных гепатитов, описторхоза и т.д.
Одной из частых причин направления в ультразвуковой кабинет остается увеличение органа /гепатомегалия/, когда врачи пальпируют печень под правой реберной дугой. Это не является истинным признаком увеличения печени, поскольку она может пальпироваться у некоторых людей с астеническим телосложением и смещаться по различным причинам, не связанным с патологией этого органа. Для исключения или подтверждения гепатомегалии используется два параметра величина правой доли, КВР не более 150 мм, толщина не более 130 мм, левая доля в соотношении 1,5-1,7 к правой, но не более 90 мм.
Следующим параметром оценивается эхогенность паренхимы печени, в норме она средняя. Оценка этого параметра целиком базируется на опыте врача исследователя и некоторых технических нюансах настройки аппарата. Все участки печени, лежащие непосредственно под датчиком и наиболее удаленные от него, должны иметь одинаковый цвет и яркость(эхогенность).
Еще одним важным признаком считается звукопроводимость органа, которая в норме является хорошей и при исследовании возможно отчетливо видеть все отделы печени и подпеченочного пространства. Чем больше изменений присутствует в ткани, тем хуже ее звукопроводимость и, соответственно видимость глубоких отделов и структур. Наоборот при отеке и значительных воспалительных процессах звукопроводимость усиливается до появления лучистости.
1. Острый
• Инфекционный. Например, вирусный, бактериальный, паразитарный или вследствие вторичного токсического эффекта какой-либо инфекции.
• Токсический. Алкоголь, химикаты, токсины, лекарства и их метаболиты.
2. Хронический
• Гранулематозный. Первичный и вторичный, билиарный цирроз, туберкулез, шистоплазмоз, саркоидоз.
• Негранулематозный, Реакция на лекарства, персистирующий, активный гепатит, часто вирусный.
Современная классификация гепатитов, принятая Международным конгрессом гастроэнтерологов в Лос-Анжелесе (1994), предусматривает выделение четырех видов хронических гепатитов по этиологическому признаку: вирусный, аутоиммунный, лекарственный и криптогенный. Появление некрозов и узлов регенерации является признаком развития цирроза печени.
Ультразвуковые признаки гепатита:
В зависимости от причины возникновения, давности, тяжести и стадии заболевания печени могут происходить самые различные изменения ультразвуковой картины гепатита. Различают два наиболее характерных описания изображений гепатита с самыми различными вариациями.
Форма печени не изменяется, контуры ровные, четко очерченные.
Увеличение/гепатомегалия/ правой доли печени
Определяется снижение эхогенности паренхимы печени или, реже, повышение ее эхогенности. При снижении эхогенности определяется симптом «звездное небо»: видна темная печень.
Диффузное понижение эхогенности паренхимы печени отмечается значительно реже, поскольку нет его четких визуальных признаков. Это состояние встречается в острой фазе гепатитов. Можно отметить при этом значительное усиление сосудистого рисунка за счет утолщения и повышения эхогенности стенок веточек воротной вены, повышения эхогенности околососудистой ткани. Сосуды прослеживаются вплоть до капсулы печени.
Звукопроводимость повышается.
Структура неоднородная за счет участков повышенной и пониженной эхогенности.
При усугублении процесса клиницисты отмечают симптом «тающей льдинки, появляются очаговые некрозы, размеры могут начать уменьшаться, но чаще гепатит переходит в хроническую форму.
При хроническом гепатите печень может выглядеть обычно.
Форма и контуры чаще всего не изменяются.
Увеличение обеих долей печени.
Отмечается повышение эхогенности паренхимы, реже — эхогенность снижается. При хроническом гепатите возможно незначительное диффузное повышение эхогенности паренхимы, но оно заметно отличается от такового при жировой инфильтрации из за структурной перестройки. Это выражается в наличии мелких гиперэхогенных включений в паренхиме печени, сохранности сосудистого рисунка. Причем рисунок может быть подчеркнут из за околососудистого фиброза.
Постепенно снижается звукопроводимость и визуализация глубоких участков.
В отличие от цирроза границы участков неоднородности неотчетливые.
В целом, структура изменений в печени может меняться в зависимости от стадии патологического процесса, особенно в том случае, когда острый гепатит переходит в хронические формы, периоды обострения сменяются периодами ремиссии(улучшения). Следующим этапом перерождения печени является цирроз.
Неалкогольная жировая болезнь печени: клиника, диагностика и лечение
В настоящее время неалкогольная жировая болезнь печени (НЖБП) является одним из самых распространенных заболеваний в гепатологии, приводящим к ухудшению качества жизни, инвалидизации и смерти. В первую очередь, это обусловлено высоким риском прогрессирова
В настоящее время неалкогольная жировая болезнь печени (НЖБП) является одним из самых распространенных заболеваний в гепатологии, приводящим к ухудшению качества жизни, инвалидизации и смерти. В первую очередь, это обусловлено высоким риском прогрессирования НЖБП с развитием неалкогольного стеатогепатита (НАСГ), печеночной недостаточности и гепатоцеллюлярной карциномы. Общая распространенность НЖБП в популяции колеблется от 10 до 40%, тогда как частота НАСГ составляет 2–4% [1, 2, 3].
Эпидемиология и патогенез НЖБП
Понятие НЖБП объединяет спектр клинико-морфологических изменений печени, представленных стеатозом, НАСГ, фиброзом и циррозом, развивающихся у пациентов, не употребляющих алкоголь в гепатотоксичных дозах (не более 40 г этанола в сутки для мужчин и не более 20 г — для женщин). НЖБП встречается во всех возрастных группах, но наибольшему риску ее развития подвержены женщины в возрасте 40–60 лет с признаками метаболического синдрома (МС) [4, 5].
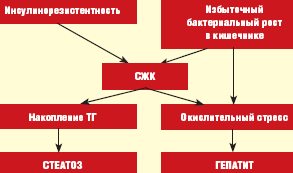
Патогенез НЖБП тесно связан с синдромом инсулинорезистентности (ИР), вследствие которого в печени накапливаются триглицериды (ТГ) и формируется жировой гепатоз (ЖГ) — первый этап или «толчок» заболевания. В последующем происходит высвобождение из жировой ткани и синтез de novo в гепатоцитах свободных жирных кислот (СЖК), способствующих возникновению окислительного стресса, являющегося вторым «толчком» заболевания и приводящего к развитию воспалительно-деструктивных изменений в печени в виде стеатогепатита [6].
Максимальный риск развития НЖБП отмечен в группе лиц с МС — это пациенты с сахарным диабетом (СД) 2 типа, ожирением, гипертриглицеридемией. Частота НЖБП у больных СД 2 типа и ожирением по данным различных исследований варьирует от 70 до 100%. При этом СД 2 типа или нарушение толерантности к глюкозе (НТГ) отмечаются у 10–75%, ожирение — у 30–100%, гипертриглицеридемия — у 20–92% пациентов с НЖБП [1, 4, 7, 8]. В то же время признаки НЖБП обнаруживаются у 10–15% людей без клинических проявлений МС, что может быть обусловлено другими патогенетическими механизмами формирования НЖБП, например, синдромом избыточной пролиферации бактерий в кишечнике или дисбиозом, как это принято формулировать в отечественной литературе [5, 10].
Основные механизмы развития НЖБП при кишечном дисбиозе связаны с нарушением синтеза апо-липопротеидов классов А и С, являющихся транспортной формой для ТГ в процессе образования липопротеидов очень низкой плотности (ЛПОНП), а также кишечным эндотоксикозом, что позволяет рассматривать это состояние в качестве дополнительного источника окислительного стресса (рис.) [11, 12].
Взаимосвязь патогенеза НЖБП с ИР позволяет считать это заболевание одним из независимых компонентов МС, клиническая значимость которого заключается в значительном прогрессировании атеросклеротического поражения сосудов.
В ряде работ показано, что НЖБП повышает риск возникновения сердечно-сосудистых заболеваний (ССЗ) независимо от других предикторов и проявлений МС [13]. Это подтверждается несколькими фактами, к которым относится связь НЖБП с концентрацией адипонектина в плазме. Известно, что адипонектин обладает антиатерогенным действием и по данным многих проспективных исследований снижение его уровня является ранним предиктором ССЗ и МС. У пациентов с НЖБП была отмечена более низкая концентрация адипонектина в плазме, чем у здоровых лиц [13].
Кроме этого, у указанной категории больных по сравнению с контрольной группой отмечается значительное увеличение толщины интимы (ТИ) сонной артерии, которое также признано достоверным субклиническим признаком атеросклероза. Доказано, что величина ТИ менее 0,86 мм связана с низким риском ССЗ, а более 1,1 — с высоким. У пациентов с НЖБП ее значение составляет в среднем 1,14 мм [14–18].
Другим субклиническим признаком атеросклероза, обнаруженным у больных НЖБП, служит выявление эндотелиальной дисфункции, что подтверждается снижением эндотелийзависимой вазодилатации плечевой артерии у пациентов с НЖБП. При этом уменьшение этого показателя коррелирует со степенью морфологических изменений в печени независимо от пола, возраста, ИР и других компонентов МС [19, 20].
Таким образом, патогенез НЖБП неразрывно связан с МС, а сам факт развития указанной патологии изменяет прогноз для этих пациентов, как в виде прогрессирования печеночной недостаточности, так и в виде значительного увеличения частоты осложнений ССЗ.
Клиника и диагностика
В целом для НЖБП характерно бессимптомное течение, поэтому наиболее часто в практике врач сталкивается со случайно обнаруженным при биохимическом исследовании синдромом цитолиза. При этом пациент с НЖБП, как правило, либо не предъявляет жалоб, либо они являются неспецифичными в виде астеновегетативного синдрома (слабость, утомляемость) и дискомфорта в правом подреберье. Наличие кожного зуда, диспепсического синдрома, наряду с развитием желтухи и портальной гипертензии, свидетельствует о далеко зашедшей стадии НЖБП [2, 3].
При объективном осмотре больных НЖБП обращают на себя внимание гепатомегалия, которая встречается у 50–75%, и спленомегалия, выявляемая у 25% пациентов [4].
При лабораторном исследовании для НЖБП характерны следующие изменения:
Основным дифференциальным отличием ЖГ от НАСГ, доступным в клинической практике, может быть выраженность биохимического синдрома цитолиза.
Следует отметить, однако, что отсутствие изменений лабораторных показателей, характеризующих функциональное состояние печени (АЛТ, АСТ, ЩФ, ГГТП), не исключает наличия воспалительно-деструктивного процесса и фиброза [10].
Как указывалось выше, диагностический поиск проводится в связи с выявлением у больного синдрома цитолиза, при этом наличие у него СД 2 типа, абдоминального ожирения, артериальной гипертензии и нарушения липидного обмена свидетельствует о высокой вероятности НЖБП. Постановка этого диагноза достаточно сложна ввиду необходимости исключения всех других причин, вызывающих цитолиз, макровезикулярный стеатоз и воспалительно-деструктивные изменения в печени. Следует исключить вторичный характер поражения печени (табл. 1) [2].
Для уточнения диагноза могут использоваться инструментальные методы (ультразвуковое исследование (УЗИ), компьютерная томография (КТ), магнитно-резонансная томография (МРТ)), которые позволяют верифицировать гепатомегалию, косвенно оценить степень стеатоза печени и зарегистрировать формирование портальной гипертензии.
УЗИ является недорогим и, по мнению некоторых авторов, достаточно информативным инструментальным методом диагностики стеатоза печени. Выделяют 4 основных ультразвуковых признака стеатоза печени:
К преимуществам УЗИ относится также возможность регистрировать динамику признаков стеатоза, в том числе на фоне лечения [20].
При проведении КТ печени основными признаками, свидетельствующими о наличии стеатоза, являются:
В целом КТ менее информативна, чем УЗИ при диффузных поражениях печени, однако она является методом выбора при очаговых заболеваниях [23].
Преимуществами современной высокопольной МРТ по сравнению с другими методами визуализации являются: высокая тканевая контрастность изображения за счет выгодного соотношения сигнал–шум, возможность получения целостного изображения органа в любой проекции, а также большие ресурсы программного обеспечения, используемые для дифференциальной диагностики.
Однако все визуализационные методы диагностики, несмотря на достаточно высокую информативность, не позволяют оценить наличие признаков стеатогепатита, степень его активности и стадию фиброзных изменений в печени [24, 25]. Поэтому с целью верификации диагноза необходимо проведение пункционной биопсии.
Значение пункционной биопсии печени в клинической практике неоднозначно. С одной стороны, только биопсия печени позволяет провести дифференциальный диагноз между стеатозом и стеатогепатитом, оценить стадию фиброза и на основании гистологических данных прогнозировать дальнейшее течение заболевания, а также исключить другие причины поражения печени. Однако отсутствие информированности врачей о целесообразности, а пациентов о безопасности метода сдерживают активное внедрение пункционной биопсии в практику.
Помимо этого, до сих пор активно обсуждаются морфологические критерии НЖБП. До настоящего времени в практике широко использовалась классификация, предложенная Brunt Е. (1999, 2001), которая подразделяет НЖБП в зависимости от степеней стеатоза, активности воспаления и стадии фиброза печени:
I. Степени крупнокапельного стеатоза:
0 степень: нет стеатоза;
1 степень: стеатоз до 33% гепатоцитов;
2 степень: стеатоз 33–66% гепатоцитов;
3 степень: стеатоз более 66%.
II. Степени НАСГ:
1 степень (мягкий НАСГ) — стеатоз 1–2 степени, минимальная баллонная дистрофия в 3 зоне ацинуса, лобулярное воспаление — рассеянная или минимальная лимфоплазмоцитарная инфильтрация, портальное воспаление отсутствует или минимальное;
2 степень (умеренный НАСГ) — стеатоз любой степени (крупно- и мелкокапельный), умеренная баллонная дистрофия в 3 зоне ацинуса, мягкое или умеренное портальное и лобулярное воспаление в 3 зоне ацинуса, может быть перисинусоидальный фиброз;
3 степень НАСГ (тяжелый НАСГ) — панацинарный стеатоз (смешанный), выраженная баллонная дистрофия, выраженное лобулярное воспаление, мягкое или умеренное портальное воспаление.
III. Стадии фиброза:
1 стадия — перисинусоидальный/перицеллюлярный фиброз в 3 зоне ацинуса, очаговый или распространенный;
2 стадия — перисинусоидальный/перицеллюлярный фиброз в 3 зоне ацинуса, очаговый или распространенный перипортальный фиброз;
3 стадия — очаговый или распространенный мостовидный фиброз;
4 стадия — цирроз печени [26].
Однако, по мнению ряда авторов, эта классификация не отражает целый спектр морфологических признаков, выявляемых у больных НЖБП при гистологическом исследовании. Недавно на основе существующей классификации была разработана и предложена Шкала активности НЖБП (NAFLD activity score — NAS), представляющая комплексную оценку морфологических изменений в баллах и объединяющая такие критерии, как стеатоз (0–3), лобулярное воспаление (0–2) и баллонную дистрофию гепатоцитов (0–2). Сумма баллов менее 3 позволяет исключить НАСГ, а более 5 свидетельствует о наличии у пациента гепатита. Данная шкала используется преимущественно для оценки эффективности лечения НЖБП, поскольку позволяет определить достоверность динамики морфологических изменений на фоне терапии за относительно короткий период времени [27].
В тех случаях, когда выполнение пункционной биопсии невозможно, диагноз НЖБП устанавливается в соответствии с алгоритмом, позволяющим пошагово исключить другие заболевания печени (табл. 2).
В связи с тем, что все пациенты с МС относятся к группе риска развития НЖБП, то больные с ожирением, СД 2 типа или НТГ, нарушением липидного обмена нуждаются в дополнительном обследовании, включающем клинические, лабораторные и инструментальные методы диагностики НЖБП и, в особенности, НАСГ. Однако до настоящего времени НЖБП и ее проявления не входят ни в критерии постановки диагноза МС, ни в алгоритм обследования больных с подозрением на его наличие (табл. 3).
Скрининг больных на стадии доклинических проявлений МС включает:
С учетом частоты, роли и значения НЖБП, в алгоритм обследования больных с МС должны входить клинико-лабораторные и инструментальные методы, позволяющие оценить морфофункциональное состояние печени:
Обязательными показаниями для биопсии являются:
Оценивать течение НЖБП возможно на основании данных гистологического исследования печени. Однако когда выполнение биопсии недоступно, существуют предикторы, позволяющие предположить высокий риск прогрессирования НЖБП с развитием гепатита и фиброза, которые были установлены при проведении статистической обработки результатов большого количества наблюдений [28–30].
Выявление более 2 критериев свидетельствует о высоком риске фиброза печени.
Для формулировки полноценного клинического диагноза необходимо учитывать данные клинико-лабораторного и инструментального обследования, выявление факторов неблагоприятного течения заболевания и других компонентов МС. Поскольку диагноз «неалкогольная жировая болезнь печени» в МКБ-10 (ВОЗ, 1998) пока отсутствует, его формулировка практическими врачами может производиться с учетом правил диагностики алкогольной болезни печени и вирусных гепатитов. В диагнозе на первом месте лучше указывать ту нозологическую единицу, на фоне которой развилась НЖБП, далее идет форма заболевания (гепатоз или НАСГ), степень стеатоза (по данным УЗИ), активность гепатита и стадия фиброзных изменений в печени в случае проведения гепатобиопсии. Если морфологическое исследование не выполнялось, допустимым, как и при других заболеваниях печени, является заключение: неустановленный фиброз. Примеры диагностических заключений:
Лечение НЖБП
В связи с высокой вероятностью неблагоприятного течения НЖБП, особенно в сочетании с другими проявлениями МС, все больные независимо от тяжести заболевания нуждаются в динамическом наблюдении и лечении. Однако до сих пор не разработаны стандартизированные терапевтические подходы к ведению пациентов с НЖБП.
Используемые направления терапии больных НЖБП основываются на механизмах развития заболевания, к которым в первую очередь относятся синдром ИР и окислительный стресс, поэтому наиболее важными задачами у данной категории пациентов являются:
Диета. С учетом современных представлений об этиологии, патогенезе и факторах прогрессирования НЖБП больным рекомендуются следующие диетические принципы:
Для пациентов с избыточной массой тела и ожирением — снижение общей энергетической ценности пищевого рациона. Суточная калорийность подбирается индивидуально в зависимости от массы тела, возраста, пола, уровня физической активности с использованием специальных формул. Сначала рассчитывают количество калорий, необходимых для основного обмена:
18–30 лет: (0,06 × вес в кг + 2,037) × 240
31–60 лет: (0,034 × вес в кг + 3,54) × 240
старше 60 лет: (0,04 × вес в кг + 2,76) × 240
18–30 лет: (0,06 × вес в кг + 2,9) × 240
31–60 лет: (0,05 × вес в кг + 3,65) × 240
старше 60 лет: (0,05 × вес в кг + 2,46) × 240.
Полученное значение умножают на коэффициент физической активности (1,1 — низкая активность, 1,3 — умеренная, 1,5 — тяжелая физическая работа или активное занятие спортом) и получают калорийность суточного рациона. Для снижения массы тела из рассчитанной величины суточных энергозатрат вычитают 500–700 ккал. Однако минимальное потребление калорий в сутки должно быть не менее 1200 ккал для женщин и не менее 1500 для мужчин. Доказано, что снижение массы тела на 5–10% сопровождается уменьшением гепатоспленомегалии, активности АЛТ, АСТ и коррелирует с регрессированием стеатоза печени [4]. Следует учесть, что быстрая потеря веса может привести к развитию «острого» НАСГ с формированием портального фиброза, центральных некрозов на фоне значительного повышения воспалительной активности вследствие увеличения поступления СЖК в печень на фоне периферического липолиза [5, 31]. Для больных ожирением и НЖБП безопасным и эффективным является снижение массы тела на 500 г в неделю для детей и на 1600 г в неделю для взрослых [31].
Кроме этого, всем пациентам с НЖБП рекомендуется:
Физическая нагрузка. Обязательным условием лечения больных НЖБП является физическая нагрузка. Она оказывает положительный эффект на снижение массы тела и чувствительность к инсулину, при этом увеличивается поступление СЖК в мышечную ткань, где происходит их окисление, тем самым уменьшается ИР [4]. Степень снижения ИР, как правило, коррелирует с интенсивностью физических упражнений, которые рекомендуется проводить не менее 3–4 раз в неделю, продолжительностью 30–40 минут.
Повышение чувствительности клеточных рецепторов к инсулину. К базисным медикаментозным средствам лечения синдрома ИР у больных НЖБП могут быть отнесены инсулиновые сенситайзеры — бигуаниды (метформин) и тиазолидиндионы (пиоглитазон, росиглитазон) — препараты, повышающие чувствительность клеточных рецепторов к инсулину. Опыт применения данных лекарственных средств свидетельствует о положительном влиянии на клинико-морфологические проявления НЖБП в виде уменьшения активности показателей цитолитического синдрома, степени стеатоза и воспаления. Но в целом вопрос применения этих препаратов у больных НЖБП требует проведения дальнейших исследований, что обусловлено отсутствием адекватных методов контроля эффективности лечения (гепатобиопсия) в выполненных работах [32].
Гиполипидемические средства. Учитывая патогенез заболевания, у пациентов с НЖБП эффективным может оказаться применение гиполипидемических средств из группы фибратов. Однако результаты исследования с назначением клофибрата больным НЖБП показали его неэффективность [33]. Не следует забывать и о возможности развития фибрат-индуцированных гепатитов. В отношении статинов также существует ряд противопоказаний, связанных с их гепатотоксическим действием. В целом данные выполненных работ противоречивы и указывают на необходимость дальнейшего изучения возможности использования этих препаратов у пациентов с НЖБП.
Пентоксифиллин. Снижение концентрации тумор-некротизирующего фактора-a (TNFa) имеет значение для прогрессирования НЖБП. Обладая высокой биологической активностью, TNFa усиливает ИР и приводит к развитию окислительного стресса. Уменьшение его уровня в крови связано с регрессом клинических и морфологических проявлений НЖБП. Подобный эффект был обнаружен у пентоксифиллина. Назначение этого препарата у пациентов с НАСГ в суточной дозе 1200 мг на протяжении 12 месяцев было связано со снижением показателей цитолитического синдрома и достоверным улучшением гистологических показателей у 67% больных [34].
Антагонисты рецепторов ангиотензина II. Формирование данного подхода обусловлено ролью ангиотензина в прогрессировании НАСГ. Установлено, что он, способствуя пролиферации миофибробластов, клеточной миграции, синтезу коллагена и провоспалительных цитокинов, активирует процессы фиброгенеза в печени. Поэтому в настоящее время исследуется возможность применения блокаторов ангиотензиновых рецепторов у пациентов с НЖБП. Так, прием лозартана у пациентов с НАСГ и артериальной гипертензией в суточной дозе 50 мг в течение 38 недель приводил к достоверному снижению АЛТ и ГГТП, что сочеталось с уменьшением степени стеатоза и воспалительной активности [35].
Антиоксиданты. Применение антиоксидантов у больных НЖБП оправдано наличием окислительного стресса, что подтверждается повышением в плазме у больных НАСГ маркера окислительного стресса — тиоредоксина и снижением концентрации антиоксидантных факторов. В настоящее время активно изучается возможность использования витамина Е, эффективность которого была продемонстрирована в ряде исследований [36]. Также имеется ряд зарубежных и отечественных работ, посвященных оценке влияния УДК на морфофункциональное состояние печени. Механизмы действия этой гидрофильной кислоты связаны с тем, что, нормализуя гепатоэнтеральную циркуляцию желчных кислот и целого ряда биологически активных веществ, вытесняя токсичные желчные кислоты, она способствует ликвидации избытка холестерина в гепатоцитах, путем уменьшения его синтеза и всасывания из кишечника. УДК также обладает цитопротективным и антиапоптотическим действием, препятствуя развитию окислительного стресса, что позволяет применять ее на обоих этапах НЖБП [33].
В отношении АЛК установлено, что она обладает плейотропным действием на весь организм, оказывая положительное влияние на энергетический, липидный (тормозит синтез холестерина, подавляя высвобождение СЖК из жировой ткани, что предупреждает развитие стеатоза гепатоцитов) и углеводный (снижает ИР, усиливает захват и утилизацию глюкозы клеткой, повышает чувствительность клеточных рецепторов к инсулину) виды обменов.
Кроме этого, АЛК, имея низкий оксислительно-восстановительный потенциал, обладает мощным антиоксидантным эффектом, действуя непосредственно на печень, способствует повышению детоксицирующих субстанций в гепатоцитах (восстанавливает глутатион) и улучшению морфологических изменений [36].
Восстановление микробиоценоза кишечника. К сожалению, большинство работ, подтверждающих патогенетическую роль дисбиоза кишечника в формировании НЖБП и эффективность антибактериальных препаратов в лечении указанной нозологии, относится к 80–90-м годам прошлого столетия.
Поэтому вопрос проведения санации кишечника антибактериальными препаратами остается открытым. Антибиотики рекомендуются только при наличии верифицированной чувствительной условно-патогенной флоры в кишечнике или формировании заболевания после оперативного лечения на брюшной полости, например «синдрома приводящей петли». Преимуществом выбора при этом принадлежит препаратам, обладающим способностью хорошо накапливаться в желчи с эффектом вторичного прохождения через желудочно-кишечный тракт, к которым относятся фторхинолоны первого поколения (ципрофлоксацин). Также могут использоваться кишечные антисептики, типа метронидазола или нифуроксазид, и невсасывающиеся в кишечнике препараты, например рифаксимин.
Во всех остальных случаях, когда нет показаний для применения антибиотиков, кишечную санацию у больных НЖБП следует проводить пребиотиками, а препаратом выбора в данном случае является Эубикор. Его преимуществом является сбалансированный состав, куда входят пищевые волокна и винные дрожжи (S. vini). Кроме мощного пребиотического эффекта, Эубикор обладает хорошими сорбционными свойствами, что позволяет не только восстанавливать нормальную микрофлору, но и проводить дезинтоксикацию. По результатам исследований, прием Эубикора у данной категории пациентов способствовал дополнительному уменьшению дислипопротеидемии и повышению чувствительности к инсулину [37, 38].
Лечение неалкогольного ЖГ
В целом требования, предъявляемые к лекарственным средствам, используемым в лечении НЖБП, достаточно высоки. В первую очередь, они должны быть максимально безопасны с точки зрения гепатотоксичности, также желательно их позитивное действие на улучшение клинико-лабораторных и морфологических изменений в печени.
Собственный опыт лечения больных НЖБП на стадии гепатоза состоит в использовании комбинации АЛК с Эубикором. АЛК (препарат «Берлитион», производитель — Берлин-Хеми, Германия) назначалась по 600 ЕД внутривенно в течение 14 дней, с переходом на пероральный прием в той же суточной дозе, однократно в течение 6 месяцев. Эубикор назначался по 2 пакетика 3 раза в день во время еды. Результаты работы показали положительное влияние Берлитион и Эубикора не только на показатели липидного и углеводного обменов, но и на степень жировой дистрофии в печени по результатам ультразвукового и морфологического исследований. Положительная динамика указанных изменений имеет значение как для формирования системной ИР, являющейся основной причиной развития МС, так и для течения собственно НЖБП и развития НАСГ. Поэтому данные препараты, наряду с немедикаментозной терапией, могут рассматриваться как средства базисной терапии первой стадии НЖБП — ЖГ.
Лечение НАСГ
При развитии у пациентов НАСГ терапия заболевания усиливалась дополнительной комбинацией метформина (препарат «Сиофор», производитель — Берлин-Хеми, Германия) в дозе 1500 мг в сутки с УДК (препарат «Урсосан» фирмы PRO.MED.CS Praha a.s.) в дозе 15 мг на 1 кг массы тела, с однократным приемом через час после ужина. Длительность лечения подбиралась индивидуально, как правило, она составляла не менее 6 месяцев, иногда достигая 12 и более месяцев. Продолжительность курса зависела от выраженности клинических проявлений, комплайнса и динамики лабораторно-инструментальных показателей на фоне лечения. Назначение этих препаратов сопровождалось уменьшением не только клинико-лабораторных проявлений заболевания, но и достоверно способствовало улучшению гистологической картины печени. При этом комбинированная терапия у данной категории пациентов являлась методом выбора, поскольку именно в группе, получавшей одновременно Сиофор, Берлитион и Урсосан, динамика показателей синдромов цитолиза, холестаза, а также жирового и углеводного обменов была более значимой. На фоне лечения у больных НАСГ также отмечалось обратное развитие жировой дистрофии, достоверно уменьшилась выраженность воспалительных изменений и отсутствовало прогрессирование стадии фиброза в печени. Таким образом, комбинированная терапия воздействует на основные этиопатогенетические механизмы формирования метаболических нарушений, приводит к улучшению показателей липидного и углеводного обменов в виде нормализации уровней ЛПВП, ТГ и индекса ИР у пациентов с НАСГ.
Предложенная схема лечения НЖБП не является стандартизированной, но она патогенетически обоснована, а ее рабочий вариант может рассматриваться как применение:
На практике рациональный выбор того или иного препарата может определяться сочетанием НЖБП с другими компонентами МС.
Рекомендуемые алгоритмы выбора терапии пациентов с НЖБП и ожирением:
ИМТ менее 40 кг/м 2 :