уксуснокислый натрий что это такое
Ацетаты натрия (Е262)

Характеристика химических свойств и способа получения добавки Е262
По своей структуре ацетаты натрия – это соли уксусной кислоты, так как именно из этого сырья её и получают: карбонаты или гидроксиды натрия подвергают реакции с кислотой. Как ни странно, часть производство вещества связано с перегонкой и обработкой древесины.
Добавка имеет вид кристаллического порошка, которое имеет слабый запах уксуса. Может иметь белесоватый, светло-жёлтый или коричневый оттенок. Вещество хорошо растворимо в воде, хуже – в спиртах и эфире. Кроме того, оно не подвержено горению.
Основные свойства ацетатов натрия, за которые его так ценят промышленники – это способность к регуляции уровня кислотности химической среды, консервации и стабилизации веществ. Добавка помогает сохранить форму и текстуру продуктов, их вкусовые и ароматические характеристики, способна улучшить консистенцию сырья.
Немногие добавки могут похвастаться тем, что они встречаются в живой природе. Как раз ацетаты натрия могут: они существуют как элемент клеток животных и растений, как составляющая кислот во фруктах, присутствует в кисломолочных продуктах как результат ферментации бактерий.
Области применения вещества человеком
Существует несколько видов ацетатов натрия: технический и пищевой. Первую разновидность используют в производстве химических грелок и обогревателей, как составную часть смеси “горячий лёд”. В сфере строительства ацетаты натрия дают противоморозный эффект для бетона, используются при возведении монолитных конструкций.
Текстильная промышленность применяет вещество при окрашивании тканей и дублении кожи. Также добавка используется в сфере фотографии и гальванотехники, в производстве красящих продуктов, средств гигиены, в химической отрасли.
По своей структуре технический ацетат натрия – это тригидрат натриевой соли уксусной кислоты, который имеет вид чешуек или кусочков различных форм.
Вообще человеку знакомы два типа добавки Е262:
Вещества имеют различные химические формулы, но мало отличаются друг от друга по своим свойствам.

В медицинской промышленности добавка применяется в изготовлении мочегонных препаратов и других лекарств.
Требования к упаковке добавки Е262
В любом из видов упаковки внутри должен быть дополнительный подклад из плотного пищевого полиэтилена. Так как вещество очень подвержено реакции с водой, на таре обычно ставят отметку “Беречь от влаги”.
Чаще всего ацетаты натрия хранятся и транспортируются в пищевых мешках из ткани (в таких обычно можно видеть муку и крупы). Также для этих целей используются ящики из гофрированного картона или многослойные бумажные пакеты, бочки, контейнеры.
Влияние на здоровье человека
По различным данным, вред от употребления продуктов с ацетатами натрия в составе колеблется от крайне незначительного уровня до среднего.
На сегодня официально добавка разрешена в США, Канаде, Европейском союзе, Украине, России, Австралии. Нет никаких официальных данных по поводу возможной связи между её применением и появлением онкологических заболеваний, генных мутаций, бесплодия, отравлений, по крайней мере, при потреблении в тех количествах, в которых вещество используется в пищевых продуктах.
Зафиксировано несколько случаев появления аллергической реакции у людей, страдающих аллергией на уксус.
Тем, кто имеет проблемы с функционированием вегетативной системы, жёлчного пузыря, кишечника, в частности, дисбактериоз, печени, почек, сердечно-сосудистой системы, лучше воздержаться от питания едой с добавкой в составе.
Превышение нормальной суточной дозировки ацетатов натрия для взрослого человека может обернуться некоторыми неприятными симптомами: головной болью и головокружением, нарушением координации, болями и спазмами в животе, судорогами, удушьем, изменением цвета кожных покровов и слизистых на более бледный.
По некоторым неподтверждённым данным, вещество всё-таки имеет свойства канцерогена по причине того, что в кишечнике оно превращается в нитраты, которые могут провоцировать появление злокачественных опухолей, или, как минимум, мощной аллергии. Официального подтверждения этой информации мировому сообществу предоставлено не было, поэтому ацетаты натрия не признаны онкогенной или опасной добавкой.
Некоторые специалисты советуют ограничить поступление вещества в организм ребёнка, чтобы не вызвать у него появление аллергии.
Натрия ацетат считается безвредным веществом, и имеет широкую сферу применения, от производства кожаных изделий до приготовления картофельных чипсов. Он обладает выраженными свойствами консерванта и стабилизатора, однако от других консервантов отличается тем, что не угнетает рост и развитие бактерий, и выступает как фермент, образующийся в процессе жизнедеятельности этих бактерий в веществах.
Существуют некоторые ограничения в употреблении продуктов с веществом в составе для аллергиков, детей и людей с нарушениями в работе внутренних органов.
Процессы исследований действия ацетатов натрия на человека продолжаются до сих пор, а пока, в силу отсутствия значительного негативного влияния на организм здорового человека, мировым сообществом не было установлено нормы суточного потребления добавки Е262.
Ацетат натрия
| Ацетат натрия | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | sodium acetate (ИЮПАК) sodium ethanoate (систематическое) ацетат натрия натрия этаноат |
| Химическая формула | CH3COONa |
| Эмпирическая формула | C2H3O2Na |
| Физические свойства | |
| Состояние (ст. усл.) | белый гигроскопичный порошок |
| Молярная масса | 82.03 грамм/моль (безводная форма) 136.08 грамм/моль (тригидрат) г/моль |
| Плотность | 1,45 г/см³ |
| Термические свойства | |
| Температура разложения | 324 °C |
| Удельная теплота плавления | 264—289 к Дж/кг |
| Химические свойства | |
| Растворимость в воде | 76 г/100 мл |
Ацетат натрия CH3COONa, — натриевая соль уксусной кислоты, производится и широко применяется в промышленных масштабах.
Содержание
Область применения
Ацетат натрия используется в текстильном производстве для нейтрализации отработанной серной кислоты в сточных водах и как фоторезист при использовании анилиновых красителей. Также используется при дублении солями хрома (для протравливания), и замедляет процесс вулканизации хлоропрена при производстве синтетических резин.
Ацетат натрия известен как пищевая добавка E262 и применяется как консервант.
В растворе ацетат натрия (будучи солью слабой кислоты) и уксусная кислота могут применяться как буфер, для сохранения относительно постоянного pH. Это особенно полезно в биохимии в pH-зависимых реакциях.
На этом свойстве основан довольно красивый опыт — «горячий лёд»
Способы получения
Ацетат натрия недорог и его легче приобрести в хим. магазинах, чем синтезировать в лабораторных условиях. В лабораторных условиях получается при взаимодействии уксусной кислоты, например, с карбонатом натрия, гидрокарбонатом натрия или гидроксидом натрия.
Это — хорошо известная реакция «гашения» пищевой соды и винного уксуса, происходящая в тесте. 84 грамма гидрокарбоната натрия реагируют с 750 граммами 8 % винного уксуса (или же с 86 граммами 70 % уксусной эссенции) с образованием 82 грамм ацетата натрия в растворе. Выпариванием воды можно получить чистый кристаллический ацетат натрия или его концентрированный раствор.
Характерные реакции
Ацетат натрия может быть использован для образования эфира с алкил галогенидами такими как бромэтан:
При сильном нагревании (более 324 °C) ацетат натрия разлагается на карбонат натрия и ацетон:
Одновременно может проходить разложение до оксида натрия, ацетона и диоксида углерода:
Галерея
Химический обогреватель, содержащий перенасыщенный раствор ацетата натрия, выделяющего тепло при фазовом переходе в кристаллическую форму тригидрата ацетата натрия.
Натрий уксуснокислый — реактив, востребованный промышленностью в больших количествах
Натрий уксуснокислый (ацетат натрия, натрия этаноат) — органическое соединение, соль уксусной кислоты, традиционно называемая ацетатом. Формула CH3COONa или C2H3O2Na. 
Кристаллическое вещество с гигроскопичными кристаллами белого, светло-желтого, желтого, коричневого цвета; со слабым запахом уксуса. Водорастворимое, плохо растворяется в спиртах и эфирах.
Процесс кристаллизации экзотермический. При нагревании ацетат натрия разлагается с образованием ацетона и углекислого натрия. Считается малотоксичным, огне- и взрывобезопасен. Взаимодействует с кислотами. Реакция с серной кислотой приводит к образованию нерастворимого осадка — это свойство используется для нейтрализации серной кислоты. Образует сложные эфиры.
 |  |
| Натрий уксуснокислый (ацетат) б/в | Натрий уксуснокислый 3-вод. (ацетат) |
«Горячий лед», который используется в бытовых химических грелках, — это 3-водный ацетат натрия. Он плавится при температуре +58 °С. При помещении грелки в кипяток, вещество становится жидким, сохраняя это состояние и при комнатной температуре. Для начала процесса кристаллизации достаточно нажать на небольшой металлический диск внутри грелки. Он становится центром кристаллизации и запускает процесс. По мере кристаллизации реактива выделяется значительное количество тепла. Тепло выделяется до тех пор, пока все вещество внутри грелки не станет твердым (поэтому и называют — «горячий лед»). Чтобы вернуть грелку в исходное состояние, ее нужно опять прокипятить в воде, чтобы расплавить содержимое.
Натрий уксуснокислый
Натрий уксуснокислый (ТУ 2432-043-07510508-2003) (ацетат натрия) CH3COONa кристаллический технический. Ацетат натрия представляет собой кристаллическое вещество от светло-желтого до коричневого цвета. Уксуснокислый натрий (далее УКН) – негорючее, взрывобезопасное, малотоксичное, высокогигроскопичное вещество. Выпускается в твердом виде – 3% водный кристалл соли уксусной кислоты. Массовая доля безводной соли не менее 50%. Безобогревный способ бетонирования, основанный на введении противоморозных добавок, обеспечивает твердение бетонов при отрицательных температурах: с нитритом натрия до –15°С.; с ацетатом натрия (УКН) до –20°С. Противоморозная добавка уксуснокислого натрия обладает пластифицирующим эффектом (5 – 7%) и улучшает удобоукладываемость бетонной смеси. Не влияет отрицательно на процесс схватывания в бетонах, а также не усложняет приготовление, транспортирование и укладку бетонной смеси. Противоморозная добавка уксуснокислого натрия не вызывает коррозии арматуры в бетонах. Не снижает марку бетона по морозостойкости.
Нарастание прочности бетона с противоморозной добавкой уксуснокислого натрия при твердении при отрицательных температурах не уступает прочности бетона с добавкой нитрата натрия и составляет в 28-дневном возрасте 25,4% до 46,5% от марочной прочности для тяжелого бетона и от 62% до 80,7% для легкого керамзитобетона. Что соответствует требованиям нормативной документации.
[Противоморозные добавки для бетонов (второе поколение). Под ред. Ложкина В.П. Специализированный производственно-практический справочник. 2013 г.]
Полезное
Смотреть что такое «Натрий уксуснокислый» в других словарях:
уксуснокислый натрий — i Регулятор кислотности пищевого продукта, получаемый нейтрализацией уксусной кислоты карбонатом натрия или едким натром, содержащий основного вещества не менее 98,5 % по безводной соли, свинца не более 2 мг/кг, имеющий показатель активной… … Справочник технического переводчика
Натрий* — (хим.; нем. Natrium, франц. и англ. Sodium). Сведения о соединениях этого металла ведут свое начало от очень старых времен. Еврейское слово neter (греч. νίτρον, лат. nitrum) встречается в Библии как название вещества, которое, по Соломону,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Натрий — (хим.; нем. Natrium, франц. и англ. Sodium). Сведения о соединениях этого металла ведут свое начало от очень старых времен. Еврейское слово neter (греч. νίτρον, лат. nitrum) встречается в Библии как название вещества, которое, по Соломону,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
уксуснокислый натрий — ацетат натрия … Cловарь химических синонимов I
71.040.30 — Хімічні реактиви ГОСТ 8.134 98 ГСИ. Шкала рН водных растворов. Взамен ГОСТ 8.134 74 ГОСТ 8.315 97 ГСИ. Стандартные образцы состава и свойств веществ и материалов. Основные положения. Взамен ГОСТ 8.315 91 ГОСТ 61 75 Кислота уксусная. Технические… … Покажчик національних стандартів
Аппаратура, реактивы и растворы — 6.2. Аппаратура, реактивы и растворы Весы по ГОСТ 29329 или ГОСТ 24104. Фотоколориметр ФЭК 56М или спектрофотометр СФ 4, или другие аналогичные приборы. Цилиндры стеклянные вместимостью 250 см3 из прозрачного бесцветного стекла (внутренний… … Словарь-справочник терминов нормативно-технической документации
199 — ГОСТ 199 < 78>Натрий уксуснокислый 3 водный. Технические условия. ОКС: 17.040.30 КГС: Л52 Органические реактивы Взамен: ГОСТ 199 68 Действие: С 01.01.79 Изменен: ИУС 6/88, 2/95 Примечание: переиздание 1997 Текст документа: ГОСТ 199 «Натрий… … Справочник ГОСТов
2080 — ГОСТ 2080 < 76>Натрий уксуснокислый технический. Технические условия. ОКС: 71.080.99 КГС: Л21 Органические полупродукты Взамен: ГОСТ 2080 63, ГОСТ 5.998 71 Действие: С 01.01.77 Изменен: ИУС 7/86, 6/91 Примечание: переиздание 1992 Текст документа … Справочник ГОСТов
Растворы и реактивы — 5.2 Растворы и реактивы Натрий уксуснокислый 3 водный по ГОСТ 199, раствор массовой концентрации 0,5 г/см3. Кислота сульфосалициловая 2 водная по ГОСТ 4478, раствор массовой концентрации 0,2 г/см3. Соль динатриевая этилендиамин N,N,N¢,N¢… … Словарь-справочник терминов нормативно-технической документации
Ацетат натрия
| Ацетат натрия | |
|---|---|
 | |
| Систематическое наименование | sodium acetate (ИЮПАК) sodium ethanoate (систематическое) ацетат натрия натрия этаноат натрий уксуснокислый |
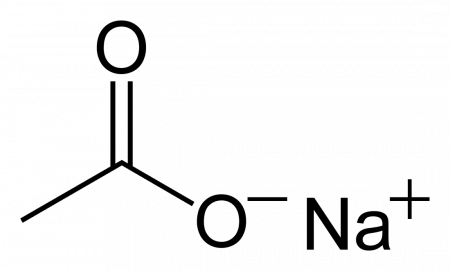
| Хим. формула | C2H3O2Na |
| Рац. формула | CH3COONa |
| Состояние | белый гигроскопичный порошок |
| Молярная масса | 82.03 грамм/моль (безводная форма) 136.08 грамм/моль (тригидрат) г/моль |
| Плотность | 1,45 г/см³ |
| Температура | |
| • плавления | 328 °C |
| • разложения | 324 °C |
| Удельная теплота плавления | 264—289 кДж/кг |
| Растворимость | |
| • в воде | 76 г/100 мл |
| Рег. номер CAS | 127-09-3 |
| PubChem | 517045 |
| Рег. номер EINECS | 204-823-8 |
| SMILES | |
| Кодекс Алиментариус | E262 |
| ChEBI | 32954 |
| ChemSpider | 29105 |
| Токсичность | ирритант, малотоксичен |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Ацетат натрия CH3COONa, — натриевая соль уксусной кислоты, кристаллы со слабым солёным вкусом и уксусным запахом, производится и применяется в промышленных масштабах.
Содержание
Область применения
Ацетат натрия используется в текстильном производстве для нейтрализации отработанной серной кислоты в сточных водах и как фоторезист при использовании анилиновых красителей. Также используется при дублении солями хрома (для протравливания), и замедляет процесс вулканизации хлоропрена при производстве синтетических резин.
Ацетат натрия известен как пищевая добавка E262 и применяется как консервант.
Также ацетат натрия является источником углерода для бактерий, выращиваемых на питательной среде.
В растворе ацетат натрия (будучи солью слабой кислоты) и уксусная кислота могут применяться как буфер, для сохранения относительно постоянного pH. Это особенно полезно в биохимии в pH-зависимых реакциях.
Ацетат натрия также используется в быту как составная химических грелок (англ. heating pad ) или химических обогревателей (англ. Hand warmer ), применяется как составная часть смеси «горячего льда» (англ. «hot ice» ), при кристаллизации ацетата натрия выделяется тепло — это экзотермический процесс. При нагреве тригидрата ацетата натрия (имеющего точку плавления в 58 °C) до 100 °C (обычно ёмкость с ним кладут в кипящую воду) он расплавляется (вернее, растворяется в собственной кристаллизационной воде) и переходит в водный раствор ацетата натрия. При охлаждении этого раствора образуется перенасыщенный раствор ацетата натрия в воде. Этот раствор прекрасно переохлаждается до комнатной температуры без образования твёрдой фазы, затем нажатием на металлический диск в ёмкости образуется центр кристаллизации, который, вырастая, заставляет перенасыщенный раствор переходить в твёрдую фазу тригидрата ацетата натрия. Этот процесс сопровождается значительным выделением тепла (экзотермическая реакция), теплота фазового перехода составляет 264-289 кДж/кг.
На этом свойстве основан довольно красивый химический опыт — «горячий лёд».
Способы получения
Это — хорошо известная реакция «гашения» пищевой соды и винного уксуса, происходящая в тесте. 84 г гидрокарбоната натрия реагируют с 750 г 8%-го винного уксуса (или же с 86 г 70%-й уксусной эссенции) с образованием 82 г ацетата натрия в растворе. Выпариванием воды можно получить чистый кристаллический ацетат натрия. Для получения тригидрата ацетата натрия без выпаривания необходимо смешать 84 г гидрокарбоната натрия (пищевой соды) с 86 г 70%-ной уксусной кислоты и 10 г воды.
Характерные реакции
Ацетат натрия может быть использован для образования сложного эфира по реакции с алкилгалогенидами, такими как, например, бромэтан:
При сильном нагревании (более 324 °C) ацетат натрия разлагается на карбонат натрия и ацетон:
2CH3COONa → Na2CO3 + (CH3)2CO
Влияние на организм
Ацетат натрия может всасываться в организм при проглатывании. Является ирритантом. LD50 25956 мг/кг. По другим данным из того же источника: LD50(крысы, орально): 3500 мг/кг, LD50(мыши, орально): 4960 мг/кг.