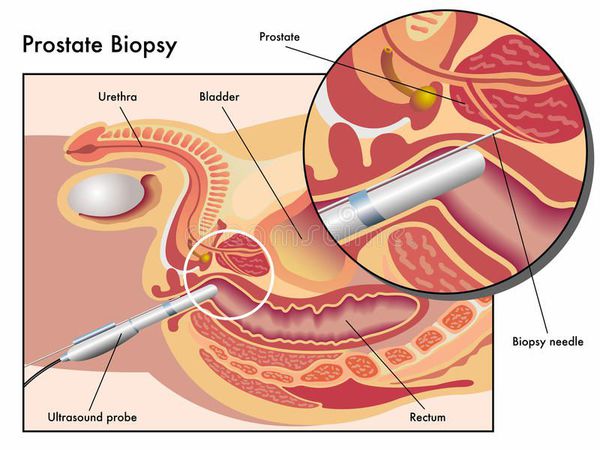
тумор простаты что это такое
Рак простаты у мужчин: прогнозы
Когда диагностируют рак простаты у мужчин, прогноз выживаемости зависит от формы рака, стадии развития опухоли, состояния здоровья и возраста больного. Выживаемость при раке простаты выше, если опухоль обнаружена на раннем этапе развития. Ранние стадии развития злокачественного новообразования относятся к локальным видам рака – опухоль не выходит за пределы органа, нет метастазов. Заболевание хорошо поддается лечению. Когда диагностирован метастазирующий рак простаты, последствия тяжелые – заболевание хуже поддается лечению, в костях, печени, легких, лимфатических узлах обнаруживаются метастазы опухоли, больной ослаблен, часто подавлен.
В Юсуповской больнице проводят лечение рака простаты на всех стадиях развития. Пациент проходит обследование у уролога, онколога, получает помощь психолога. В больнице пациент со злокачественными заболеваниями простаты может пройти диагностику на инновационном медицинском оборудовании, получить все виды медицинской помощи в зависимости от типа опухоли, стадии развития новообразования. В реабилитационном центре пациенты проходят восстановление по специальной программе для онкологических больных.
Симптомы рака простаты
Симптомы локального рака простаты на первой стадии – это небольшое увеличение предстательной железы, изредка возникает дискомфорт во время мочеиспускания. На стадии Т1а и 1b локальные опухоли простаты не пальпируются из-за небольшого объема новообразования, чаще всего представляют собой высокодифференцированные опухоли. В некоторых случаях определяется хорошо дифференцированный рак (обнаруживаются раковые клетки менее чем в 5% исследуемых тканей). Если ПСА находится в пределах нормы, устанавливают динамическое наблюдение за больным. Локальный рак простаты может представлять собой латентную форму рака, которая никогда не переходит в клинические формы заболевания.
Рак простаты на раннем этапе обнаруживается редко, основным методом, который помогает выявить злокачественное заболевание простаты на ранней стадии, считается тест ПСА. Характеристика злокачественной опухоли простаты по стадиям:
Лечение рака предстательной железы
Лечение рака на стадиях Т1с-Т2с проводится в зависимости от возраста больного. Хирургическое лечение рака простаты не показано мужчинам после 70 и старше. Не назначают хирургическое лечение пожилым мужчинам с сопутствующими раку простаты тяжелыми заболеваниями, при наличии высокодифференцированной опухоли. В большинстве случаев радикальная простатэктомия назначается молодым мужчинам. В старшем возрасте поддержка больного проводится с помощью лучевой терапии и химиотерапии. При повышении уровня ПСА после радикальной простатэктомии назначают адъювантную терапию. Повышение уровня ПСА указывает на развитие рецидива опухоли простаты или метастазы.
Третья стадия рака простаты характеризуется появлением стойкого нарушения мочеиспускания из-за увеличения простаты, располагающейся вокруг уретры. После проведения радикальной операции назначают адъювантную лучевую терапию при Т3 с показателями суммы Глисона больше 7 баллов, уровня ПСА более 10, если доказан местный рецидив опухоли простаты. Лучевая терапия показана пациентам с локальными формами рака простаты на первой и второй стадии заболевания, в случае невозможности или нежелания проведения хирургического лечения, а также больным со стадией Т3 и отсутствием метастазирования опухоли в регионарные и отдаленные лимфоузлы. Для проведения лучевой терапии пациент должен иметь прогноз долгой продолжительности жизни. Для повышения эффективности используют комбинированное лечение: лучевая терапия + гормональная терапия.
Использование адъювантной гормональной терапии оправдано у пациентов с диплоидными опухолями. Для лечения Т1-Т2 также применяют брахитерапию – облучение простаты путем введения радиоактивных гранул. Пациентам со стадией Т3 брахитерапию проводят в комплексе с наружным облучением. В случае если опухоль простаты обнаружена у мужчины в возрасте, при наличии сопутствующих тяжелых заболеваний, высокодифференцированном раке простаты в стадии Т1а, Т1с оправдано динамическое наблюдение. В случае прогрессирования опухоли принимается решение о методах лечения с учетом возраста, состояния здоровья больного.
3 степень: продолжительность жизни
2 степень: продолжительность жизни
Прогноз выживаемости при онкологии простаты
Рак предстательной железы – это тяжелое заболевание, которое бессимптомно протекает на ранних стадиях развития, агрессивные опухоли простаты развиваются стремительно, быстро приводят к смерти больного. Прогноз выживаемости при раке рассчитывается исходя из пятилетнего срока, в зависимости от стадии и агрессивности опухоли определяется прогноз пятилетней выживаемости больного. Прогноз составлен на основании выживаемости определенного процента пациентов после постановки первичного диагноза. В прогноз выживаемости не вошли пациенты, у которых в течение пятилетнего срока произошли рецидивы рака.
2 степень: продолжительность жизни
Средняя продолжительность жизни
Повышение уровня тестостерона в организме мужчины может привести к развитию гормонозависимого рака предстательной железы. Прогноз выживаемости при такой форме рака негативный. Опухоль отличается быстрым прогрессом, при появлении метастазов продолжительность жизни при раке простаты этого типа составляет не более 3-4 лет. Если обнаружена онкология предстательной железы, прогноз выживаемости составляется после полного обследования пациента, постановки диагноза.
В Юсуповской больнице проводится комплексная диагностика рака простаты. Определяется вид злокачественного заболевания и стадия развития опухоли. Диагностика заболевания проходит с помощью различных методов исследования:
В зависимости от показателей исследований, возраста, состояния здоровья пациента врач-онколог назначает лечение. В онкологическом отделении больницы применяют инновационные методы лечения рака простаты. Записаться на консультацию к врачу можно по телефону.
Рак простаты (предстательной железы)
Рак предстательной железы – одно из самых распространённых онкологических заболеваний. На его долю приходится более 14% всех злокачественных опухолей, диагностируемых у мужчин. Заболевание развивается медленно и может годами протекать без специфических симптомов. Зачастую новообразование выявляется только на 2 стадии или позднее, когда опухоль уже создает давление на уретру, и ее размеры можно прощупать при урологическом осмотре. Ранняя диагностика позволяет разработать эффективный план лечения и предотвратить опасные последствия – метастазы в костной ткани и внутренних органах.
Размеры и функции здоровой простаты
Аденома предстательной железы
Изменение структуры клеток с возрастом повышает риск развития рака простаты. Прямой связи между наличием аденомы простаты и перерастанием аденомы в рак простаты не обнаружено. Однако при выявлении доброкачественной гиперплазии предстательной железы рекомендуется регулярно проходить осмотр у уролога-андролога и контролировать уровень онкомаркера ПСА (простатспецифический антиген).
Рак предстательной железы
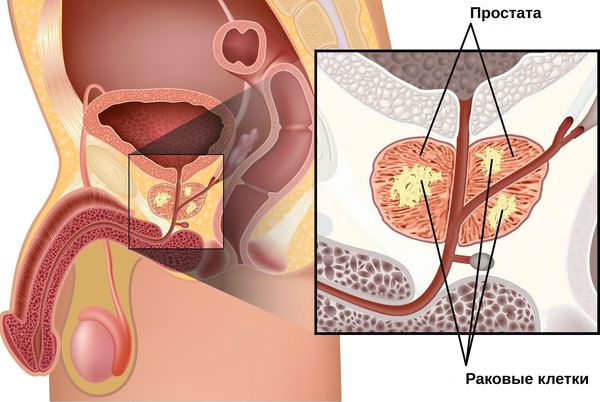
Рак простаты (аденокарцинома предстательной железы) – это злокачественное новообразование, развивающееся из клеток железистого эпителия или соединительной ткани. На ранних стадиях опухоль не выходит за пределы простаты и практически никак не проявляет себя.
Первые признаки рака простаты появляются по мере увеличения массы опухоли, когда она пережимает уретру и нарушает нормальный отток мочи. Без лечения опухоль способна прорастать через капсулу простаты и метастазировать в другие органы.
Очень важно своевременно отреагировать на тревожные симптомы, установить диагноз и начать терапию. Рак простаты относится к категории медленнорастущих опухолей и на незапущенных стадиях хорошо поддается лечению.
Причины рака простаты
Науке до сих пор не удалось со 100 % уверенностью установить истинные причины рака простаты. Основными факторами риска считаются возраст, наследственная предрасположенность, особенности питания (недостаток витамина A и β-каротина), курение. Более 70 % случаев впервые диагностированного рака простаты приходится на долю мужчин старше 65 лет.
При наличии наследственной предрасположенности в группу риска попадают мужчины после 45 лет. На своем опыте мы можем сказать, что рак простаты становится моложе. К нам нередко попадают пациенты в возрасте от 40 лет. Поэтому важность регулярных урологических обследований нельзя недооценивать, особенно если в семье встречались случаи заболевания раком простаты.
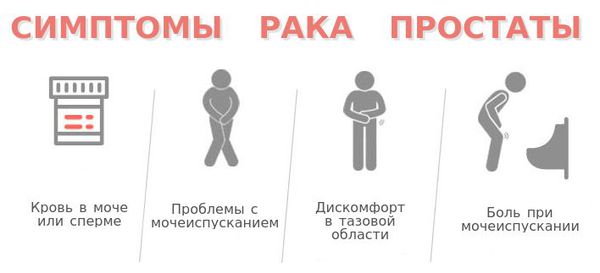
Симптомы рака простаты
• Струя мочи становится вялой;
• Долгое мочеиспускание;
• Частые позывы к мочеиспусканию, в т. ч. ночные;
• Незначительное количество мочи при мочеиспускании;
• Прерывистое выделение мочи в конце мочеиспускания;
• Ощущение неполного опорожнения мочевого пузыря;
• Ощущение жжения при мочеиспускании;
• Трудносдерживаемые позывы к мочеиспусканию, недержание.
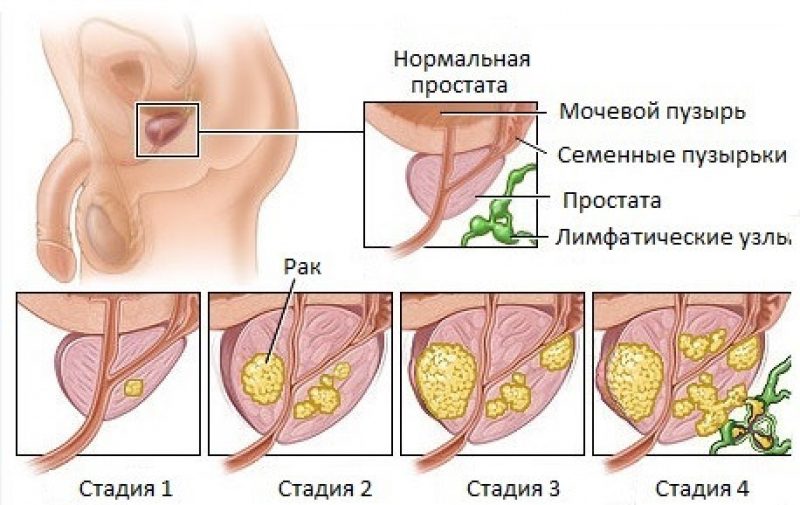
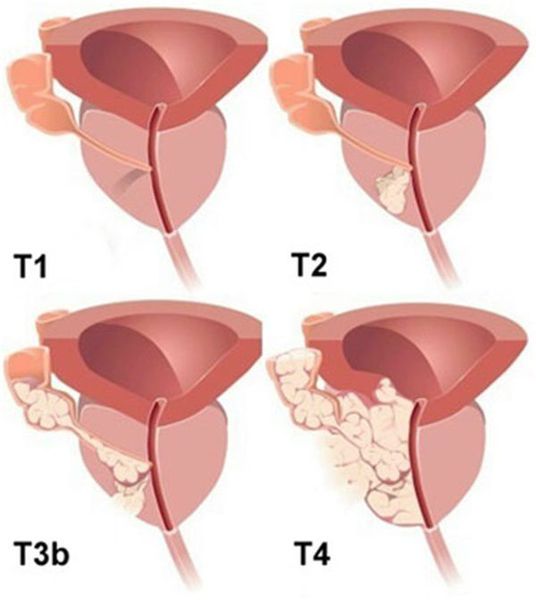
Стадии рака простаты
Классификация опухоли предстательной железы определяется по системе TNM и шкале Глисона (Gleason Score) после биопсии простаты, МРТ, КТ и других исследований.
TNM классификация
Любой вид рака имеет свою собственную TNM классификацию. Каждой из трех букв присваивается цифра, чтобы дать более точное описание каждой из градаций.
На основании точной TNM классификации лечащий врач может сделать прогноз и определить правильный вид лечения.
Рак простаты, классификация ТNМ
Tx: опухоль в простате не найдена.
T0: нет явных доказательств присутствия опухоли в простате.
T1: опухоль имеет крайне малый размер, не пальпируется и не видна на рентгеновских снимках;
T2: опухоль находится только в капсуле простаты;
T3: опухоль проросла за капсулу простаты;
T4: опухоль поразила близлежащие органы: кишечник, сфинктер, мышцы малого таза, стенку малого таза и т.д.
Nx: недостаточно данных для определения статуса лимфоузлов.
N0: отсутствие метастазирования в регионарные лимфоузлы.
N1: есть метастазирование в регионарные лимфоузлы.
T2aN0M0 означает что опухоль растет в одной доле простаты, лимфоузлы не затронуты и метастазирование в другие органы отсутствует.
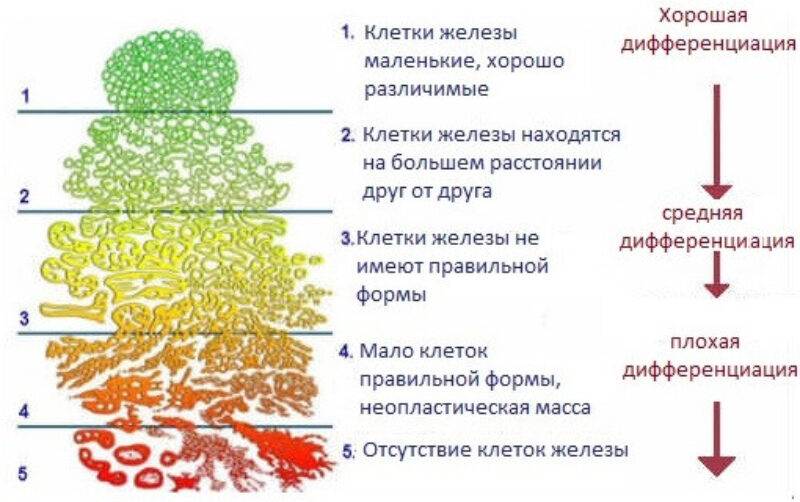
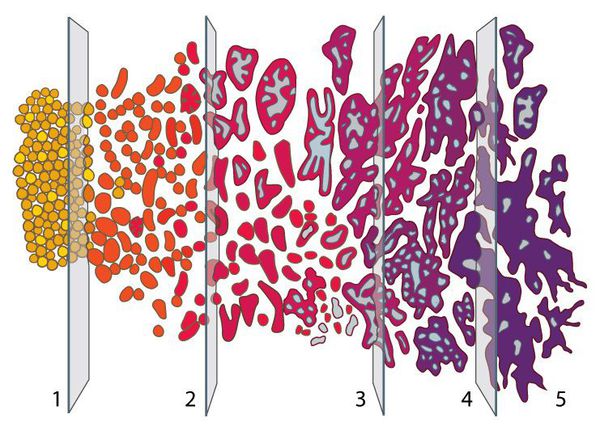
Шкала Глисона
Шкала Глисона используется для определения агрессивности опухоли предстательной железы. Чем меньше раковых клеток схожи с нормальными (здоровыми) клетками, тем выше значение шкалы Глисона и тем агрессивнее рак простаты.
Диагностика рака простаты
Урологическое обследование
Вы заметили у себя симптомы рака простаты? Сдайте кровь на ПСА и запишитесь на урологическое обследование.
Лечение рака простаты
Выбор методов лечения рака простаты у мужчин зависит от стадии заболевания, общей физической формы и особенностей конкретного пациента. На ранних стадиях может применяться высокоточная лучевая терапия (наружная или внутренняя, брахитерапия). Золотым стандартом в лечении рака предстательной железы считается радикальная простатэктомия. В некоторых случаях для замедления роста опухоли перед операцией может потребоваться гормональная терапия. Химиотерапия применяется при наиболее тяжелых формах рака предстательной железы с метастазированием в другие органы.
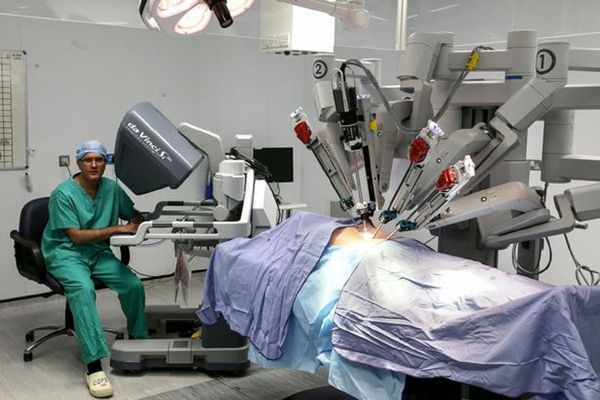
Радикальная роботизированная простатэктомия Да Винчи
Рак предстательной железы: почему возникает, симптоматика, методы диагностики и лечения
Введение
Согласно данным множества исследований, отмечается неуклонный рост случаев обнаружения первичного рака предстательной железы (РПЖ). В России это заболевание находится на 4-м месте среди всей онкологии, выявляемой во время профосмотров. Опережает его рак шейки матки, молочной железы и губы. В западных странах рак простаты составляет 25% от всех онкологических заболеваний.
Что такое рак простаты?
РПЖ представляет собой злокачественное новообразование, которое развивается из тканей предстательной железы.
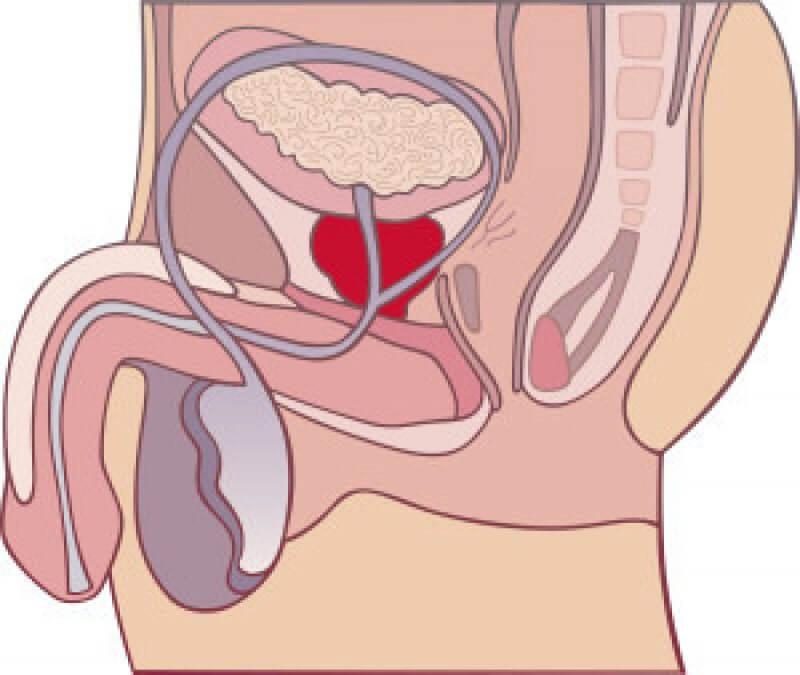
Предстательная железа, или простата, – мужской репродуктивный орган, по размерам схожий с каштаном. Он находится под мочевым пузырем и охватывает передний отдел мочеиспускательного канала.
Рис. 1. МРТ (Т2-взвешенные изображения) картина поражения левой доли предстательной железы.
Разновидности рака предстательной железы
В 95% случаев РПЖ развивается из эпителиальных клеток собственных желез (их называют «ацинусы»), из которых сформирована периферическая часть предстательной железы. Эта форма болезни называется «ацинарная аденокарцинома». В остальных 5% случаев диагностируется интрдуктальная разновидность, для которой характерно более агрессивное течение.
Важная характеристика аденокарциномы – степень ее дифференцировки, которая выявляется при гистологическом исследовании биоптата или биоматериала, полученного в ходе операции. Дифференцировка сегодня выражается шкалой Глисона (Gleason), в соответствии с которой присваивается сумма баллов: от 6 (самый благоприятный прогноз) до 10 (самый неблагоприятный вариант).
Характерные признаки заболевания
Риск развития РПЖ растет с возрастом: средний показатель в этой категории заболевших – 68 лет. Существуют также факторы риска, то есть то, что повышает шанс появления онкологического заболевания. Современной медициной не выявлены достоверные факторы, которые приводят к повышению риска развития РПЖ (какие-либо препараты, характер рациона, вредные привычки, плохая экология и др.). Поэтому основным фактором остается возраста, а также возрастной гормональный дисбаланс (между эстрогенами и андрогенами).
Симптоматика, первые признаки
На ранних стадиях злокачественная опухоль обычно не проявляет себя. Кроме аденокарциномы, у людей с повышенным риском развития РПЖ почти всегда присутствуют сопутствующие патологии (простатит, аденома простаты), и они могут давать симптоматику. Чаще всего встречаются следующие симптомы:
Таким образом, чем выше стадия, тем больше вероятность проявления симптоматики. Чаще всего РПЖ обнаруживается во время профилактического обследования (оно рекомендовано всем мужчинам старше 40-ка лет). Такое обследование включает в себя:
ПСА – это маркер, используемый для раннего выявления РПЖ. Он достаточно чувствителен и специфичен, чтобы заподозрить наличие рака на начальной стадии. Кроме ПСА, анализу могут подвергаться его производные – индекс здоровья простаты, плотность ПСА, соотношение свободного ПСА и общего.
Методы диагностики
Основа диагностики РПЖ – биопсия предстательной железы, иными словами, морфологическая верификация.
Показания к биопсии:
Важно! Если уровень ПСА ниже верхней допустимой границы, это не всегда говорит о том, что РПЖ отсутствует. Примерно 25% случаев заболеваемости отмечаются на фоне нормальных значений этого показателя. Поэтому решение о необходимости проведения биопсии должно приниматься после комплексного обследования, которое включает все виды диагностики.
Варианты биопсии простаты:
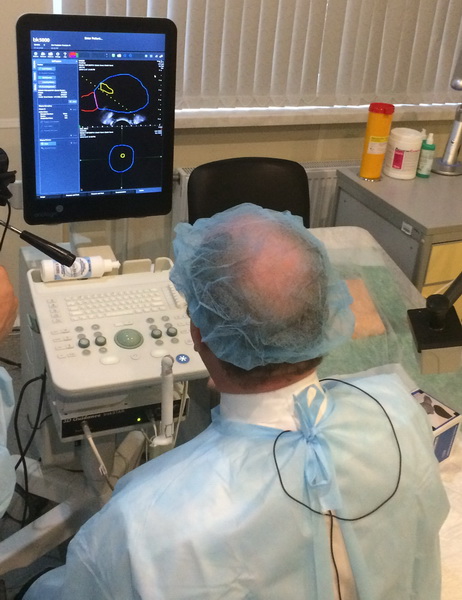
Рис. 2 А., 2 Б. Фьюжн-биопсия. Мастер-класс в НМИЦ онкологии им. Н.Н. Петрова
Стадии рака предстательной железы
Стадирование РПЖ и определение группы риска рецидивирования после возможной терапии производятся после гистологической верификации заболевания.
Стадирование при стандартном подходе подразумевает остеосцинтиграфию и МРТ органов малого таза. Магнитно-резонансная томография нужна, чтобы выявить степень локального распространения процесса в зоне простаты (прорастание в семенные пузырьки, выход новообразования за капсулу железы), а также определить, есть ли поражение регионарных лимфоузлов.
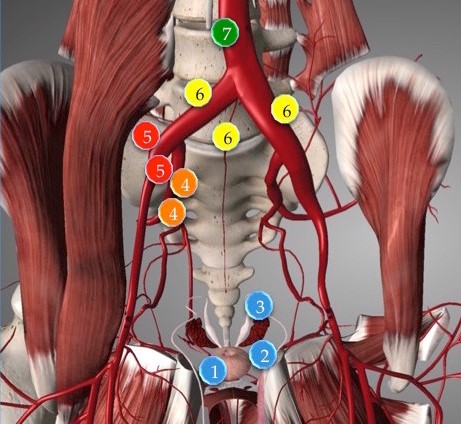
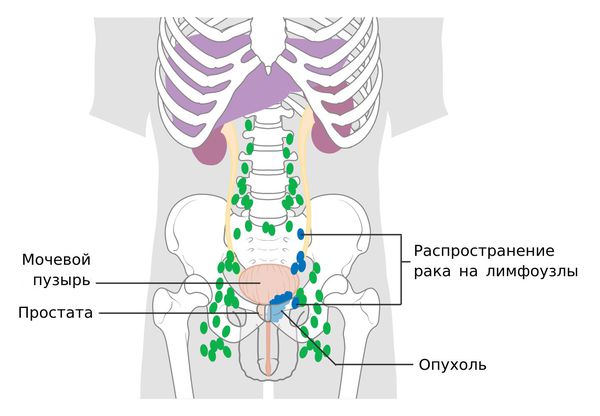
Рис. 3. Пути распространения рака предстательной железы в лимфоузлы таза.
В случае необходимости дополнительно проводится КТ органов груди или брюшной полости.
Цель проведения остеосцинтиграфии – выявление возможного поражения опухолью костей скелета.
Могут назначиться дополнительные исследования – рентгенография (прицельная), УЗИ, урофлоуметрия.
Группа риска определяется, исходя из уровня ПСА на момент до начала терапии, суммы Глисона, согласно данным биопсии, и клинической стадии болезни. Группа риска может быть низкой, промежуточной и высокой. Ее определение крайне важно, чтобы выбрать оптимальный метод лечения.
ПСА от 10 до 20 нг/мл
Методики лечения
В соответствии с результатами многоцентрового проспективного рандомизированного исследования ProtecT (2016) лучевая терапия и хирургическое лечения демонстрируют раную противоопухолевую эффективность и обеспечивают надежный контроль над заболеванием у большинства (более 90%) больных раком предстательной железы с низким и промежуточным риском рецидива заболевания. В настоящее время решающим фактором при выборе противоопухолевого лечения у этой категории больных является безопасность терапии и снижение риска осложнений.
Рассмотрим основные виды терапии: хирургическое лечение, брахитерапия, стереотаксическое облучение, сочетанная лучевая терапия.
Хирургическое вмешательство
РПЭ, или радикальная простатэктомия, представляет собой хирургическое вмешательство по удалению предстательной железы, а также окружающей клетчатки и лимфоузлов. При такой операции с железой единым блоком удаляют семенные пузырьки и участок канала уретры.
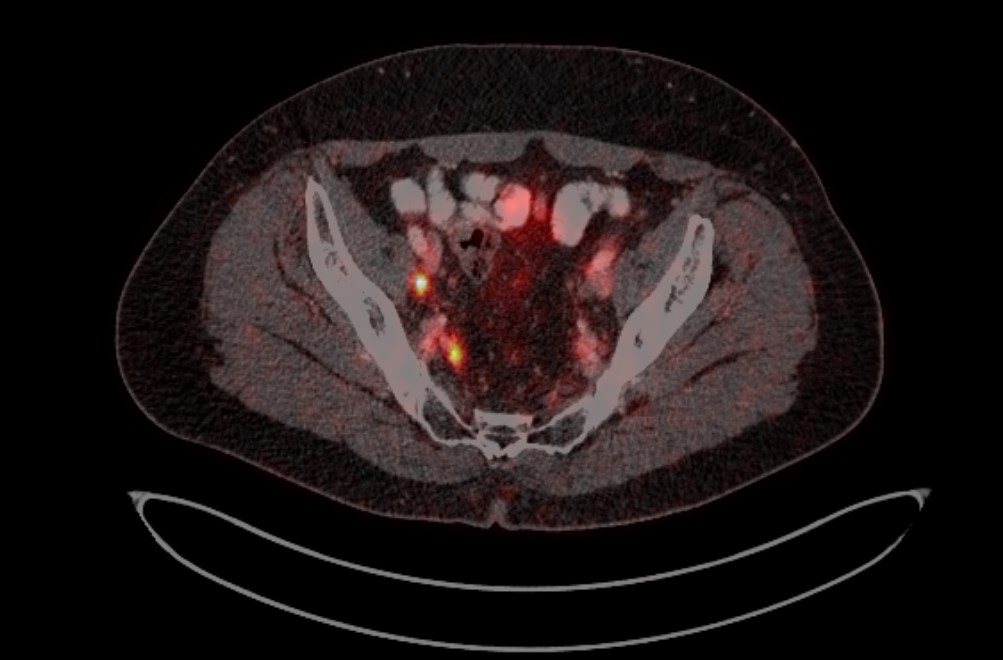
Рис. 4. ПЭТ-КТ изображения больного М. с поражением тазовых лимфоузлов
РПЭ различается по виду доступа и степени инвазивности:
Позадилонный доступ предполагает разрез в нижней части живота, через который удаляется простата и местные ткани.
Промежностная методика – это открытый способ, при котором небольшой надрез делается в зоне между анусом и кожно-мышечным мешком, то есть мошонкой. Методика позволяет удалить простату, но при ее применении нельзя также удалить неблагоприятные ткани и узлы, расположенные около железы. Если после проведения промежностной операции в органах малого таза обнаружатся раковые клетки, нужно будет дополнительно делать лимфаденэктомию. Сейчас промежностная методика применяется крайне редко.
Лапароскопическая методика – наиболее щадящая. Врач имеет доступ к пораженному органу через маленький разрез внизу живота. В него вводится камера и все нужные хирургу инструменты. Камера подает на экран изображение органов малого таза, благодаря чему врач полностью контролирует процесс, а пациент получает минимум вреда. При таком способе минимизированы кровопотери, посторонние органы почти не травмируются, эректильная функция сохраняется частично или полностью и т. д.
Рассмотрим также наиболее распространенные осложнения, которые могут возникнуть после операции на простате:
Брахитерапия
Брахитерапия представляет собой введение в ткани источников излучения. Эта методика – самая «молодая» среди способов лечения РПЖ. Сегодня это один из наиболее востребованных методов облучения простаты, обеспечивающий очень высокую избирательность подведения дозы. Основная особенность брахитерапии заключается в том, что простата облучается изнутри – источник облучения вводится непосредственно в нее. Такой метод дает возможность применять высокие дозы (100-140 Гр и более), при этом избегая высокого риска лучевого поражения не подверженных раку тканей.
Стремительный рост клинического применении брахитерапии, по сравнению с хирургическими вмешательствами, обуславливается высокой эффективностью, которая сопоставима с простатэктомией, при гораздо более низкой частоте возникновения осложнений.
Различают 2 вида брахитерапии, в зависимости от способа введения источника излучения в железу и его мощности:
При проведении низкомощностной брахитерапии в ткани простаты вживляется источник излучения и остается в них до полного распада. Долгое время при РПЖ именно этот вид брахитерапии применялся чаще всего. Наиболее часто для выполнения терапии используется изотоп радиоактивного йода, то есть I125.
Согласно многочисленным исследованиям, брахитерапия низкой мощности обеспечивает не очень высокую точность облучения. Это объясняется смещением источника излучения, изменением формы и размеров простаты, затрагиванием прилежащих здоровых органов. Ввиду этого низкомощностная методика показана в основном пациентам с самыми начальными стадиями, когда опухоль небольшая и не выходит за пределы железы. Такая брахитерапия имеет и другие существенные недостатки. Первый – это высокая частота осложнений, возникающих со стороны мочевыводящих путей, может даже возникнуть острая задержка мочи и необходимость эпицистостомы, то есть формирования надлобкового мочепузырного свища, на долгий срок. В основе осложнений – отек предстательной железы из-за того, что в ней остается несколько сотен зерен (инородных тел). Кроме того, радиоактивные зерна, если они долго находятся в организме, представляют собой источники излучения, представляющие определенную опасность для других людей. Из-за этого контакт пациента с родными ограничен (нельзя близко общаться с маленькими детьми).
Рис. 5. Высокомощностная (высокодозная) брахитерапия
Самая современная методика внутритканевой терапии – высокомощностная брахитерапия. Источники излучения автоматически загружаются и извлекаются. Эта лучевая терапия обладает принципиальным плюсов – высокой точностью облучения, достигаемой путем введения игл под контролем специального УЗ-аппарата. Одновременно в автоматическом режиме рассчитываются дозы и возможность быстрой корректировки плана лучевого лечения. Источник излучения находится в организме пациента временно, поэтому уровень осложнений – самый низкий, по сравнению со всеми радикальными методиками терапии РПЖ, включая низкодозную разновидность брахитерапии.
Технологические особенности методики позволяют предлагать ее большинству больных, вне зависимости от размеров злокачественного новообразования и его распространенности за пределы простаты. Кроме того, высокомощностная брахитерапия – это «золотой стандарт» при комбинированном лечении, то есть одновременном использовании с дистанционным облучением у больных с неблагоприятными характеристиками новообразования.
Самый большой недостаток высокомощностной методики – высокие требования, касающиеся квалификации медицинского персонала, а также необходимость использования высокотехнологичного оборудования. Этим объясняется малая распространенность метода в России.
Противопоказания к брахитерапии подразделяются на общие и урологические. Самые частые урологические противопоказания – это серьезные нарушения процесса мочеиспускания:
Нужно отметить, что большой объем простаты, который имеет значение для низкодозной брахитерапии (50-60 см 3 ), почти не ограничивает возможности лечения в режиме высокомощностной методики.
Данные противопоказания относятся не только к брахитерапии, но и к другим методикам лучевой терапии РПЖ.
Стереотаксическое облучение
СТЛТ (стереотаксическая лучевая терапия) – высокоточная методика лечения очага РПЖ высокими дозами ионизирующего излучения.
Рис. 6. Стереотаксический лучевой ускоритель
Сегодня СТЛТ при раке простаты реализуется несколькими основными методами, каждый из которых обладает своими особенностями, плюсами и минусами:
Сравнительная характеристика техник СТЛТ простаты
Что такое рак предстательной железы? Причины возникновения, диагностику и методы лечения разберем в статье доктора Скатова Бориса Васильевича, уролога со стажем в 27 лет.
Определение болезни. Причины заболевания
Рак предстательной железы (РПЖ) — это злокачественное новообразование, развивающееся из патологических клеток предстательной железы. Рак предстательной железы является самым распространённым новообразованием у мужчин старше 50 лет и характеризуется значительной летальностью (свыше 16% в отдельных случаях), занимая второе место в структуре смертности после рака лёгких. [1]
Предстательная железа — особый орган мочеполовой системы мужчин, расположенный в промежутке между прямой кишкой, лобковой костью и мочевым пузырём, охватывает значительный участок мочеиспускательного канала. Простата вырабатывает гормоны и сок простаты, являющийся средой для жизни сперматозоидов, при попадании их в матку участвует в регуляции мочеиспускания.
Наиболее высокий процент заболевания РПЖ наблюдается в США, Канаде, а также в некоторых европейских странах — там болезнь занимает первое место среди всех онкологических заболеваний. Согласно данным Национального института рака (National Cancer Institute, США), с 1986 по 1992 год процент заболеваемости раком простаты среди белокожего населения вырос на 108% и на 102% — для афроамериканцев. [2]
Уровень заболеваемости РПЖ на территории России также неумолимо увеличивается. В 2006 году впервые было выявлено 18 092 случая рака предстательной железы, а стандартизованный показатель равнялся 21,4 на 100 тысяч населения. Прирост заболеваемости с 1996 по 2006 год составил 94,84% при учёте среднего темпа прироста за 2006 год — 6,9%.
Прирост летальности от рака простаты за последние 20 лет составил 58,76%. Такой прирост равнозначен распространению самой настоящей эпидемии. Так, в США в 2016 году было заявлено 272843 (а в 2009 году — 207789) первичных выявлений рака предстательной железы, приведших к 29225 летальным случаям в 2009 году. По данным европейских урологов, в 2017 году заболеваемость в Европе составила 219 случаев на 1000 мужчин. В России, согласно эпидемиологическим данным Чиссова В.И., в 2012 году впервые выявлено 24911 случаев рака предстательной железы. [3]
Следует понимать, что интенсивный прирост заболеваемости раком предстательной железы связан, в частности, с широким внедрением в клиническую практику новейших диагностических методов обследования пациентов среднего и пожилого возраста. Огромное значение имеет определение ПСА в качестве скрининга мужчин старше 50 лет, основанный на выявлении простатического специфического антигена в крови и моче мужчин. Например, в 60-х и 70-х годах прошлого века, при отсутствии данной методики, рак предстательной железы выявляли только на поздних стадиях уже в крайне запущенном состоянии. [4]
Частота распространения онкологии этой локализации неодинакова в разных регионах, а также среди лиц разных профессий и представителей определённых национальностей. Чаще всего рак предстательной железы выявляется у североамериканцев и европейцев, реже всего у азиатов. [5]
Причины заболевания раком предстательной железы:
Симптомы рака предстательной железы
Как распознать первые симптомы рака простаты
Следует знать, что рак предстательной железы на ранних стадиях протекает совершенно бессимптомно.
По мере распространения опухоли и появления метастазов начинают проявляться определённые клинические симптомы:
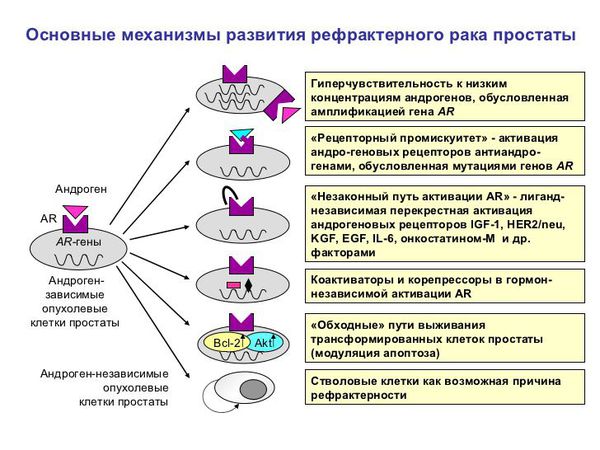
Патогенез рака предстательной железы
Причины, по которым возникает рак простаты, разнообразны и до конца не установлены. Выделяют следующие механизмы молекулярного возникновения РПЖ:
Классификация и стадии развития рака предстательной железы
Классификация рака предстательной железы по системе TNM
Классификацию стадий развития рака разработал французский хирург Пьер Денуа в 1952 году. В дальнейшем она была многократно переработана. В 2002 году было принято решение о прекращении внесения изменений до возникновения радикальных перемен в диагностике и лечении злокачественных опухолей. Идею новой знаковой классификации по системе TNM поддержали национальные комитеты TNM различных стран, данная система получила признание во всём мире. Классификация 2002 года помогает интерпретации полученных результатов, оптимизирует алгоритмы лечения. Система TNM в последней редакции повсеместно используется в установлении диагноза и определении стадии рака предстательной железы.
Т — опухоль первичная:
— ТX — недостаточно сведений для интерпретации первичной опухоли;
— Т0 — первичная опухоль не выявляется;
— Т1 — клинических проявлений опухоли нет, она не проявляется при пальпации, её не удаётся визуализировать специальными методами:
— Т2 — опухоль, ограниченная предстательной железой или распространённая в капсуле:
— Т3 — опухоль распространяется за пределы капсулы предстательной железы:
— Т4 — несмещаемая опухоль или опухоль, которая распространяется на соседние ткани и органы, но не на семенные пузырьки: шейку мочевого пузыря, наружный сфинктер, прямую кишку, мышцу, поднимающую задний проход, и/или тазовую стенку.
N — регионарные лимфоузлы
Регионарные лимфоузлы предстательной железы — это узлы малого таза, находящиеся ниже бифуркации общих подвздошных артерий. Категория N не зависит от стороны локализации регионарных метастазов.
— NX — недостаточно данных для оценки регионарных лимфоузлов;
— N0 — отсутствие метастаз в регионарных лимфоузлах;
— N1 — метастазы в регионарных лимфоузлах присутствуют.
M — отдалённые метастазы:
— МX — определение наличия отдалённых метастазов невозможно;
— М0 — признаки отдалённых метастазов отсутствуют;
— М1 — присутствие отдалённых метастазов:
Классификация рака простаты по шкале Глисона (Gleason score)
Шкала Глисона позволяет определить степень злокачественности опухоли, выявленной при биопсии предстательной железы. Об уровне опасности опухоли свидетельствуют набранные баллы по данной шкале: чем бал больше, тем опаснее опухоль. В основе оценки опухоли лежит сравнение раковых клеток, полученных при биопсии простаты, с нормальными клетками. Так, отсутствие отличия раковых клеток от обычных позволяет оценить опухоль в 1 балл по шкале Глисона. При радикальном отличии клеток опухоли ставится максимальная оценка в 5 баллов.
Степень злокачественной опухоли определяется по сумме Глисона, то есть путём суммирования баллов данной шкалы (от 1 до 5) по двум самым обширным и злокачественным новообразованиям, которые обнаружили в тканях предстательной железы.
Оценка злокачественных опухолей по сумме Глисона:
Классификация рака простаты по системе Джюит-Уайтмор
По системе Джюит-Уайтмора классификация рака предстательной железы делится на стадии: А, В, С и D. Стадии А и В — излечимы, стадии С и D также вылечиваются, но прогноз их излечения менее благоприятный.
Стадия А. Она является самой ранней стадией. Симптомы не проявляются, хотя раковые клетки уже локализуются в простате:
Стадия В. Опухоль не выходит за пределы простаты. Определяется при пальпировании, и/или фиксируется повышенный уровень ПСА:
Стадия С. Опухоль выходит за пределы капсулы простаты и распространяется на соседние ткани и органы, включая семенные пузырьки:
Стадия D. Опухоль распространяет метастазы в регионарные лимфатические узлы или в отдалённые органы и ткани (лёгкие, печень, кости, желудок и т. д.):
Осложнения рака предстательной железы
Метастазы при раке простаты
Раковые клетки продвигаются через соединительную ткань и в результате проникают внутрь кровеносной или лимфатической системы. Затем они переносятся с кровью или лимфой, пока не закрепятся на новом месте, — так образуются метастазы.
Наиболее часто метастазы рака простаты поражают кости. При этом возникает боль в поражённой костной ткани, иногда в отдалённых участках. Если сдавливается нерв, боль может отдавать в другие участки, особенно такое характерно для рук и ног. При поражении метастазами позвоночника часто сдавливается спинной мозг и возникают переломы. Сдавливание нервных стволов может приводить к различным неврологическим симптомам: боли, парестезии (ощущению покалывания, жжения, «ползания мурашек»), гиперестезии (повышенной чувствительности) и т. д.
Помимо костей, метастазы рака простаты часто развиваются в лимфоузлах. Выделяют поражение ближайших лимфатических узлов и отдалённых. Если опухоль распадается и продукты её распада разносятся по организму, метастазы могут появиться в любом лимфатическом узле. Увеличенные лимфоузлы сдавливают органы, что приводит к нарушению их работы и характерным проявлениям. Симптомы зависят от того, где именно локализовались очаги опухоли.
Диагностика рака предстательной железы
Пальцевое исследование предстательной железы через прямую кишку (задний проход) долгое время являлось основным и чуть ли не единственным методом диагностики рака простаты. Метод не потерял своего значения и на сегодняшний день. Специфической характеристикой РПЖ при ректальном исследовании является плотность узлов в одной или двух долях предстательной железы, доходящая до так называемой «каменистости». Однако низкий процент выявления первичного рака простаты (меньше 6% по последним данным), при развитии более информативных методов, постепенно сводит диагностическую ценность метода к минимуму. Кроме того, пальцевое исследование приводит к ложному повышению уровня простатического специфического антигена в результате вынужденной стимуляции предстательной железы. [11] [12]
Простатический специфический антиген (ПСА) является онкомаркером рака предстательной железы и обладает высокой чувствительностью и хорошей специфичностью в отношении данного процесса. ПСА — это белок гликопротеин, который может вырабатываться только эпителием простаты. При раке он старается блокировать развитие клеток эндотелия простаты.
В норме содержание ПСА в крови равно 4,0 нг/мл. Значения 4,0-10,0 нг/мл являются промежуточными (так называемая «серая зона»), а более 10,0 нг/мл — диагностически значимые. ПСА является калликреиноподобной сериновой протеазой, секретируемой клетками эпителия предстательной железы. Этот маркер считается не опухолеспецифическим, а органоспецифическим, в связи с этим сывороточный уровень ПСА может увеличиваться не только при раке простате, но и при доброкачественной гиперплазии предстательной железы, хроническом простатите, а также при любой стимуляции предстательной железы. [13]
Простатический специфический антиген 3 (ПСА 3) (PCA 3 (Prostate Cancer Gen 3) важен при решении вопроса о повторной биопсии после отрицательного результата первоначально проведённого исследования. PCA — наиболее значимый новый биомаркер. Антиген определяется в моче после 3-кратного массажа предстательной железы во время ректального исследования. Показатель РСА 3 превосходит чувствительность общего ПСА и свободного ПСА. Показатель РСА 3 стоит применять вместе с ПСА и иными клиническими факторами риска в номограммах или других системах стратификации риска для того, чтобы принять решение о проведении первичной или повторной биопсии. Считается, что уровень РСА 3 повышается с увеличением объёма РПЖ. [14]
Индекс здоровья простаты (показатель PHI — Prostate healthindex). Его определение основано на определении фракции свободного ПСА (-2проПСА). [15]
Инструментальная диагностика
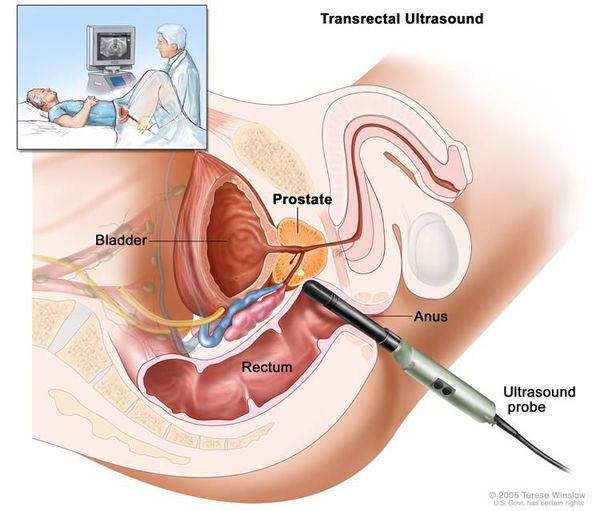
Ультразвуковое исследование рака предстательной железы (трансректальное УЗИ предстательной железы, ТРУЗИ). Эхографическая диагностика рака предстательной железы неоднозначна. Классическая ультразвуковая картина представлена гипоэхогенными очаговыми зонами в периферических отделах предстательной железы. С увеличением площади опухолевых очагов эти зоны содержат как гипо-, так и гиперэхогенные участки. 40 % опухолей предстательной железы, которые диагностированы при биопсии, представлены изоэхогенными участками. [16]
ТРУЗИ проводится для решения двух первоочерёдных задач:
Биопсия простаты — самый точный метод диагностики рака предстательной железы. Стандартная методика выполнения биопсии предстательной железы — трансректальная биопсия под контролем трансректального УЗИ, которая обязательно выполняется, как минимум, из 12 точек. Проводится по результатам одного из трёх методов диагностики: пальцевого ректального исследования, определения концентрации ПСА в сыворотке крови и ТРУЗИ. [17]
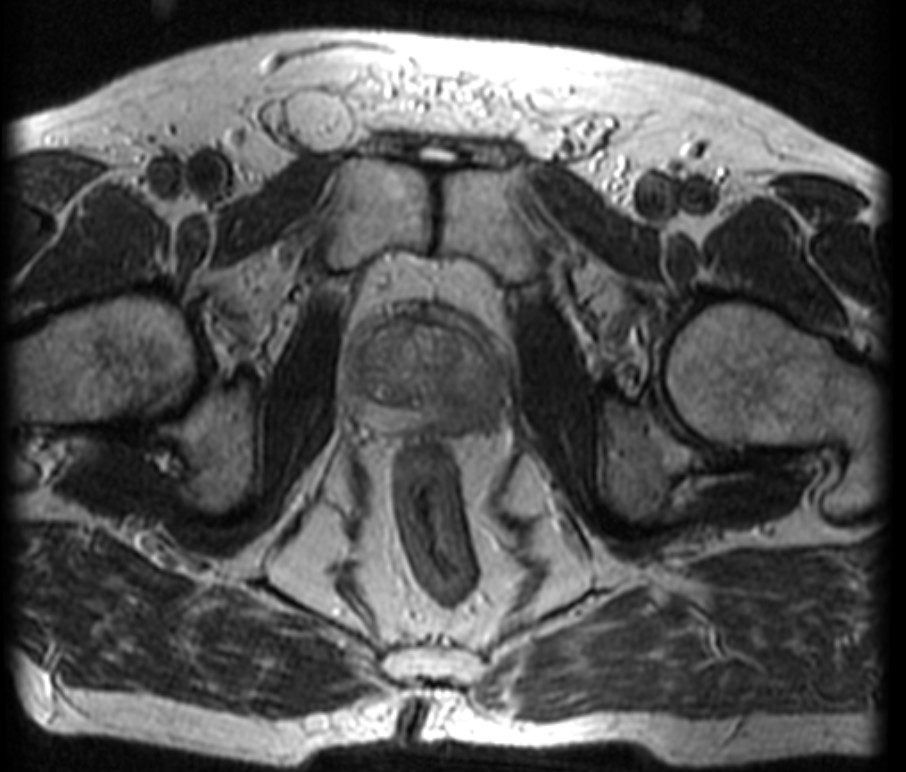
Магнитно-резонансная томографии (МРТ) предстательной железы является наиболее чувствительным методом диагностики экстрапростатической инвазии опухоли, а применение динамической магнитно-резонансной простатовезикулографии с помощью контрастного усиления и эндоректальной магнитной катушки повышает точность диагностики ещё на 18%. [18]
Компьютерная томография (КТ). Выполнение КТ предстательной железы для определения стадии процесса не рекомендуется, так как КТ предстательной железы менее информативна, чем МРТ, для дифференциальной диагностики локализованного и экстрапростатического процесса. КТ чаще назначают для планирования дистанционной лучевой терапии (ДЛТ) (ссылка). [19]
Методы диагностики отдалённых метастазов. Для диагностики отдалённых метастазов рекомендуются следующие методы:
Радиоизотопное исследование (сканирование) скелета применяется при первичном обследовании пациентов с высоким баллом злокачественного роста по шкале Gleason, высоким уровнем ПСА (> 10 нг/мл) и щелочной фосфатазы или при выраженном болевом синдроме (в таком случае риск костных метастазов достаточно высок).
Для радиоизотопного исследования внутривенно вводят аналог пирофосфата, объединённый с радиоактивным изотопом технеция-99.
Через три часа после введения препарата (пирофосфат + технеций-99), когда изотоп накопился в костной ткани, пациента укладывают на диагностический стол и с помощью гамма-камеры исследуют расположение радиоактивной метки в костной ткани. Обработка информации происходит с помощью компьютерной программы. Доза радиации, получаемая пациентом при обследовании, очень мала и безопасна.
Лечение рака предстательной железы
Радикальная простатэктомия (РПЭ) — полное удаление простаты
Хирургическое вмешательство в объёме полной простатэктомии является наиболее радикальным методом лечения. Большинство урологов рекомендуют радикальную простатэктомию как метод выбора при лечении локализованного рака предстательной железы. Под таким оперативным лечением подразумевается удаление предстательной железы с семенными пузырьками и участком мочеиспускательного канала. Целью операции при локализованном и некоторых вариантах местно распространённого РПЖ является полное излечение пациента. В редких случаях полное удаление простаты нацелено на паллиативную помощь при лечении местно распространённого процесса, т. е. для улучшения состояния больного. В этих случаях задача операции состоит в удалении основной массы опухоли для повышения эффективности консервативного лечения.
Радикальное хирургическое лечение обычно проводится у пациентов с РПЖ локализованной формы с ожидаемой продолжительностью жизни более 10 лет.
Варианты операционного доступа при выполнении радикальной простатэктомии:
Показания к радикальной простатэктомии:
Преимущества радикальной простатэктомии перед консервативными методами лечения:
В последние несколько лет стала широко применяться лапароскопическая радикальная простатэктомия, которую можно выполнить чрезбрюшинным или внебрюшинным доступами. Применение данной техники позволяет снизить число осложнений и ускорить процесс реабилитации больных.
Один из вариантов лапароскопической операции — робот-ассистированная радикальная простатэктомия (согласно материалам Guidelines EAU 2015 года — клинического руководства Европейской ассоциации урологов). Робот-ассистированная радикальная простатэктомия (РАРП) активно «вытесняет» РПЭ в качестве «золотого стандарта» оперативного лечения локализованного рака простаты во всём мире. [22] При РАРП, по сравнению с РПЭ, достоверно уменьшается объём кровопотери, имеются преимущества при оценке восстановления удержания мочи и эректильной функции. [14]
Лучевая терапия (ЛТ)
Как и простатэктомия, лучевую терапию относят к радикальным методам лечения локализованного рака простаты. При местно распространённом РПЖ, ЛТ проводят для того, чтобы улучшить выживаемость больных, и чаще в сочетании с гормонотерапией. Цель лучевой терапии — максимально точное достижение терапевтической дозы ионизирующего излучения в ткани предстательной железы при условии минимального лучевого воздействия на окружающие органы и ткани. [23]
Брахитерапия (внутритканевая ЛТ) — имплантация радиоактивных источников в ткань предстательной железы. Для терапии РПЖ применяется постоянная (низкодозная) и временная (высокодозная) брахитерапия. Для временной брахитерапии применяют изотоп 192 Ir. Удаление радиоактивных игл осуществляется после подведения необходимой дозы к предстательной железе. Высокодозную брахитерапию применяют при местно распространённом РПЖ (T3 N0 M0), комбинируя с дистанционным облучением. При локализованном РПЖ чаще применяют постоянную брахитерапию: в предстательную железу вводятся радиоактивные гранулы 125I (период полураспада — 60 дней) или 103Pd (период полураспада — 17 дней). Более локализованное распределение ионизирующего излучения при брахитерапии позволяет подвести более высокую дозу облучения к предстательной железе с меньшим лучевым воздействием на окружающие ткани, чем при проведении дистанционной ЛТ. Внедрение радиоактивных источников производится через промежность под контролем трансректального УЗИ. Доза облучения при имплантации 125I составляет 140-160 гр, при имплантации 103Pd — 115-120 гр. [24]
Минимально инвазивные методы лечения РПЖ
К минимально инвазивным методам лечения РПЖ относятся криоабляция простаты и абляция предстательной железы с помощью высокоинтенсивного сфокусированного ультразвука — HIFU (англ. High Intensity Focused Ultrasound). Криоабляция простаты — хорошо изученный альтернативный метод терапии РПЖ, в то время как метод HIFU до конца не изучен. Фокальная терапия РПЖ с помощью различных методик, таких как криоабляция, ультразвуковая или лазерная абляция и пр.) активно изучается во многих клиниках. [14]
Гормональная терапия
Гормонотерапия, в качестве самостоятельного способа лечения РПЖ, рекомендуется с паллиативной целью. В то же время назначение гормональных препаратов может быть показано в сочетании с радикальным оперативным или лучевым лечением в качестве комбинированной противоопухолевой терапии. Основой механизма действия эндокринного лечения является снижение концентрации тестостерона в клетках предстательной железы, реализованное одним из следующих способов:
К методам гормонотерапии относят:
Гормональные препараты других классов
Рекомендуется принимать кетоконазол — противогрибковый препарат, угнетающий синтез андрогенов надпочечников. Применяют в качестве второй линии гормональной терапии метастатического РПЖ на фоне прогрессирования процесса после проведения максимальной андрогенной блокады. Кетоконазол назначают внутрь в дозе 400 мг 3 раза в сутки.
Иммунотерапия рака простаты
Иммунная терапия рака предстательной железы активирует лимфоциты, способные уничтожить раковые клетки. Мишень — антигены, характерные для рака простаты. Это, прежде всего, PSA, а также простатическая фосфатаза и простатспецифический мембранный антиген (PSMA). При иммунологическом лечении злокачественных опухолей простаты применяются дендритно-клеточные вакцины, вакцины клеток всей опухоли, векторсвязанные вакцины и моноклональные антитела.
На сегодняшний день появились новые лекарственные средства, которые могут стать препаратами первой линии лечения данного заболевания. Абиратерон (Zytiga) — препарат, утверждённый в Израиле и предназначенный для лечения кастрат-резистентного рака предстательной железы. Проствак, как вакцина, стимулирует иммунитет для мобилизации организма на борьбу с раковыми клетками. Выживаемость пациентов с тяжёлыми формами рака простаты, принимающих проствак, повышается с 16-ти месяцев до 24-х. Алфарадин — радиофармпрепарат, выделяющий радиоактивные альфа-частицы, они локально воздействуют на метастазы. Деносумаб защищает кости при возникновении метастаз, препятствуя выводу кальция из костей, притормаживая развитие метастатического процесса в 5 раз эффективнее других препаратов. [14]
Химиотерапия рака простаты
На начальных этапах рака простаты химиотерапия малоэффективна. Это связано с тем, что злокачественные опухолевые клетки предстательной железы растут так же, как и здоровые. Цитостатики же действуют исключительно на быстрорастущие клеточные структуры. Чаще всего противоопухолевые препараты назначаются на III–IV стадии болезни — при больших размерах первичной опухоли, сильной боли, метастазах и наличии нескольких очагов в костной ткани.
Преимущество противоопухолевых химиопрепаратов — это возможность использовать их при агрессивных опухолях предстательной железы, которые уже дали метастазы и не могут быть удалены хирургически. В сочетании с операцией и гормональными препаратами химиотерапия позволяет стабилизировать или улучшить состояние пациента.
Химиотерапия заключается во внутривенном введении специальных химиотерапевтических средств. В среднем один цикл химиотерапии при раке простаты длится 1–4 недели. При раке предстательной железы применяется Доцетаксел с Гозерелином, Бусерелином и Трипторелином.
При неэффективности Доцетаксела или устойчивости к нему применяется Кабазитаксел (Джевтана). Результаты исследований показали, что этот химиопрепарат гораздо эффективнее Митоксантрона, который ранее выбирался для замены Доцетаксела.
Химиотерапевтические препараты останавливают деление злокачественных клеток, замедляя или полностью останавливая рост опухоли. В то же время эти препараты вызывают тяжёлые побочные эффекты, такие как:
Виротерапия
Спасительная терапия
У всех пациентов с метастатическим процессом в костях, получающих терапию на основе доцетаксела, наблюдалось прогрессирование. В связи с этим были проведены многочисленные исследования, связанные с изучением роли спасительной терапии. Результаты этих исследований показали, что терапия кабазитакселом, интермиттирующая химиотерапия доцетакселом и молекулярно-направленная терапия — наиболее приемлемые режимы лечения. В настоящее время эти методики не рекомендуются в связи с малым количеством рандомизированных исследований.
Методы паллиативной терапии
У большинства пациентов с костно-распространённым раком предстательной железы с (КР РПЖ), костные метастазы сопровождаются выраженным болевым синдромом. Два радиоизотопа, Sr-89 и Sа-153, способны уменьшить или купировать боль в костях у 72 % пациентов. У больных с костными метастазами, которые сопровождаются болевым синдромом, применение Rа-233 оказалось весьма эффективным.
Осложнения, вызванные костными метастазами, выражаются в болевых ощущениях в костях, разрушении позвонков, деформирующих патологических переломах и компрессии спинного мозга. Ещё одна причина патологических переломов — остеопороз, поэтому необходимо проведение его профилактики.
Применение костного цемента — продуктивный метод лечения патологических переломов, который позволяет значительно уменьшить болевые ощущения и повысить качество жизни. При возникновении подозрения на существование компрессии спинного мозга необходимо как можно скорее назначить высокие дозы кортикостероидов и выполнить МРТ.
Бифосфонаты используются для торможения резорбции костной ткани. При применении золедроновой кислоты было отмечено увеличение времени до появления первого скелетного осложнения, что улучшало качество жизни пациентов. В настоящее время бифосфонаты показаны пациентам с КР РПЖ с костными метастазами для профилактики скелетных осложнений, хотя однозначного оптимального интервала между приёмами не существует (на данный момент он составляет 3 недели или менее).
Всегда стоит помнить о том, что у этих препаратов существуют побочные эффекты, в особенности у амино-бисфосфонатов (например, некроз верхней челюсти). Бисфосфонаты назначают на раннем этапе лечения КР РПЖ с клиническими проявлениями. При дополнительной системной терапии обнаруживают методы устранения возможных побочных эффектов — болевого синдрома, запора, отсутствия аппетита, тошноты, усталости, депрессии, которые развиваются при проведении паллиативного лечения. Терапия включает в себя паллиативную ДЛТ, кортизон, анальгетики и противорвотные средства.
Деносумаб — моноклональное антитело человека, направленное против рецептора-активатора ядерного фактора В-лиганда, является ключевым медиатором образования остеокластов (больших многоядерных клеток). У пациентов с КР РПЖ стадии М0 деносумаб привёл к увеличению показателя выживаемости без костного метастазирования по сравнению с плацебо. При проведении третьей фазы лечения было отмечено, что эффективность и безопасность деносумаба сопоставима с золедроновой кислотой у пациентов с метастатическим КР РПЖ. Деносумаб разрешён к применению Управлением по контролю качества пищевых продуктов и лекарственных средств США для профилактики скелетных осложнений у пациентов с костными метастазами, обусловленными наличием раковых опухолей.
После терапии доцетакселом, при прогрессии РПЖ рекомендовано применение кабазитаксела.
Рейтинг ведущих онкоцентров России:
Рейтинг ведущих зарубежных клиник, специализирующихся на лечении рака предстательной железы:
Далее рассмотрим осложнения различных методов лечения РПЖ.
Осложнения радикальной простатэктомии:
Нарушение эрекции может развиваться у всех больных после выполнения радикальной простатэктомии, не применяя при этом нервосберегающую технику. Для того, чтобы сохранить эректильную функцию, разработана техника операции, позволяющая сохранить кавернозные нервно-сосудистые пучки.
Осложнения дистанционной лучевой терапии:
Осложнения эстрогенотерапии:
Прогноз. Профилактика
Классификация прогностических факторов риска по DAmico
По этой классификации учитывается вероятность прогрессирования рака на начальных стадиях до проявления клинических симптомов и летального исхода, а также риск возникновения рецидивов после локализованного лечения рака.
По классификации рака предстательной железы DAmico, пациентов относят к одной из трёх групп прогрессирования болезни: низкой, средней или высокой. Для оценки берутся следующие показатели:
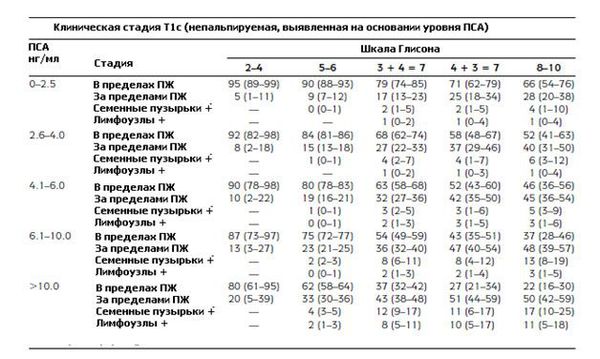
В группу низкого риска относятся пациенты, у которых уровень ПСА ≤ 10 нг/мл, шкала Глисона ≤ 6 баллов, клиническая стадия — T1-2a. К группе среднего риска относят пациентов, у которых уровень ПСА 10-20 нг/мл, шкала Глисона — 7 баллов, клиническая стадия — T2b. К группе высокого риска относят пациентов, у которых уровень ПСА > 20 нг/мл, шкала Глисона ≥ 8 баллов, клиническая стадия — T2c-3a.
Прогнозирование по таблицам Алана Партина (номограммам)
Таблицы Партина представляют собой шкалы, в которых учитываются математические модели, высчитанные на основании значения уровня ПСА, баллов по шкале Глисона и клинической стадии рака простаты по классификации по системе ТNM. График Партина позволяет сделать прогноз дальнейшей прогрессии заболевания. Номограммы составлялись на основании исследования данных о мужчинах, которые проходили лечение рака предстательной железы. Таким образом, базируясь на этих данных, были составлены таблицы, которые делятся следующим образом:
Вот так выглядят модифицированные номограммы Партина, по которым можно определить вероятность дальнейшего прогрессирования рака простаты:
Прогноз выживаемости при раке простаты
Профилактика
— Ежегодное урологическое обследование после 50 лет, а мужчин с генетической предрасположенностью — после 40 лет по стандартной программе обследования, включающее:
— Правильное сбалансированное питание:
— Отказ от вредных привычек: курения, алкоголя, наркотиков.
— Физическая активность.
Одним из основных факторов, способствующих развитию болезни, является образ жизни. Умеренные физические нагрузки на свежем воздухе — бег трусцой, ходьба, плавание, езда на велосипеде — улучшают иммунитет, устраняют гиподинамию как фактор развития рака простаты, усиливают кровообращение малого таза мужчины.