трг тест что такое
Что такое ТРГ (Телерентгенограмма)
Содержание
Телерентгенограмма или ТРГ это разновидность рентгена лицевой части головы. Изображение снимается на удалении 1,5 — 2 метра, что позволяет получить картинку в естественной пропорции 1:1 с минимальным искажением. Процедура может выполняться детям после 6 лет.
Описание / что показывает ТРГ
На телеснимке изображается человеческий череп в рентгеновских лучах. Видны твёрдые и мягкие ткани, их соотношение и положение. ТРГ в стоматологии считается важным этапом подготовки к ортодонтическому лечению, вмешательствам в челюстно-лицевой хирургии и травматологии.
Что показывает ТРГ-снимок:
Изображение, получаемое в ходе телерентгенографии, даёт стоматологу информацию об особенностях строения лицевой и мозговой части черепа, состоянии костей, возможность строить план и прогнозы лечения. В процессе коррекции прикуса ортодонтическими конструкциями процедуру повторяют. Так появляется возможность отследить ход изменений, проверить правильность продвижения зубов.
Отвечая на вопрос о том, что такое снимок ТРГ, можно сказать, что это второй по популярности метод стоматологической диагностики после ортопантомограммы.
Как часто можно делать
В ходе проведения телерентгенографического обследования пациент получает минимальную дозу облучения, равную 20 мкЗв. Она меньше цифры, допустимой СанПиНом России в течение 1 года, в 50 раз.
Для справки, во время флюорографии органов грудной клетки излучение составляет Несмотря на почти безвредность, данный вид исследования не стоит проводить беременным и кормящим женщинам.
Кратность проведения, как и других типов инструментальной диагностики, определяет лечащий врач. Телеснимок назначают на этапе подготовки к постановке ортодонтических устройств, в процессе лечения и после его завершения для контроля результата.
Обратите внимание, что при подсчёте лучевой нагрузки суммируются все полученные за год процедуры по любому поводу (не только стоматологические). Информация о количестве и дозах облучения должна быть занесена в личную карту.
Точки ТРГ



Как проводится
В современных клиниках используют цифровые аппараты, позволяющие снизить дозу облучения и получить результат в течение Расшифровка ТРГ в ортодонтии требует от диагностов исключительной квалификации и проводится самыми опытными сотрудниками.
Телерентгенограмма — безопасный способ получить данные о строении черепа, который используется в подготовке к вмешательствам в имеющуюся структуру челюстей.
Оценка функции щитовидной железы (вен. кровь) в Москве
Комплексное исследование направлено на выявление нарушений функции щитовидной железы (гипер- и гипотиреоза).
Исследование рекомендовано людям, входящим в группы риска по заболеваниям щитовидной железы, в том числе жителям регионов с низким природным содержанием йода в питьевой воде, и пациентам с заболеваниями щитовидной железы в анамнезе.
Что входит в комплекс
Приём и исследование биоматериала
Когда нужно сдавать анализ Оценка функции щитовидной железы?
1. Сниженный или повышенный уровень ТТГ;
4. Клиническая картина гипотиреоза или тиреотоксикоза.
1. Диагностика субклинических стадий первичного гипо- и гипертиреоза. Состояния, связанные с задержкой умственного и полового развития у детей, сердечными аритмиями, миопатией, идиопатической гипотермией, депрессией, алопецией, бесплодием, аменореей, импотенцией и снижением либидо, гиперпролактинемией;
3. Мониторинг заместительной терапии при первичном гипотиреозе;
4. Скрининг беременных в I триместре для выявления скрытого гипотиреоза, потенциально опасного для плода;
5. Контроль состояния при выявленном гипотиреозе (пожизненно 1-2 раза/год);
6. Контроль состояния при выявленном диффузном токсическом зобе (в течение 1,5-2 лет 1-3 раза/месяц).
Дифференциальная диагностика заболеваний щитовидной железы;
2. Контрольное исследование при изолированном Т3-токсикозе.
Подробное описание исследования
ТТГ (тиреотропный гормон) – это гормон, синтезирующийся передней долей гипофиза.
Главной его функцией является регуляция деятельности щитовидной железы: стимулирует синтез Т3 и Т4 клетками щитовидной железы и выделение их в кровь
Уровень ТТГ находится в обратной логарифмической зависимости от концентрации Т4: при возрастании уровня Т4 выработка ТТГ снижается, при снижении уровня Т4 выработка ТТГ компенсаторно возрастает, что способствует поддержанию концентрации тиреоидных гормонов на необходимой высоте.
Повышение уровня ТТГ в крови указывает на недостаточную продукцию гормонов щитовидной железы, т.е. гипотиреоз. При этом важным является тот факт, что данный показатель реагирует на снижение функции железы первым, нередко на субклинических стадиях заболевания, когда уровни Т3 и Т4 в сыворотке крови еще в норме.
Поэтому контроль содержания гормона ТТГ в крови является обязательным для пациентов с любой патологией щитовидной железы, и особенно для получающих лечение по этому поводу.
Трийодтиронин (Т3) – гормон щитовидной железы, биологическая активность которого в 3-5 раз превышает активность тироксина (Т4). Некоторое количество трийодтиронина синтезируется в щитовидной железе, однако в основном он образуется при дейодировании тироксина вне ее. Большая часть циркулирующего в крови трийодтиронина связана с белками плазмы, в частности с тироксинсвязывающим глобулином, тироксин-связывающим преальбумином и альбумином. Оставшаяся доля (менее 1 %) трийодтиронина является биологически активной (свободной) фракцией.
Гормон регулирует теплопродукцию, потребление кислорода всеми тканями организма, кроме тканей головного мозга, ретикуло-эндотелиальной системы и гонад. Также стимулирует рост костей, производство половых гормонов. синтез витамина А в печени и всасывание в кишечнике витамина B12. У детей Т3 регулирует рост и развитие центральной нервной системы. Повышает экскрецию кальция с мочой, активирует обмен костной ткани, снижает концентрацию холестерина и триглицеридов в крови, ускоряет обмен белка. Стимулирует ретикулярную формацию и корковые процессы в центральной нервной системе.
Особые указания: При первичной проверке уровня тиреоидных гормонов следует отменить препараты, влияющие на функцию щитовидной железы за 2-4 недели до исследования (после согласования с лечащим врачом). При контроле лечения-исключить прием препаратов в день исследования и обязательно отметить это в направительном бланке (отметить также информацию о приеме других лекарств-аспирина, транквилизаторов, кортикостероидов, пероральных контрацептивов).
Если щитовидная железа не в состоянии производить необходимое количество тироксина либо вырабатывается недостаточно тиреотропного гормона для ее стимуляции, появляются симптомы гипотиреоза. У больных с пониженным уровнем Т4 увеличивается масса тела, сохнет кожа, повышается утомляемость, они становятся очень чувствительны к холоду, у женщин нарушается менструальный цикл. В случае если уровень свободного Т4 выше нормы, обменные процессы в организме и выработка в клетках энергии усиливаются, что приводит к гипертиреозу, для которого характерны учащенное сердцебиение, беспокойство, потеря веса, нарушение сна, дрожь в руках, сухость и покраснение глаз, отечность лица.
Подготовка к исследованию
Взятие крови предпочтительно проводить утром натощак, после 8-14 часов ночного периода голодания (воду пить можно), допустимо днем через 4 часа после легкого приема пищи.
При контроле динамики показателя рекомендуется сдавать кровь на исследование в одинаковое время суток.
Недавние воздействия на щитовидную железу, включая оперативное вмешательство, радиотерапию, лекарственную терапию (в том числе, прием тиреоидных гормонов, йодсодержащих препаратов), могут повлиять на результат теста.
Исключить физическое и эмоциональное перенапряжение за 24 часа до исследования.
Не курить в течение 3 часов до исследования.
Щитовидная железа (скрининг) (венозная кровь) в Москве
Комплексное исследование, которое позволяет выявить гипо- и гиперфункцию щитовидной железы, диагностировать ее аутоиммунное поражение и определить необходимость дальнейшего обследования. Также применяется в целях контроля эффективности проводимой терапии.
Что входит в комплекс
Приём и исследование биоматериала
Когда нужно сдавать анализ Щитовидная железа (скрининг)?
Подробное описание исследования
Щитовидная железа локализована на передней поверхности шеи, немного выше ключицы. Это одна из эндокринных желез, то есть орган, секретирующий в кровь гормоны.
Клетки щитовидной железы продуцируют 2 главных тиреоидных гормона:
Эти гормоны контролируют множество процессов в организме. Они имеют значительное влияние на обмен веществ, рост и развитие человека. Кроме этого, тиреоидные гормоны регулируют уровень инсулина в крови, могут изменять потребление глюкозы организмом.
Для образования гормонов щитовидной железы необходимо присутствие йода, который человек получает в основном из продуктов питания.
В организме существует система отрицательной обратной связи для контроля уровня тиреоидных гормонов. Она также включает тиреотропный гормон (ТТГ), вырабатываемый гипофизом, и тиреотропин-рилизинг-гормон (ТРГ), выделяемый гипоталамусом.
Когда концентрация тиреотропных гормонов в крови снижается, гипоталамус высвобождает ТРГ, который, в свою очередь, воздействует на гипофиз и стимулирует выделение ТТГ. ТТГ влияет на щитовидную железу, в результате чего образуются тиреоидные гормоны.
По мере увеличения концентрации тиреоидных гормонов в крови, гипоталамус и гипофиз вырабатывают меньше ТРГ и ТТГ. В результате щитовидная железа уменьшает синтез T4 и T3. В нормальных условиях данная система регулирует активность щитовидной железы и поддерживает стабильный уровень ее гормонов.
В крови большая часть T4 и T3 связана с белком, называемым тироксин-связывающим глобулином (TBG). Несвязанные Т3 и Т4, называемые свободный Т3 и Т4, являются активными формами гормонов и могут воздействовать на периферические ткани.
Для диагностики основных заболеваний щитовидной железы (гипо-/гипертиреоз, эутиреоидный зоб, рак щитовидной железы) врачу необходимо провести ряд лабораторных исследований. По их результатам специалист может определить причину патологии и назначить адекватную терапию.
Измерение уровня тиреотропного гормона (ТТГ)
ТТГ стимулирует выработку Т4 и Т3. По уровню ТТГ в сыворотке крови судят о наличии гипертиреоза, когда концентрация ТТГ ниже нормы, и гипотиреоза, когда уровень ТТГ повышен.
Характерные клинические признаки гипотиреоза включают:
Характерные клинические проявления гипертиреоза:
Измерение уровня свободного тироксина (Т4) и трийодтиронина (Т3)
Т3 и Т4, находящиеся в крови, практически полностью связываются с белком. Небольшая часть гормонов остается несвязанной (свободной) и представляет собой биологически активную форму.
При образовании избыточного количества Т4 и Т3 у человека могут наблюдаться симптомы гипертиреоза. Если Т4 и Т3 синтезируются в количестве менее необходимого, это состояние характеризуется наличием симптомов, гипотиреоза.
Определение титра антител (АТ) к белку тиреоглобулину (ТГ)
Тиреоглобулин — предшественник гормонов щитовидной железы. В норме он практически не выделяется в кровоток.
Антитела к этому белку появляются в крови человека при иммуноопосредованной патологии щитовидной железы (диффузный токсический зоб, аутоиммунный тиреодит), а также в результате системных аутоиммунных заболеваний (системная красная волчанка, ревматоидный артрит, сахарный диабет 1 типа).
Определение титра антител (АТ) к тиреопероксидазе (ТПО)
Тиреопероксидаза — фермент, который находится в клетках щитовидной железы и участвует в образовании тиреоидных гормонов.
Антитела к ТПО появляются в крови человека при аутоиммунных заболеваниях щитовидной железы (тиреоидит Хашимото) и нарушают функцию щитовидной железы, в результате чего возникает дефицит тиреоидных гормонов и появляются симптомы гипотиреоза. Тем не менее, количество антител к ТПО напрямую не отражает тяжесть аутоиммунной патологии.
Данное комплексное лабораторное исследование позволяет определить уровень основных тиреоидных гормонов в крови и выявить гипер- или гипофункцию щитовидной железы, а также подтвердить ее иммуноопосредованное поражение. Анализ может быть рекомендован здоровым людям в качестве профилактического обследования, пациентам с ранее выявленным заболеванием щитовидной железы, а также лицам, имеющих близких родственников с указанными патологиями.
Подробное описание исследований, референсные значения представлены на страницах с описаниями отдельных исследований.
Трг тест что такое
You are using an outdated browser. Please upgrade your browser or «>activate Google Chrome Frame to improve your experience.
mun.Chişinău, str. Alba Iulia, 21 карта
(+373) 22 944 944 (+373) 69 944 944
Blvd. Traian 7/1, Chisinau
Гипотиреоз встречается относительно часто, примерно у 2-3% всего населения, и обусловлен уменьшением содержания в крови одного или обоих гормонов щитовидной железы.
Клинически гипотиреоз проявляется следующими симптомами
В подавляющем большинстве случаев (90-95%) гипотиреоз обусловлен патологическим процессом в щитовидной железе. Определение свободного Т4 и ТТГ в сыворотке крови является наилучшей комбинацией тестов для диагностики гипотиреоза. При гипотиреозе базальный уровень ТТГ повышен вследствие первичного поражения щитовидной железы (первичный гипотиреоз) и понижен при первичной недостаточности гипофиза (вторичный гипотиреоз) или гипоталамуса (третичный гипотиреоз).
С помощью ТРГ можно провести дифференциальную диагностику между различными клиническими формами гипотиреоза. При гипотиреозах могут быть 3 варианта ответа на ТРГ-тест (см.ниже):
ТРГ-тест – после внутривенной дачи тироксин-рилизинг-гормона (тиролиберина) у здоровых лиц уровень ТТГ повышается на 300-1000% в течение 20-30 мин. При подозрении на гипертиреоз при нормальной базальной концентрации ТТГ в крови отрицательный ответ на введение ТРГ подтверждает диагноз гипертиреоза, тогда как положительный – исключает.
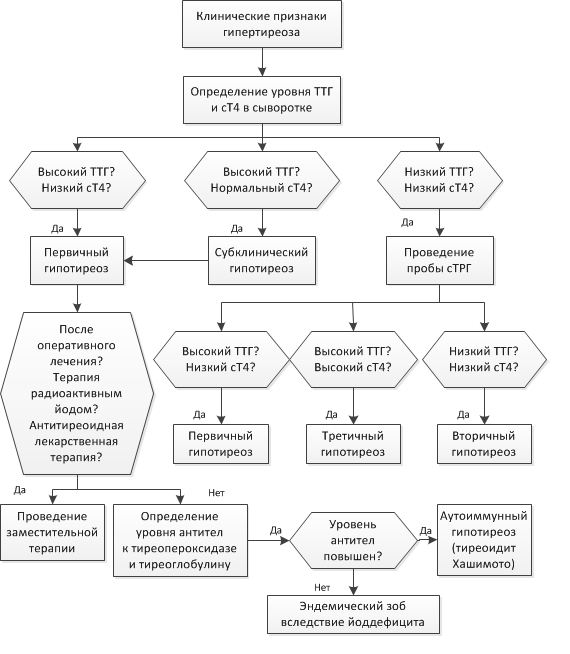
Алгоритм диагностики гипотиреоза и оценка результатов исследований
Повышение уровня ТТГ в крови служит (за редчайшим исключением!) наиболее ранним лабораторным признаком тиреоидной недостаточности. Повышение уровня ТТГ предвещает снижение свободного Т4 по экспоненциальному типу: при снижении свободного Т4 в 2 раза, секреция ТТГ возрастает в 100 раз! В связи с этим повышение ТТГ на фоне нормального содержания свободных Т3 и Т4, называют субклиническим гипотиреозом. Выделяют 3 степени (стадии) развития субклинического гипотиреоза с различными клинико-гормональными проявлениями:
Уровень ТТГ и антител к тиреопероксидазе в сыворотке крови является показателем для оценки прогноза манифестации гипотиреоза. Доказано, что уровень ТТГ в пределах 2-4,2 мМЕ/л в сочетании с субклиническим содержанием антител к тиреопероксидазе в сыворотке крови, являются угрожаемыми параметрами для прогрессирования снижения функции щитовидной железы. Наличие повышения только ТТГ или только антител определяет меньший, но достоверно повышенный риск возникновения патологии (в 5-8 и 25-44 раза соответственно).
Лабораторные критерии оценки эффективности лечения первичного гипотиреоза
Эффективной считается терапия, при которой нормализуются уровни ТТГ и свободного Т4. Динамический контроль за уровнем этих маркеров позволяет подходить к подбору дозы препараты индивидуально. Уровень ТТГ, как правило, нормализуется медленно, особенно при длительно существующем гипотиреозе, поэтому если состояние больного улучшилось и уровень свободного Т4 в пределах нормы, то повышать дозу тиреоидного препарата только для достижения нормально уровня ТТГ, не нужно. После подбора оптимальной дозы препарата необходим ежегодный контроль ТТГ. С возрастом потребность в гормонах щитовидной железы уменьшается, и дозу L-Т4 уменьшают в соответствии с уровнем ТТГ в крови. Необходимо помнить, что период полувыведения Т4 длительный, вследствие чего определять уровень ТТГ в крови следует не ранее чем через 4 недели после изменения дозы L-Т4. Эксперты Национальной академии клинической биохимии США считают, что с практической точки зрения минимальная тиреоидная недостаточность, как стадия гипотиреоза, должна приниматься во внимание для назначения заместительной терапии. При подборе лечения рекомендуется поддерживать уровень ТТГ в крови в пределах от 0,5 до 1,5 мМЕ/л.
Вторичный гипотиреоз у взрослых: диагностика и лечение
Полный текст:
Аннотация
Вторичный гипотиреоз – редкая патология, при диагностике и лечении которой возникает ряд вопросов и трудностей. Выделяют казуистически редко встречающуюся врожденную и приобретенную формы данного заболевания. Основными причинами вторичного гипотиреоза у взрослых являются опухоли гипоталамо-гипофизарной области и состояния после оперативного и лучевого воздействия на эту область. Гормонально активные и неактивные макроаденомы гипофиза служат причиной развития приобретенного вторичного гипотиреоза более чем в 50% случаев. При лучевой терапии опухолей головного мозга развитие вторичного гипотиреоза возможно спустя годы после проведенного лечения. Как и при первичном гипотиреозе, клинические проявления вторичного гипотиреоза неспецифичны. Диагностика и лечение данного заболевания зачастую осложняются его сочетанием с недостаточностью других тропных гормонов. Основу диагностики вторичного гипотиреоза составляют анамнестические данные и лабораторные показатели – одновременное определение концентрации св.Т4 и ТТГ. Содержание св.Т4 на сегодняшний день также используют как основной маркер адекватности дозы L-Т4 при лечении вторичного гипотиреоза. Результаты недавно проведенных работ позволяют оптимизировать заместительную терапию при вторичном гипотиреозе, однако до настоящего времени остается неизученным вопрос использования дополнительных биохимических маркеров для оценки адекватности заместительной терапии.
Ключевые слова
Для цитирования:
Киеня Т.А., Моргунова Т.Б., Фадеев В.В. Вторичный гипотиреоз у взрослых: диагностика и лечение. Клиническая и экспериментальная тиреоидология. 2019;15(2):64-72. https://doi.org/10.14341/ket10303
For citation:
Kienia T.A., Morgunova T.B., Fadeyev V.V. Secondary hypothyroidism in adults: diagnosis and treatment. Clinical and experimental thyroidology. 2019;15(2):64-72. (In Russ.) https://doi.org/10.14341/ket10303
Введение
Вторичный гипотиреоз (ВтГ) – клинический синдром, развивающийся вследствие недостаточной продукции тиреотропного гормона (ТТГ) при отсутствии первичной патологии самой щитовидной железы (ЩЖ), которая бы могла привести к снижению ее функции. В отличие от первичного гипотиреоза ВтГ одинаково часто диагностируется как у мужчин, так и у женщин; его распространенность в популяции, по разным данным, варьирует от 1 : 16000 до 1 : 100000 населения в зависимости от возраста и этиологии [1, 2].
Выделяют врожденную и приобретенную формы ВтГ. Причиной казуистически редко встречающегося врожденного ВтГ, как правило, являются генетические нарушения в таких генах, как TRHR, POU1F1, PROP1, HESX1, SOX3, LHX3, LHX4 и TSHB [3]. Распространенность этой патологии по данным неонатального скрининга в Нидерландах составляет 1 : 16000, в Японии и Индиане (США) 1 : 160000 новорожденных [4–6]. Столь значительная разница может быть объяснена тем, что в Японии и США программа скрининга включает определение концентрации ТТГ и Т4, в то время как в Нидерландах интерпретация отношения ТТГ/Т4 проводилась с учетом содержания тироксин-связывающего глобулина (ТСГ).
Приобретенный ВтГ у детей наиболее часто развивается при краниофарингиоме и вследствие ее хирургического и лучевого лечения [2]. Так, по данным E.N. Gonc и соавт., ВтГ развивается у 75% пациентов. При этом дефицит гормона роста (ГР) наблюдается в 100% случаев, а дефицит гонадотропинов – в 80% случаев [7].
У взрослых за крайне редким исключением встречается приобретенный ВтГ, основными причинами которого являются опухоли гипоталамо-гипофизарной области, а также состояния после оперативного и лучевого воздействия на гипоталамо-гипофизарную область [8]. Так, более чем в 50% случаев причиной приобретенного ВтГ являются гормонально активные и неактивные макроаденомы гипофиза [11]. После лучевой терапии опухолей головного мозга ВтГ развивается в 65% случаев, причем произойти это может спустя годы после проведенного лечения [9, 10]. Такое отсроченное развитие недостаточности ТТГ является одной из причин недооценки распространенности данной патологии. Не меньшее значение, вероятно, имеет отсутствие четких и общепринятых диагностических критериев ВтГ. Недостаточность тропных гормонов, как правило, развивается после лучевого воздействия на аденогипофиз в суммарной дозе 20 Гр и более. При этом поражение тиреотрофов имеет дозозависимый характер: по данным M.D. Littley и соавт., в течение 5 лет ВтГ развился у 9% пациентов, получавших лучевую терапию в суммарной дозе 20 Гр, и у 52% пациентов, получавших лучевую терапию в дозе более 40 Гр [12]. При краниоспинальном облучении возможно развитие так называемого смешанного гипотиреоза – термин впервые был введен S. Rose и соавт. и предполагает сочетанное радиационное поражение как гипоталамуса, так и щитовидной железы. Другой причиной развития ВтГ у взрослых может быть тяжелая травма головного мозга: распространенность гипотиреоза у таких пациентов составляет, по данным разных авторов, от 5 до 29%, что определяется тяжестью травмы, а также временем, прошедшим с ее момента [13–15].
Причиной развития ВтГ у взрослых может быть поздно манифестирующая краниофарингиома: распространенность гипотиреоза у таких пациентов составляет около 40%, дефицит ГР – 80–90%, дефицит гонадотропинов – 70% и АКТГ – 40%. Оперативное лечение этих пациентов приводит в большинстве случаев к развитию гипопитуитаризма, при этом ВтГ развивается у 78–95% пациентов [8].
В последнее время в литературе появились сообщения о развитии недостаточности аденогипофиза на фоне терапии противоопухолевыми препаратами из группы ингибиторов цитотоксического Т-лимфоцит-ассоциированного антигена 4 (CTLA-4). У пациентов, получающих терапию этими моноклональными антителами, частота развития гипофизита достигает 10% [8]. Так, гипофизит, развившийся на фоне терапии ипилимумабом, характеризуется множественной недостаточностью тропных гормонов; у этих пациентов наиболее часто развивается ВтГ (до 90% случаев), реже вторичная надпочечниковая недостаточность и вторичный гипогонадизм [16].
Особенности клинической картины и диагностики ВтГ
Как и при первичном гипотиреозе, клинические проявления ВтГ неспецифичны. Их выраженность и характер зависят от этиологии, тяжести повреждения гипоталамо-гипофизарной области, наличия дефицита других тропных гормонов, а также возраста пациента в дебюте заболевания. Наиболее часто пациенты предъявляют жалобы на общую слабость, головную боль, подавленное настроение, непереносимость холода, сухость кожи, репродуктивные или сексуальные расстройства. Выраженность симптомов при ВтГ, как правило, меньше, чем при первичном [8, 17]. По мнению ряда авторов, менее выраженные клинические проявления при ВтГ могут быть обусловлены сохраняющейся остаточной секрецией ТТГ, неизмененной ЩЖ, а также базальной физиологической активностью рецептора к ТТГ [18, 19].
Изолированный ВтГ встречается крайне редко – в большинстве случаев он сопровождается недостаточностью других тропных гормонов (см. рисунок), что чаще всего и определяет клиническую картину [20, 21]. Представленная на рисунке “классическая” последовательность развития дефицита аденогипофизарных функций была описана во второй половине ХХ века и отражала соответствующий ей уровень лабораторной диагностики; на самом деле эта последовательность может быть совершенно любой и зависеть от использованных критериев – точек разделения в стимуляционных тестах.
Рисунок. “Классическая” последовательность нарушения секреции гормонов гипофиза на фоне роста опухоли гипофизарной области.
Диагностика ВтГ на основании клинической картины вызывает значительные трудности, и основную роль в этом плане играют лабораторные методы. Как правило, отправной точкой для обследования пациента на предмет ВтГ является анамнез хирургического вмешательства на гипоталамо-гипофизарной области или выявление крупной аденомы или краниофарингиомы, которые потенциально могут приводить к гипопитуитаризму. Реже ВтГ диагностируется при обследовании по поводу выявления низкой концентрации ТТГ (и Т4), определение которого проводилось без прямых показаний. Классическим лабораторным критерием диагностики ВтГ является сочетание низкой концентрации ТТГ и низкой концентрации Т4 в сыворотке крови, но эта ситуация, как выяснилось в 90-х гг. прошлого века, далеко не единственный возможный вариант: концентрация ТТГ при ВтГ может быть как низкой, так и нормальной и даже слегка повышенной; в последнем случае определяемый иммунометрически ТТГ не обладает биологической активностью, поскольку находится в гликозилированном состоянии [17, 22]. Впервые это было показано в работах итальянского эндокринолога Paolo Beck-Pecoz.
Тиреотропный гормон имеет в составе три N-концевые цепи (2 на α-субъединице и 1 на β-субъединице), которые в процессе трансляции гликозилируются при помощи специальных трансфераз. Получены данные о том, что механизм отрицательной обратной связи в системе гипофиз–ЩЖ реализуется в том числе путем изменения активности этих трансфераз. То есть тиролиберин (ТРГ), регулируя биосинтез ТТГ, влияет на высвобождение ТТГ и посттрансляционный процессинг его олигосахаридных цепей. Таким образом снижается как количество синтезируемого ТТГ, так и его биоактивность. Интересно, что при ВтГ, когда биологическая активность ТТГ снижена (низконормальная или низкая концентрация св.Т4 при нормальной или высокой концентрации ТТГ), длительное назначение ТРГ может приводить к восстановлению биологической активности ТТГ. Присутствие ТРГ необходимо для биосинтеза ТТГ, комплементарного рецептору на тиреоците [23, 24]. Таким образом, высоконормальный ТТГ или даже высокая концентрация ТТГ при низкой концентрации св.Т4 характерны для поражения на уровне гипоталамуса [22, 25].
Основным критерием диагностики ВтГ является концентрация св.Т4. Исследование содержания в крови общего Т4 нецелесообразно, поскольку оно зависит от концентрации ТСГ, которая в свою очередь весьма изменчива. Так, концентрация ТСГ снижается с возрастом, при назначении препаратов андрогенов; увеличивается во время беременности, при приеме эстрогенов, оральных контрацептивов и тамоксифена. Кроме того, изменение концентрации ТСГ будет наблюдаться при нарушении функции печени, недостаточном питании и других заболеваниях [26].
После появления синтетического тиролиберина в 1969 г. в диагностике ВтГ стал использоваться стимуляционный тест с ТРГ. Несмотря на существование его различных препаратов (подкожные, для приема внутрь, внутримышечные, ректальные), при проведении стимуляционного теста применяется раствор для внутривенного введения, так как в этом случае может быть получен наиболее быстрый ответ на стимуляцию. В современной версии теста концентрацию ТТГ определяют через 20–30 и 60 мин после введения 200–500 мг ТРГ. На сегодняшний день не существует общепринятой точки разделения для стимулированного ТТГ, характеризующего нормальный ответ на ТРГ. Считается, что концентрация ТТГ около 10 мкЕд/мл на 20–30-й минуте теста и ее постепенное снижение примерно на 8 мкЕд/мл в течение последующих 30 мин может расцениваться как адекватная реакция. Однако повышение концентрации ТТГ уже более 5,5 мкЕд/мл рекомендуется трактовать как адекватный ответ. В случае гипофизарной недостаточности повышения концентрации ТТГ не происходит либо оно незначительно и сглажено. При гипоталамической недостаточности пик концентрации ТТГ отсрочен и приходится на 60-ю минуту [27, 28, 29]. Именно стимуляционный тест с тиролиберином использовался S. Rose и соавт. для дифференциальной диагностики первичного и вторичного гипотиреоза при обследовании пациентов, получивших краниоспинальное облучение. При этом авторы указывают, что суточный ритм секреции ТТГ является более значимым при диагностике ВтГ, чем тест с тиролиберином. Это связано с тем, что даже адекватное повышение концентрации ТТГ на фоне теста с тиролиберином не позволяет исключить наличие скрытого ВтГ, связанного с нарушением суточного ритма ТРГ и ТТГ и отсутствием ночных пиков секреции ТТГ. Авторы предлагают следующие критерии диагностики ВтГ: 1) нарушение суточного ритма секреции ТТГ; 2) недостаточный или отсроченный пик секреции ТТГ после введения ТРГ; 3) отсроченное снижение концентрации ТТГ после введения ТРГ. Присутствие хотя бы одного из вышеуказанных признаков расценивается как критерий наличия ВтГ [13].
Поскольку используемые в рутинной практике лабораторные методы позволяют достаточно точно определить концентрацию ТТГ и св.Т4, необходимость проведения стимуляционного теста с ТРГ существенно снизилась – по сути он является дополнительным шагом в подтверждении диагноза ВтГ. Кроме того, особенно у детей, введение ТРГ сопряжено с риском возникновения ряда нежелательных явлений (наиболее часто тошноты, гиперемии) [30]. Также следует учитывать существующие меж- и внутрииндивидуальные отличия ответа ТТГ на введение ТРГ, ответ также может зависеть от пола, возраста, адекватности синтеза других гормонов гипофиза, что еще больше усложняет интерпретацию теста с ТРГ [31].
Таким образом, на сегодняшний день в основе диагностики ВтГ лежит одновременное определение концентрации св.Т4 и ТТГ.
Заместительная терапия при ВтГ
Как и при первичном гипотиреозе, для лечения ВтГ используется монотерапия левотироксином, коррекция дозы которого традиционно осуществляется под контролем содержания св.Т4 в сыворотке крови. Так же, как и для диагностики ВтГ, определять концентрацию общего Т4 для оценки адекватности заместительной терапии в большинстве рекомендаций считается нецелесообразным, поскольку концентрация общего Т4 в большей мере, чем св.Т4, искажается рядом дополнительных факторов.
Известно, что у пациентов с компенсированным (по содержанию ТТГ) первичным гипотиреозом концентрация св.Т4 выше, чем у здоровых людей [33]. Таким образом, можно предположить, что для поддержания реального эутиреоза пациентам с ВтГ также требуется достижение более высокого содержания св.Т4, чем в референсном диапазоне.
Согласно рекомендациям Американской тиреоидной ассоциации (АТА), целью заместительной терапии при ВтГ служит поддержание концентрации св.Т4 в верхней половине референсного диапазона. Гипотетически целевой показатель концентрации св.Т4 может быть ниже для пожилых пациентов и пациентов с тяжелыми сопутствующими заболеваниями. Вместе с тем эти рекомендации носят эмпирический характер и не подкрепляются какими-либо данными проспективных исследований; они основаны на ряде небольших ретроспективных работ и одном непродолжительном рандомизированном исследовании, продемонстрировавшем снижение веса, индекса массы тела (ИМТ), содержания холестерина и креатинкиназы, а также уменьшение выраженности симптомов гипотиреоза у пациентов, получавших относительно большие дозы L-Т4 и имевших более высокую концентрацию св.Т4 [32].
Рекомендации Европейской тиреоидной ассоциации (ЕТА), вышедшие в 2018 г., в целом созвучны с рекомендациями АТА. Согласно рекомендациям ЕТА, при заместительной терапии ВтГ доза L-Т4 составляет около 1,21–1,6 мкг/кг/сут для пациентов моложе 60 лет и 1,0–1,2 мкг/кг/сут для лиц старше 60 лет. При этом в качестве цели терапии предлагается поддержание концентрации св.Т4 выше медианы референсного диапазона. Однако для лиц 75 лет и старше как целевой может рассматриваться низкий (низконормальный) уровень св.Т4 [34].
В реальной клинической практике высоконормальная концентрация св.Т4 достигается далеко не у всех пациентов. По данным ряда исследований, у пациентов с ВтГ, получающих заместительную терапию L-T4, концентрация св.Т4 оказалась ниже, чем у пациентов с компенсированным первичным гипотиреозом. Так, по данным О. Koulouri и соавт., у пациентов с ВтГ концентрация св.Т4 на 2–3 пмоль/л ниже в сравнении с аналогичной группой пациентов с компенсированным первичным гипотиреозом. При этом содержание св.Т4 в группе пациентов с ВтГ не всегда находилось в верхней половине референсного диапазона, а у 20% пациентов концентрация св.Т4 была ниже 10-го перцентиля. Соответственно возникает вопрос о возможной избыточности дозы L-T4 у пациентов с ВтГ при поддержании св.Т4 в верхней трети референсного диапазона, ведь в соответствии с данными О. Koulouri и соавт. концентрация св.Т4 выше 15–16 пмоль/л будет превышать таковую у 30–50% пациентов с первичным гипотиреозом, компенсированным по данным ТТГ [35].
Такая неопределенность закономерно приводит к вопросу и о концентрации св.Т3, общего Т4 и общего Т3 на фоне заместительной терапии L-T4 при ВтГ. Интересные данные были получены в небольшом проспективном исследовании E. Ferretti и соавт. В него были включены 37 пациентов с подтвержденным ВтГ, получающих заместительную терапию L-T4. Всем пациентам L-T4 был полностью отменен с последующим возобновлением приема через 2 мес. После отмены тироксина концентрация св.Т4 упала ниже референсного диапазона у всех пациентов, в то время как концентрация св.Т3, общего T4 и общего T3 оказалась низкой лишь в 73, 57 и 19% случаев соответственно. Концентрация ТТГ была ниже 0,2 мкЕд/мл у 19% пациентов, в пределах референсного диапазона – у 70% и слегка повышена – у 11% пациентов. Как указывалось, при ВтГ концентрация ТТГ исходно может быть снижена, слегка повышена или находиться в пределах референсного диапазона, при этом если на момент диагностики ВтГ концентрация ТТГ находится в пределах референсного диапазона или повышена, то назначение даже малых доз L-T4 может привести к его полной супрессии [22]. Это, вероятно, связано с тем, что образующиеся при ВтГ биологически неактивные формы ТТГ подавляются гораздо быстрее, чем нативный ТТГ [25]. В связи с этим ряд авторов делают выводы о том, что на фоне адекватной заместительной терапии ВтГ содержание ТТГ должно быть снижено у большинства пациентов.
Возвращаясь к исследованию E. Ferretti и соавт., при возобновлении в нем приема L-T4 в дозе 50 мкг/сут закономерно отмечалось повышение концентрации тиреоидных гормонов, при этом концентрация св.T4 оставалась ниже референсного диапазона у 73% пациентов, а концентрация общего Т4, общего Т3 и св.Т3 нормализовалась в 75% случаев. При назначении полной расчетной заместительной дозы L-T4 отмечалась нормализация как общих, так и свободных форм тиреоидных гормонов, но у существенной части пациентов (8 из 37) концентрация общего Т4 была выше референса при нормальных значениях св.Т4, св.Т3 и общего Т3. Полученные в этом исследовании данные, вероятно, подтверждают тот факт, что концентрация св.Т4 является наиболее чувствительным показателем для оценки адекватности заместительной терапии при ВтГ [36].
Наряду с целевым показателем неоднозначным является вопрос о расчетной дозе L-T4 пациентам с ВтГ. Так, по мнению ряда авторов, которое опять же не имеет экспериментальных подтверждений, для пациентов молодого возраста расчетная доза L-T4 составляет около 1,3–1,6 мкг/кг массы тела и примерно 1,0 мкг/кг для пациентов старшей возрастной группы [36, 37].
Поскольку изолированный ВтГ у взрослых практически не встречается, вполне закономерно, что доза L-T4 будет зависеть от наличия и выраженности недостаточности других тропных гормонов, а также проводимой заместительной терапии. При назначении заместительной терапии эстрогенами, как правило, требуется увеличение дозы L-T4, поскольку возрастает содержание ТСГ. Кроме того, как известно, при назначении заместительной терапии ГР может впервые обнаружиться ВтГ либо потребоваться увеличение дозы L-T4 [38]. Предполагается, что ГР может ингибировать периферическое превращение T4 в T3, а также оказывать ингибирующее действие на высвобождение ТТГ.
O. Alexopoulou и соавт. провели ретроспективное исследование, в рамках которого оценивали компенсацию ВтГ и недостаточность других тропных гормонов, а также дозу L-T4 в зависимости от параллельно проводимой заместительной терапии гипогонадизма, гипокортицизма и недостаточности ГР. В исследование было включено 108 взрослых пациентов, у 28 из них диагноз ВтГ был установлен в детском возрасте. В среднем доза L-T4 составила 1,6 мкг/кг в сутки, не зависела от пола пациента, но находилась в обратной зависимости от возраста. Также было выявлено, что пациенты, заболевшие в детстве, нуждались в назначении большей дозы L-Т4 по сравнению с пациентами, манифестация ВтГ у которых произошла во взрослом возрасте (1,98 ± 0,56 vs 1,48 ± 0,41 мкг/кг, р< 0,001). Пациенты, получающие заместительную терапию по поводу множественной гипофизарной недостаточности, нуждались в назначении большей дозы L-Т4 [17, 39].
В течение последних 10–15 лет были опубликованы работы по изучению целесообразности назначения комбинированной терапии левотироксином и трийодтиронином (L-T4 + T3) пациентам с гипотиреозом. Хорошо известно, что Т4 является основным гормоном, продуцируемым щитовидной железой, и лишь 10–15 мкг в сутки синтезируется Т3. Т3 является биологически более активным гормоном, чем тироксин, и основным его источником служит периферическое дейодирование, преимущественно в печени и почках. Основанием для проведения исследований по применению комбинированной терапии L-T4 + T3 служила гипотеза о недостаточном дейодировании Т4 в Т3 на фоне монотерапии L-T4 и, как следствие, возможных преимуществах комбинации по сравнению с монотерапией L-T4. В большинство подобных работ включались пациенты с первичным гипотиреозом, однако в исследование S. Slawik и соавт. были включены пациенты с ВтГ. В исследовании участвовало 29 человек с гипопитуитаризмом, возраст пациентов составил 52 ± 2 года. Они были разделены на 3 группы: монотерапии L-T4 в дозе 1,0 мкг/кг массы тела, 1,6 мкг/кг и комбинированной терапии L-T4 + Т3. В работе оценивались показатели липидного спектра, ИМТ, скорость коленного рефлекса, выраженность симптомов гипотиреоза, когнитивные функции и качество жизни. Лучшие результаты отмечались в группе, получавшей монотерапию L-Т4 в дозе 1,6 мкг/кг массы тела. При этом концентрация св.Т4 находилась у них в верхней трети референсного диапазона [37].
На сегодняшний день недостаточно данных, позволяющих сделать вывод об отдаленных последствиях применения различных доз L-T4 [32].
Целесообразно ли использование периферических маркеров эффектов тиреоидных гормонов для оценки адекватности дозы L-T4 при ВтГ?
Идеальной моделью заместительной терапии является назначение L-T4 при первичном гипотиреозе, поскольку, определяя концентрацию ТТГ в качестве контрольного параметра, мы фактически оцениваем количественно реакцию клеток-мишеней (тиреотрофов) на содержание циркулирующих тиреоидных гормонов. Совершенно закономерно, даже при первичном гипотиреозе многие исследователи рассуждают о том, что неплохо было бы неким образом оценить реакцию на концентрацию тиреоидных гормонов (то есть адекватность заместительной дозы) и других клеток или тканей – например, головного мозга, мышц, жировой ткани и т.д. Отсюда возникла концепция так называемых периферических маркеров эффектов тиреоидных гормонов, к которым были отнесены такие неспецифические параметры, как ЛПНП, глобулин, связывающий половые гормоны (ГСПГ) и ряд других.
При вторичном гипотиреозе этот вопрос еще более актуален, поскольку определение концентрации ТТГ с целью оценки адекватности терапии в данном случае невозможно, а оценка концентрации св.Т4 на фоне терапии L-T4 фактически оценивает не реакцию на содержание тиреоидных гормонов органов-мишеней, а фармакокинетику препарата L-T4.
Таким образом, при ВтГ ряд биохимических (липидный спектр, ГСПГ, маркеры костного метаболизма, креатинкиназа) и клинических параметров (симптомы гипотиреоза, качество жизни, масса тела) можно потенциально рассматривать в качестве дополнительных критериев для оценки адекватности проводимой терапии L-T4. Однако надо учитывать, что на концентрацию большинства из них влияют не только тиреоидные гормоны, но также и половые гормоны, ГР, кортизол – то есть они неспецифичны и сложны для интерпретации, особенно при проведении комбинированной терапии пангипопитуитаризма. Вероятно, за исключением холестерина остальные маркеры скорее будут полезны для выявления передозировки L-T4, чем для подтверждения недостаточной дозы.
В работе Е. Ferretti и соавт. в качестве периферических маркеров эффектов тиреоидных гормонов использовали липидный профиль (общий холестерин, ЛНП, ЛВП, триглицериды), активность креатининкиназы, АЛТ, АСТ, АПФ, карбокси-терминальной телопептидазы коллагена 1 типа (ICTP), содержание ферритина, ГСПГ, остеокальцина (BG-P), растворимого рецептора интерлейкина-2 (sIL-2R) [36]. У всех пациентов определяли указанные параметры на фоне заместительной терапии L-T4, после отмены препарата и возобновления его приема. При исследовании биохимических показателей изменения были отмечены в содержании свободного холестерина, ЛНП, активности креатининкиназы и АСТ – после прекращения приема L-T4 их содержание и активность были выше нормальных значений в 95, 89, 54 и 33% случаев соответственно. При этом увеличение активности креатининкиназы было наиболее значимым (р < 0,0001). Концентрации ГСПГ и маркеров костного метаболизма в значительной степени зависели от пола и наличия/отсутствия гипогонадизма. Фактически, в соответствии с полученными данными, эти показатели можно расценивать как маркеры периферических эффектов тиреоидных гормонов только у мужчин без гипогонадизма. Кроме того, концентрация остеокальцина и ICTP была значительно ниже у пациентов, получавших заместительную терапию гидрокортизоном (р < 0,05). При возобновлении приема L-T4 и последующем увеличении дозы препарата значимая корреляция наблюдалась между содержанием св.Т3 и sIL-2R (р < 0,0001). Принимая во внимание тот факт, что содержание sIL-2R не зависит от наличия гипогонадизма и приема глюкокортикоидов, авторы утверждают, что он может рассматриваться как маркер передозировки L-T4.
Из дополнительных инструментальных методов исследования в литературе обсуждается возможность проведения ЭхоКГ. J. Abucham и соавт. провели исследование, целью которого было выявление эхокардиографических показателей, свидетельствующих о компенсации ВтГ. В исследование было включено 35 пациентов с гипоталамо-гипофизарными заболеваниями и 30 пациентов с первичным гипотиреозом (манифестным и субклиническим). В группу пациентов с гипоталамо-гипофизарными заболеваниями были включены больные как со сниженным, так и с нормальным содержанием св.Т4. Затем последние на основании данных эхокардиографии были разделены на пациентов с эутиреозом и пациентов с субклиническим гипотиреозом. Эхокардиографические признаки гипотиреоза (снижение систолической и диастолической функции левого желудочка, уменьшение сократительной активности миокарда) были выявлены у 9 из 10 пациентов с субклиническим гипотиреозом и у 14 из 25 пациентов (56%) с гипоталамо-гипофизарными заболеваниями и нормальной концентрацией св.Т4. Далее всем пациентам с диагностированным гипотиреозом (манифестным и субклиническим) был назначен L-T4. По достижении целевых показателей (ТТГ в пределах референсного диапазона при первичном гипотиреозе, св.Т4 в верхней половине референсного диапазона и нормальный св.Т3 при ВтГ) повторно проводилось эхокардиографическое исследование. В результате было выявлено значительное улучшение эхокардиографических показателей как у пациентов с первичным гипотиреозом, так и у пациентов с ВтГ. Из этого авторы делают вывод, что ЭхоКГ может использоваться как дополнительный метод контроля ВтГ у пациентов с гипоталамо-гипофизарными заболеваниями [40].
Заключение
Несмотря на то, что за последние несколько лет были опубликованы результаты ряда исследований, посвященных ВтГ, требуется дальнейшее изучение вопросов его диагностики и лечения у взрослых. Результаты недавно проведенных работ позволяют оптимизировать заместительную терапию при ВтГ, однако до настоящего времени остается неизученным вопрос использования дополнительных биохимических маркеров для оценки адекватности заместительной терапии.
Важно отметить, что выделение ВтГ в отдельное заболевание и обсуждение его заместительной терапии неизбежно, но в реальной клинической практике достаточно схематично и искусственно, поскольку на самом деле перед нами почти всегда предстают пациенты с недостаточностью сразу нескольких аденогипофизарных функций. Совершенно очевидно, что гипофизарная недостаточность – это не механическая сумма того, что мы знаем о дефиците отдельных тропных гормонов, а качественно другое состояние (1 + 1 здесь не равно 2). Это проявляется во взаимном влиянии дефицита тропных гормонов на данные лабораторной диагностики, взаимном и разнонаправленном влиянии на эти показатели заместительной терапии сразу несколькими гормональными препаратами. Заместительная терапия недостаточности тропных гормонов на сегодняшний день проводится почти исключительно эмпирически: мы назначаем фиксированные дозы половых гормонов при вторичном гипогонадизме, эмпирическую дозу гидрокортизона при вторичном гипокортицизме и определяемую фармакокинетически дозу L-T4 при вторичном гипотиреозе. Заместительная терапия дефицита гормона роста у взрослых в реальной клинической практике проводится достаточно редко, но как ее отсутствие, так и назначение может изменить лабораторные параметры, используемые одновременно как для диагностики, так и для лечения. Таким образом, в реальной клинической практике диагностика и лечение гипопитуитаризма, неотъемлемой частью которого является вторичный гипотиреоз, представляет собой многомерную модель с многочисленным взаимным влиянием ее компонентов. На сегодняшний день проблема заместительной терапии ВтГ по большей части все еще решается эмпирически и мы находимся лишь в начале пути в своих попытках ее объективизации.
Дополнительная информация
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Источник финансирования. Поисково-аналитическая работа и подготовка настоящей публикации осуществлены на личные средства авторского коллектива.
Участие авторов: все авторы внесли равный вклад в проведение поисково-аналитической работы и подготовку статьи, прочли и одобрили финальную версию до публикации.