Как узнать строение молекулы
Одним из основополагающих понятий современной науки является понятие молекулы. Его введение европейскими учеными в 1860 г. дало толчок к развитию не только химии и физики, но и других естественных наук.
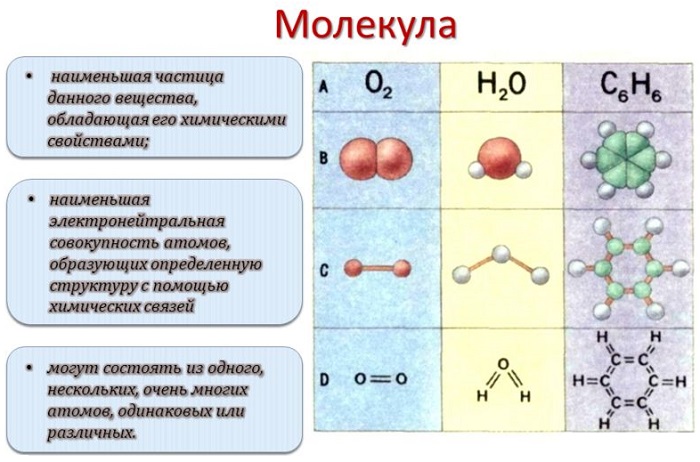
Молекулой, в наиболее общем определении, называется частица, образованная из нескольких (двух или более) атомов, объединенных между собой ковалентными связями. Она не имеет электрического заряда, все электроны в её составе имеют пару.
Молекулы, несущие заряд, называются ионами, неспаренные электроны – радикалами. Качественный и количественный состав их стабилен. Количество ядер атомов, электронов и их взаимное расположение позволяют отличать молекулы разных веществ друг от друга.
Что такое молекула в физике
В физике этим понятием оперируют при изучении свойств разных сред (газы, жидкости) и твердых тел.
Также их свойствами объясняются явления диффузии, теплопроводности и вязкость веществ.
Что такое молекула в химии
Учение о молекулах для химической науки является одним из самых главных. Именно химические исследования дали важнейшие сведения о составе и свойствах этой мельчайшей единицы вещества.
При прохождении химического превращения молекулы обмениваются атомами, распадаются. Поэтому знания о строении и состоянии этих частиц лежат в основе изучения химии веществ и их превращений.
На основании знаний о проходящей химической реакции можно предсказать строение молекул веществ, в ней участвующих. Противоположное заключение тоже будет верным: на основании сведений о строении молекулы вещества реально предсказать его поведение во время химической реакции.
Строение молекулы
Понятие о строении включает геометрическую структуру и распределение электронной плотности.
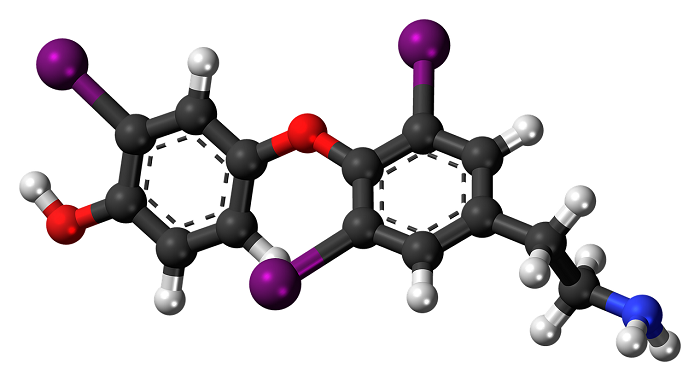
В качестве примера рассмотрим строение наименьшей частицы воды.
Существует несколько способов взаимодействия атомов. Основным способом являются химические связи, благодаря им поддерживается стабильное существование молекул. Прочие (неосновные) взаимодействия происходят между теми атомами, которые не связаны непосредственно.
Виды химической связи:
Водородная — основана на способности атома водорода образовывать дополнительную связь при смещении от него электронной плотности.
Связи характеризуются следующими показателями:
длина – степень удаления друг от друга ядер атомов, образовавших связь;
энергия – сила, прилагаемая для разрушения связи;
полярность – смещение электронного облака к одному из атомов;
порядок или кратность – количество пар электронов, образовавших связь.
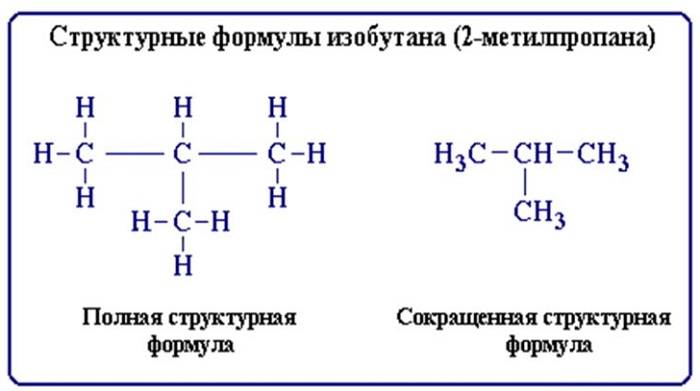
Строение молекул условно отражается структурными формулами. Основные взаимодействия атомов, при составлении таких формул, отображается черточками. В таких формулах связи образуют неразрывную цепь и иллюстрируют валентности образовавших их элементов (атомов).
Структурные формулы также отражают то, как выглядит молекула (линейная, циклическая, наличие радикалов и т. д.).
Масса (размер) молекулы
В зависимости о количества ядер атомов, входящих в их состав, можно выделить молекулы двухатомные, трехатомные и т. д.
В том случае, если количество атомов велико, молекула носит название макромолекулы.
Путем сложения масс атомов, входящих в состав частицы, можно определить молекулярную массу. В зависимости от её величины, все вещества делят на высоко- и низкомолекулярные.
Свойства молекулы
Современная наука выделяет следующие свойства молекул:
Знания о свойствах и строении молекул являются основополагающими для развития теоретических и прикладных наук и играют важную роль в жизни человека.
Молекула. Строение и типы химических связей
Молекула — совокупность двух или более атомов, образующих наименьшее целое, на которое можно разделить чистое вещество, сохраняя при этом состав и его химические свойства (способность вступать в соединения, вкусовые свойства, свойства растворимости).
Молекула является одной из фундаментальных концепций современной науки. Впервые ввели эту концепцию европейские учёные в 1860 году, что послужило основой для развития химии, физики и ряду других естественных наук.
Молекула, по самому общему определению, — это частица, сформированная из нескольких (двух и более) атомов, связанных друг с другом ковалентной связью. Она не имеет электрического заряда, и все электроны в ее составе парные.
Молекулы, имеющие заряд, называются ионами, а непарные электроны — радикалами. Их качественный и количественный состав остается постоянным. Число ядер атомов, электронов и их взаиморасположение помогают различать молекулы разных веществ между собой.
Что такое молекула в физике
В физике термин молекула используется для описания характеристик газов, жидкостей и твердых тел. Мобильность молекул напрямую зависит от способности вещества к диффузии, его вязкости, теплопроводности и т. д. Впервые прямое экспериментальное подтверждение факта существования молекул получил французский физик Жан Перрен в 1906 году во время изучения броуновского движения.
Что такое молекула в химии
Для химической дисциплины изучение молекул играет одну из самых важных ролей. Благодаря химическим исследованиям была получена важнейшая информация о составе и характеристиках этой крошечной единицы материи.
Когда молекулы проходят через химические превращения, они обмениваются атомами и распадаются. Именно поэтому знания о строении и состоянии данных частиц являются основой для изучения химии веществ и их преобразования.
Основываясь на имеющихся знаниях о происходящих химических реакциях, мы имеем возможность прогнозировать структуру молекул задействованных в них веществ. Верен и обратный вывод: на основании знаний о структуре молекулы вещества вполне реально прогнозировать его поведенческие характеристики в ходе химической реакции.
Строение молекулы
Физико-химические свойства молекул обусловлены их конструктивным строением. Таким образом, многие свойства можно предсказать на основе структурной формулы. К таким свойствам относятся размер, форма, в некоторой степени конформация молекул (т.е. взаимное расположение отдельных атомов), в момент, когда вещество находилось в растворе, и, в заключение, реакционная способность.
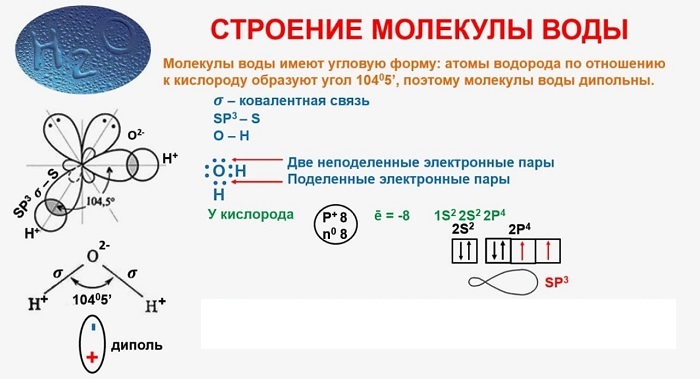
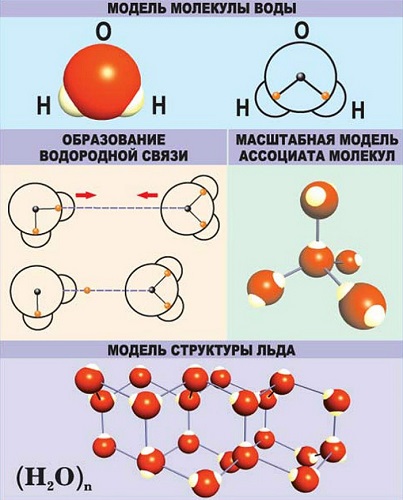
Молекула воды имеет угловую структуру: это равнобедренный треугольник с углом наклона в верхней части 104°5′. Масса молекулы воды в состоянии пара составляет 18 г/моль. Вместе с тем, уровень молекулярной массы воды в жидком состоянии выше. Это указывает на то, что молекулы в жидкой воде связаны водородными связями. Когда вода замерзает, она расширяется (поскольку образуется множество водородных связей), однако лед легче воды, всплывает на ее поверхность, «самая тяжелая вода» при значении +4°C.
Молекула полярна: атом кислорода несет частично отрицательный заряд, а два атома водорода несут частично положительный заряд. Это означает, что молекула воды является диполем. Поэтому взаимодействие молекул воды создает между ними водородные связи, которые сказываются на физических свойствах воды. Благодаря высокой полярности молекул вода является непревзойденным растворителем других полярных соединений. В воде распадается больше веществ, чем в других жидкостях.
Типы химической связи
Связи обозначаются нижеуказанными признаками:
Структура молекул может быть представлена графически (структурной формулой). Главные взаимосвязи атомов в формуле обозначаются штрихами. В подобных структурах связи формируют целостную цепь и демонстрируют валентность элементов (атомов), которые их образовывали.
Структурные формулы также демонстрируют, каков внешний вид молекулы (линейный, циклический, наличие радикалов и т.д.).
В настоящее время интенсивно изучается структура частицы вещества. С этой целью применяются различные эксперименты и теоретические методы. Экспериментальные методы включают рентгеновский структурный анализ, спектроскопию, масс-спектрометрию и др. Теоретические методы включают методы расчета квантовой химии.
Масса (размер) молекулы
В соответствии с количеством ядер атомов могут быть выделены двух-, трехатомные и т.д. молекулы.
Mr — Относительная молекулярная (атомная) масса вещества — отношение массы молекул (или атомов) данного вещества к 1/12 массы атома углерода.
М — молярная масса — масса вещества, взятого в количестве одного моля.
В случае большого количества атомов молекулу называют макромолекулой.
При сложении масс атомов, из которых состоит частица, определяется молекулярная масса. В зависимости от размера молекулярной массы, все химические вещества разделяются на низко- и высокомолекулярные.
Свойства молекулы
В современной науке отмечаются следующие свойства молекул:
Между веществами проводится разграничение:
Изучение свойств и структуры молекул имеет фундаментальное значение для развития теоретической и прикладной науки, а также играет важнейшую роль в жизнедеятельности человека.
Атомы и молекулы
Любые тела и предметы состоят из молекул — мелких частиц, на которые можно раздробить вещество физическими методами (например, растворением). Из этого вытекает определение молекулы: это самая мелкая частица вещества, сохраняющая его химические свойства.
Атомы — это мельчайшие частицы, сохраняющие свойства химического элемента, из них составляются молекулы. Атомы выделяются из молекул химическими методами.
Химические вещества могут быть газообразными, жидкими и твердыми. Частицы твердых веществ расположены ближе, а газов — дальше друг от друга, и они находятся в постоянном движении. Чем выше температура тела, тем быстрее движение молекул и атомов в нем, называемое броуновским, и тем больше расстояние между частицами. Внутри этого «бульона» постоянно действуют силы взаимного притяжения и отталкивания частиц, которые выражены тем сильнее, чем меньше разделяющее их расстояние.
Виды веществ
Вещества определяются как молекулярные и немолекулярные, в зависимости от того, из каких частиц они состоят. Разные типы частиц создают разные виды взаимосвязей, и это определяет физические и химические свойства соединений.
Имеющие молекулярное строение
Здесь связи между отдельными молекулами относительно слабые, поэтому легко разрываются при нагреве, причем тем легче, чем меньше молекулярная масса. Поэтому такие вещества плавятся при низких температурах и в нормальных условиях многие из них находятся в жидком или газообразном состоянии.
Это могут быть простые вещества: сера (S8), азот (N2), кислород (O2) и сложные, например, оксиды азота с разной валентностью (N2O, NO, N2O5, NO3), углекислый газ (CO2), серная кислота (H2SO4).
Самый известный пример такого рода — вода. Человеческое тело содержит около 65% воды. Даже шкала Цельсия привязана к ее плавлению (0°С) и кипению (100°С). В нормальных условиях это жидкость, но в природе встречается во всех трех агрегатных состояниях в виде снега или льда, воды и пара.
Электрическая полярность молекулы задает воде интересные особенности. Например, ее удельная теплоемкость настолько велика, что это делает ее одним из главных регуляторов климата Земли. Интересно, что наибольшей плотности она достигает не в виде льда, а в жидком состоянии, при 4 °C. Поэтому возле дна скапливается самая тяжелая вода, не достигающая замерзания, а более легкий твердый лед выталкивается наверх.
Еще один пример — йод. В нормальных условиях он имеет форму кристаллов, а при нагревании сразу переходит в газообразное состояние, что называется возгонкой.
Строящиеся из немолекулярных частиц
Целые классы соединений состоят не из молекул, а из атомов или ионов. Поскольку электрические связи разнозаряженных ионов или ковалентные атомные связи крепче, чем межмолекулярные, они разрушаются при нагреве гораздо труднее. Поэтому такие вещества, как правило, имеют твердую форму и высокие температуры плавления и кипения. Их определяют как вещества немолекулярного строения.
Примеры:
Таблица молекулярного и немолекулярного строения вещества:
| Строение вещества | Молекулярное | Немолекулярное |
| Мельчайшие структурные единицы | Молекулы | Ионы и атомы |
| Агрегатное состояние | Газообразное, жидкое, твердое | В основном, твердое |
| Температуры плавления и кипения | Низкие | Высокие |
Аморфные и кристаллические вещества
Твердые вещества могут быть аморфными или кристаллическими.
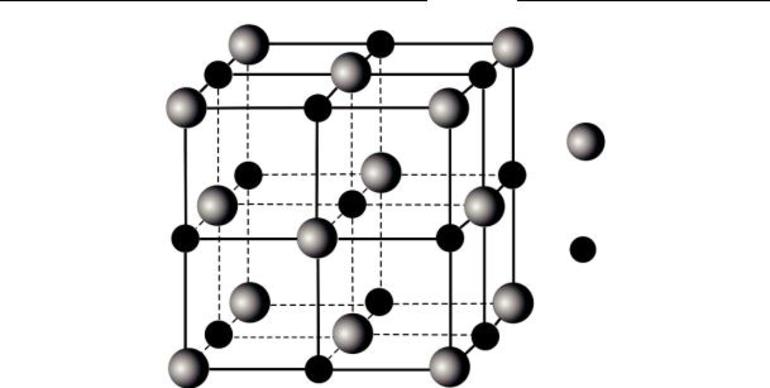
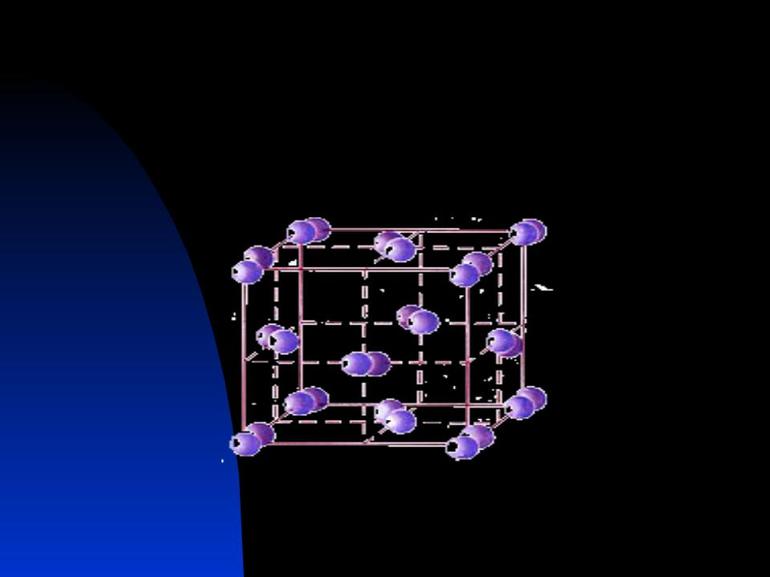
Кристаллические отличаются тем, что их структурные единицы располагаются в повторяющемся порядке, образуя кристаллические решетки.
Аморфные соединения имеют в своем составе длинные тяжелые молекулы, которые не помещаются в правильные структуры кристаллических решеток, и поэтому переход из твердого состояния в жидкое у них совершается постепенно, без четкой границы. То есть аморфные вещества не имеют точно определенной температуры плавления. Очень знакомый пример такого типа — пластилин, который используется в мягком, а не твердом или жидком состоянии. Также это различные пластмассы, смолы, стекло.
Пластичность и мягкость разогретого стекла дает возможность лепить из него, как из пластилина, только не руками, а инструментами. Стеклянная посуда, лампочки, трубки, оконное стекло — все это было бы невозможно сделать из кристаллических веществ. А как выручают человека полиэтиленовые бутылки и фасовочные пакетики!
Еще один близкий пример — сахарная карамель. Она при нагревании становится тягучей, мягкой, как и все аморфные вещества. А если дать карамели залежаться в сухом помещении несколько месяцев, ее поверхность покроется белым налетом маленьких кристаллов сахара. То есть некоторые аморфные вещества способны переходить в кристаллическую форму.
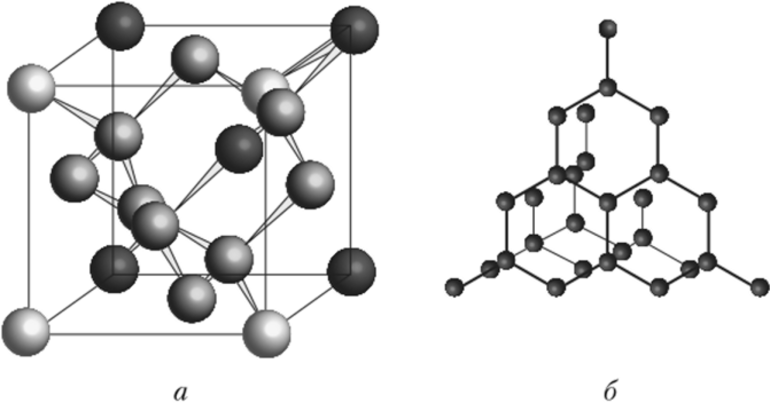
Типы кристаллических решеток
Разные виды частиц образуют разные кристаллические решетки. Существует 4 их типа:
Ионный тип кристалла
Это вид решетки, образуемый ионами — частицами, несущими на себе разноименные электрические заряды, чередующиеся в узлах решетки. Электроотрицательность анионов притягивает к себе положительно заряженные катионы, что придает решетке твердость. Поэтому такие соединения тугоплавки, зато хрупки, обладают хорошей растворимостью в воде и электропроводностью. Это основания, основные оксиды, органические и неорганические соли.
Пример такого кристалла — обычная поваренная соль, хлорид натрия. Его кубическая решетка сформирована катионами Na+ и анионами Cl-.
Атомная решетка
Этот вид кристаллов сформирован атомами, образующими между собой полярные и неполярные ковалентные связи. Такие связи очень прочны, поэтому эти вещества обладают высокой твердостью, тугоплавки и не растворяются в воде. В природе они мало распространены.
Характерный пример — углерод, имеющий две аллотропных формы, и обе — атомного типа.
Кристалл графита имеет слоистую структуру, атомы в слоях расположены по углам шестиугольника, расстояние между слоями значительно больше и межатомные связи слабее, чем внутри слоя. Поэтому кристалл хрупкий, легко расслаивается и крошится. Благодаря этому свойству, графит используется в карандашах или в виде графитовой смазки.
Алмаз — очень плотный кристалл кубической формы, среди природных минералов имеет наивысшую твердость. Образуется такая форма углерода из графита при очень высоких температуре и давлении.
Другие примеры: бор (B), германий (Ge), кремний (Si), оксид кремния (SiO2), карбид (B4C) и нитрид (BN) бора.
Состоящая из молекул
Такая решетка имеет в узлах молекулы. Силы межмолекулярного притяжения относительно слабее, и это определяет свойства веществ с молекулярной кристаллической решеткой — их кристаллы непрочные, плавятся при низких температурах, не электропроводны.
Примеры веществ с молекулярной кристаллической решеткой: полярной ковалентной связью обладает вода (H2O); а соединения неполярной ковалентной связью — твердый оксид углерода (CO2), сера (S8).
Очень интересно, что сера образует два вида кристаллов. В нормальных условиях кристаллы серы имеют интересную усечённо-ромбическую форму, а при 96 °C и выше вырастают длинные игольчатые кристаллы.
Также молекулярные кристаллы образуют многие из твердых органических соединений с достаточно сложной формулой: сахар, глюкоза.
Металлическая решетка
Эта решетка выделяется из общего ряда необычностью строения. Атомы металла, расположенные в узлах решетки, легко расстаются с внешними электронами, что превращает атом в катион, а свободно блуждающие электроны создают делокализованное электронное облако. Эта необычность определяет характерные особенности металлов: ковкость, пластичность, металлический блеск, электро- и теплопроводность.
Ионы более химически активны, чем электронейтральные атомы, этим объясняется способность металлов к поверхностному окислению. Окислы некоторых металлов, например, алюминия, образуют пленку, защищающую поверхность от контакта с кислородом воздуха. Такая особенность даже используется для защиты металлических изделий. Металлы, окислы которых образуют рыхлую структуру (например, железо), подвержены коррозии в гораздо большей степени. Примеры: железо (Fe), серебро (Ag), медь (Cu), алюминий (Al).
Из чего состоит все вокруг или что такое молекула?
Каждый раз, когда два атома соединяются вместе, они образуют молекулу. На самом деле все, что нас окружает – да и мы сами – состоит из триллионов различных типов молекул. Понятие молекулы было принято в 1860 году на международном съезде химиков в Карлсруэ. Согласно принятому определению молекула – это наименьшая частица химического вещества, которая обладает всеми его химическими свойствами (растворимость, вкус, способность вступать в соединения и пр). Введение понятия молекулы подтолкнуло развитие физики, химии и других естественных наук. В более общем понимании молекулой называют частицу, образованную из двух или более атомов, соединенных между собой ковалентными связями.
Молекула воды содержит 1 атом кислорода и 2 атома водорода
Атом – мельчайшая частица вещества, которая обладает всеми его физическими свойствами (цвет, твердость, плотность и пр.)
Когда атомы различных типов элементов соединяются вместе, они образуют молекулы, называемые соединениями. Так, вода состоит из сложных молекул, состоящих из 2 атомов водорода и 1 атома кислорода. Вот почему она называется H2O: у молекулы воды всегда будет в 2 раза больше атомов водорода, чем атомов кислорода. Существует чуть более 100 типов атомов, но типов различных веществ миллионы. Причина такого неравенства кроется в том, что они состоят из различных типов молекул.
Важно понимать, что молекулы состоят не только из различных типов атомов, но и из различных соотношений. Как и в приведенном выше примере с водой, молекула воды состоит из двух атома водорода и одного атома кислорода, что записывается как H2O. Другими примерами являются углекислый газ (C02), аммиак (NH3) и сахар или глюкоза (C6H12O6). Некоторые молекулярные формулы могут получиться довольно длинными и сложными. Давайте посмотрим на молекулу сахара:
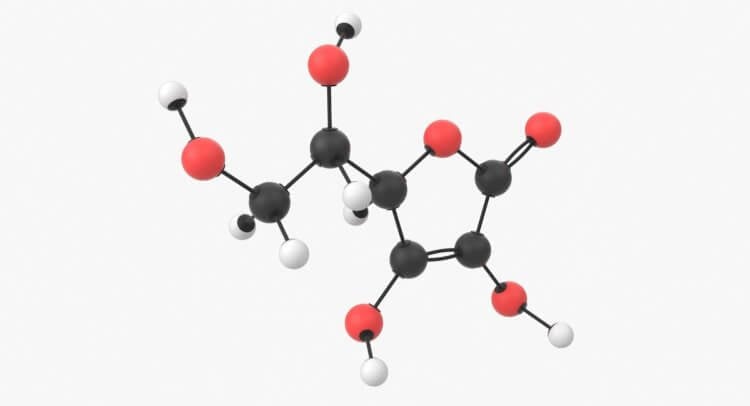
Чтобы она получилась, нужны определенные атомы в определенном количестве. Но молекулы могут быть гораздо больше. Одна молекула витамина С состоит из 20 атомов (6 атомов углерода, 8 атомов водорода и 6 атомов кислорода – C6H8O6). Если взять эти 20 атомов витамина С и смешать, соединяя их вместе в другом порядке, то получится совершенно другая молекула, которая не только выглядит по-другому, но и действует иначе.
Молекула витамина С выглядит так
Некоторые молекулы, особенно некоторые белки, содержат сотни или даже тысячи атомов, которые соединяются вместе в цепи, которые могут достигать значительной длины. Жидкости, содержащие такие молекулы, иногда ведут себя странно. Например, жидкость может продолжать вытекать из колбы, из которой была вылита некоторая ее часть, даже после того, как колба будет возвращена в вертикальное положение.
Факты о молекулах
Чтобы всегда быть в курсе последних научных открытий, подписывайтесь на наш новостной канал в Telegram
Химические связи
Молекулы и соединения удерживаются вместе силами, называемыми химическими связями. Существует четыре типа химических связей, которые удерживают большинство соединений вместе: ковалентные связи, ионные связи, водородные и металлические, однако в качестве основных выделяют ковалентные и ионные, так как они связаны с электронами. Как известно, электроны вращаются вокруг атомов в оболочках. Эти оболочки хотят быть «полными» электронов. Когда они не заполнены, то будут пытаться соединиться с другими атомами, чтобы получить нужное количество электронов и заполнить их оболочки.
Ковалентные связи делят электроны между атомами. Это происходит, когда получается, что атомы делятся своими электронами, чтобы заполнить свои внешние оболочки. В свою очередь ионные связи образуются, когда один электрон передается другому. Это происходит, когда один атом отдает электрон другому, чтобы сформировать баланс и, следовательно, молекулу или соединение.
Еще больше увлекательных статей о том, как ученые дробят реальность на атомы, читайте на нашем канале в Яндекс.Дзен. Там выходят статьи, которых нет на сайте!
Знания о свойствах и строении молекул легли в основу современной науки и нашего понимания Вселенной
Немаловажным также является тот факт, что молекулы всегда находятся в движении. В твердых телах и жидкостях они находятся очень близко друг к другу, а их движение можно сравнить с быстрой вибрацией. В жидкостях молекулы могут свободно перемещаться между собой, как бы скользя. В газе плотность молекул обычно меньше, чем в жидкости или твердом теле того же химического соединения, а потому молекулы движутся даже более свободно, чем в жидкости. Для конкретного соединения в данном состоянии (твердом, жидком или газообразном) скорость молекулярного движения возрастает с увеличением абсолютной температуры.