Болит старый шов после операции что делать
Боли после операции
Автор, редактор и медицинский эксперт – Мураева Юлия Юрьевна.
Количество просмотров: 66 247
Дата последнего обновления: 16.11.2021 г.
Среднее время прочтения: 9 минут
Почему возникают послеоперационные боли
Как уменьшить послеоперациооную боль
К задачам послеоперационного обезболивания специалисты относят 4 :
Группы препаратов, которые используются как обезболивающие после операции:
Они действуют непосредственно на причину развития повышенной чувствительности, а именно – на выработку простагландинов и других биологически активных веществ, участвующих в воспалительном процессе. Есть методики, которые предлагают использовать НПВС еще за 20-30 минут до разреза, что позволяет снизить интенсивность боли в области послеоперационных швов. 4
Для каждого пациента комплексная схема обезболивания подбирается индивидуально. Во внимание принимаются такие факторы, как возраст, пол, объем хирургического вмешательства, сопутствующая патология, психические особенности, чувствительность к боли и ее наличие до операции.
Сколько длится послеоперационная боль
Для формирования хронической послеоперационной боли, в том числе рубцов, предрасполагающими факторами являются 6 :
Профилактика развития хронического болевого синдрома проводится в несколько этапов:
Современная комплексная (мультимодальная) тактика обезболивания включает использование комбинации нестероидных противовоспалительных средств, местных анестетиков, анальгетиков центрального действия и препаратов, действующих на уровне проводимости нервных импульсов. Она должна применяться на протяжении всего периода существования зоны поврежденных тканей до окончательного заживления.
Информация в данной статье носит справочный характер и не заменяет профессиональной консультации врача. Для постановки диагноза и назначения лечения обратитесь к квалифицированному специалисту.
Литература:
боль после операции
Боль в области шва и другие виды боли
Почему не проходит боль после операции? Как снять боль после операции? Каковы причины боли после операции? – в данной статье мы поможем найти ответы на эти и подобные вопросы, а именно – расскажем об эффективном и безопасном методе лечения боли после операции, о причинах и симптомах этого заболевания, а также о наиболее популярных мифах, связанных с ним.
что такое боль после операции
Боль после операции – это мучительные или неприятные ощущения у пациента, перенёсшего операцию. Боли ощущаются не только в области шва или смежных с ней, но и в отдаленных областях.
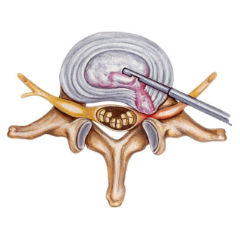
Характер болей зависит от того, по поводу какого заболевания была проведена операция. Чаще всего такие боли развиваются после операций по удалению грыжи межпозвонкового диска, паховой грыжи, желчного пузыря, протезирования суставов, гинекологических операций, а также после кесарева сечения, травм и ожогов.
причины боли после операции
Боли после операции по удалению грыжи межпозвонкового диска имеют особые проявления: боль в пояснице может исчезнуть, но появиться спустя некоторое время; может начать неметь стопа, усиливаться боль в ноге, появиться покалывание всей ноги и ощущение «ползания мурашек», зачастую на ногу больно опираться. Относительное облегчение наступает лишь в постели в определенном положении (на боку, лежа на животе и т.д.).
Боли после других видов операций схожи в своих проявлениях: боль и скованность при движении, мышечные спазмы, ноющая боль в области шва.
Причинами развития боли после операции по удалению грыжи межпозвонкового диска как в ближайшем, так и в отдаленных послеоперационных периодах, являются:
После других операции боли возникают по следующим причинам:
развенчиваем мифы о боли после операции
На сегодняшний день существует ряд заблуждений о лечении боли после операции, порождаемых в основном отсутствием у человека, столкнувшегося с данной проблемой, объективной информации по поводу предлагаемой терапии. Постараемся внести ясность в этом вопросе и развенчать наиболее популярные мифы.
Что такое рубцы? Причины возникновения, диагностику и методы лечения разберем в статье доктора Силкиной Кристины Александровны, пластического хирурга со стажем в 10 лет.
Определение болезни. Причины заболевания
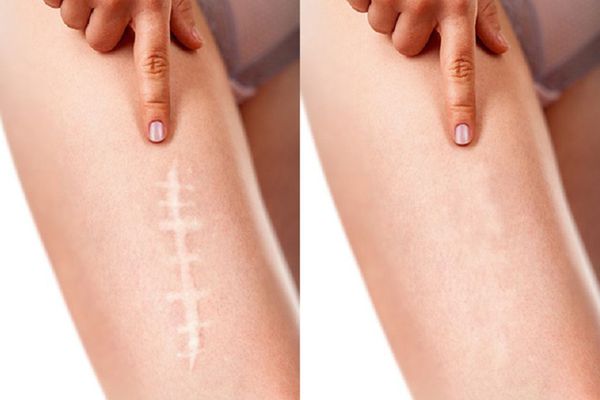
Практически у каждого человека на Земле есть рубцы: после операций, падений, оспы, ветрянки, у женщин иногда появляются растяжки (стрии), которые являются ничем иным, как атрофическими рубцами.
На заживление раны и, соответственно, на качество рубца влияют местные и общие факторы. Местные факторы:
Общие факторы, которые плохо поддаются контролю:
Симптомы рубцов
Симптомы рубцов отличаются в зависимости от типа рубца.
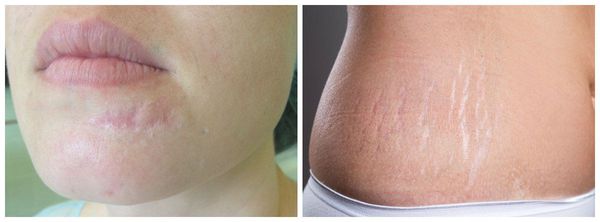
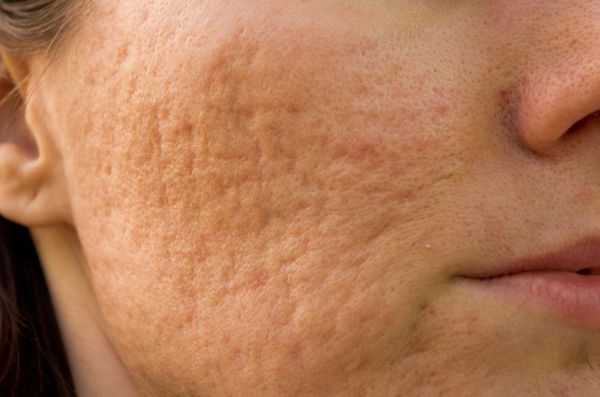
К атрофическим рубцам относятся растяжки, или стрии, постакне, а также последствия ветрянки и оспы. Такие рубцы расположены ниже уровня кожи, они как бы провалены. Формируются из-за замедления формирования новых коллагеновых и эластиновых волокон.
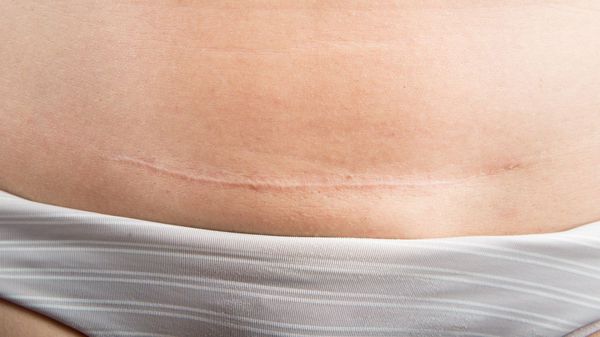
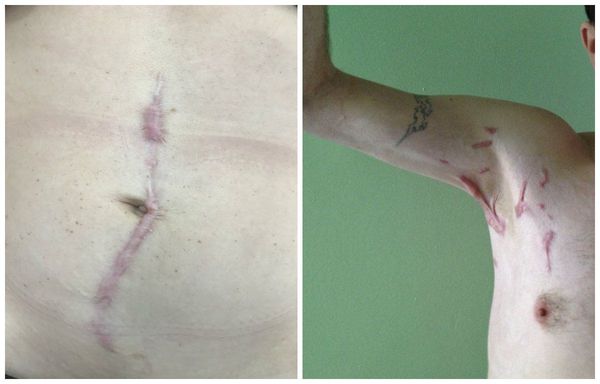
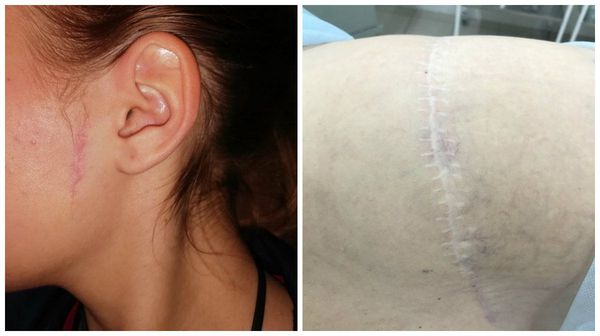
Нормотрофические рубцы. Это практически все рубцы после оперативных вмешательств, если они расположены по линиям натяжения кожи. Такие рубцы находятся на одном уровне с кожей, могут быть более или менее заметны. Иногда имеют шовные знаки или пигментацию, иногда это совсем тонкие царапины. Такие рубцы не доставляют боли и беспокойства.
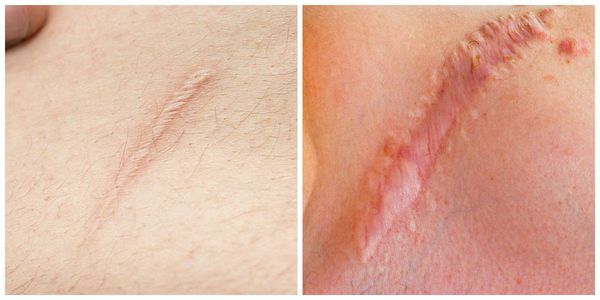
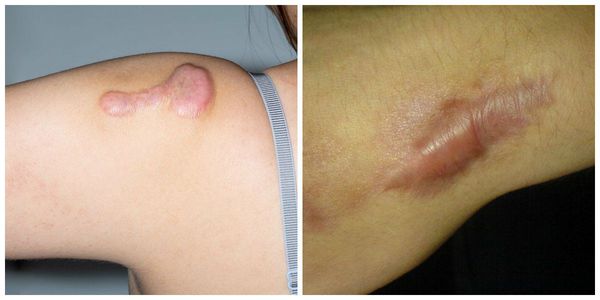
Гипертрофические рубцы в основном формируются при пересечении линий натяжения кожи, они красноватые, бугристые, возвышаются над поверхностью кожи, доставляют дискомфорт и эстетически беспокоят пациента. Иногда у пациента с детства есть склонность к гипертрофическому рубцеванию, иногда это следствие гормональных изменений. Например, у детей с 12 до 16 лет перестраивается работа организма и травма кожи может привести к образованию гипертрофического или келоидного рубца. Классический пример такого рубца:
Излюбленным местом локализации являются мочки ушей и декольте. Здесь мельчайший прокол может вызвать такое бурное разрастание рубца, которое вовлечёт всю мочку. Такие рубцы ярко-розовые, иногда красноватые, зудят (особенно ночью), вызывают крайне неприятные ощущения, значительно возвышаются над поверхностью кожи.
Образование келоидных рубцов может быть генетически детерминировано, в этом случае пациент знает, что с детства у него развиваются келоиды. Причиной может быть огромное количество самых разнообразных мелких генетических дефектов, влияющих на любой из процессов течения раневого процесса: от количества и качества цитокинов до фактора некроза опухолей и количественного соотношения коллагена в коже. Кроме того, келоидные рубцы могут возникнуть при гормональной перестройке, например у подростков, беременных, иногда у женщин в климактерическом периоде, иногда у мужчин при активных занятиях спортом. Но бывает, что установить точную причину сложно: иногда даже обычные прыщи после воспаления перерастают в зудящие рубцы.
Патогенез рубцов
Российские авторы выделяют три основных типа заживления ран:
Заживление раны не зависит от её длины, а зависит от того, какой характер у травмы, была ли рана ушита и в какой срок была проведена хирургическая обработка. Например, в эстетической хирургии есть операция – бодилифтинг, которая совмещает обширную по травме абдоминопластику и иссечение тканей боков и спины. Рана получается циркулярной по всему телу, но адекватно ушитая она заживает первичным натяжением с образованием нормотрофического рубца.
Ведутся исследования такого интересного факта, что у плода при фетальной (внутриутробной) хирургии не образуются рубцы. Связано ли это с особым строением клеток у плода или большим количеством стволовых клеток, пока сказать нельзя, но исследования в этом направлении крайне интересны.
При прочих равных условиях качество рубцов определяется генетически и/или гормональными изменениями. Кроме того, крайне важно, как человек получил травму: резаные раны заживают более гладко, размозжённые или рубленные заживают с худшим результатом. Также имеет значение, есть ли дефект тканей, например, многие операционные раны тоже становятся некрасивыми рубцами, если был иссечён участок кожи и рана находится под натяжением.
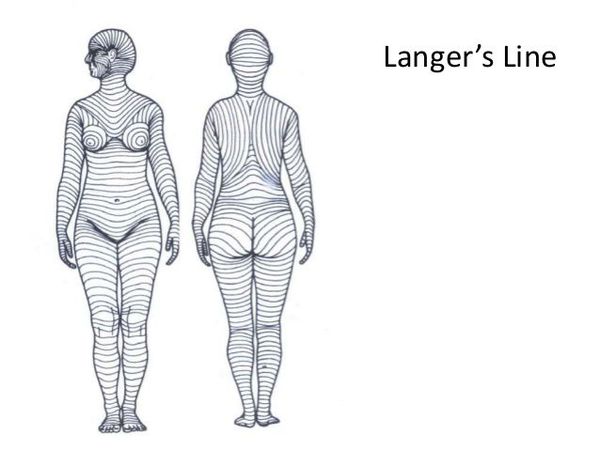
Линии натяжения — линии Лангера — это направление расположения в коже коллагеновых волокон, оно совпадает с формированием мимических морщинок и складок кожи. Волокна достаточно длинные, в коже они расположены пучками. Если кожа повреждается вдоль пучков, то рана получается узкой, линейной и заживает достаточно хорошо. Но если коллагеновые пучки пересекаются, кожа сокращается, рана зияет и заживление идёт хуже, а значит и качество рубца будет хуже.
Классификация и стадии развития рубцов
Как уже было отмечено, все рубцы делятся на нормотрофические, атрофические, гипертрофические и келоидные. Чтобы понять, как улучшить качество конкретного рубца (т. е. сделать его менее заметным, так как полностью избавиться от рубца невозможно), нужно понимать механизмы раневого процесса. А зная его, мы можем влиять на патогенез, заставляя процесс течь по нашему сценарию.
Стадии созревания рубца:
Эти стадии характерны для острой раны, в случае хронических ран (трофических язв, тяжёлых ран, которые не заживают дольше шести недель) процесс заживления будет отличаться в связи с иным течением биохимических процессов в ране.
Известна ещё одна классификация, которая определяет соотношение клеточных элементов и волокон в рубце. В ней выделяют три стадии:
Осложнения рубцов
Рубцы неблагоприятного качества заметны на видимых частях лица и тела. Как правило, такие рубцы изменяют функцию окружающих тканей, например, вызывают рубцовую контрактуру (стяжение тканей), выворот век, угла рта, из-за рубцов бывает невозможно согнуть или разогнуть пальцы и т. д. Иногда рубцы болят сами, а иногда в рубце спаян подлежащий нерв и это может выражаться болью или онемением кожи. Келоидные рубцы разрастаются и вызывают мучительный зуд. Нарушение рельефа кожи и контурные деформации часто развиваются после акне и гнойных воспалений.
Диагностика рубцов
Существование рубца на коже может констатировать любой нормально видящий человек. Рубцы внутренних органов и тканей сложнее поддаются диагностике, но в этой статье мы их не рассматриваем — они требуют отдельного обсуждения.
В диагностике заживления и формирования рубца редко требуются дополнительные методы исследования, кроме самых простых: осмотра и пальпации. Тщательный сбор жалоб и анамнеза — один из самых верных способов диагностики. Иногда используются УЗИ и МРТ для определения качества подлежащих тканей. Для оценки мягких тканей целесообразно выполнение МРТ. Оно считается более безопасным, его применяют детям и даже беременным женщинам. Однако при наличии металлоконструкций в организме пациента выполнение МРТ ограничено.
Лечение рубцов
Лечение уже сформированных рубцов должно основываться на типе рубца и его возрасте. Лечение может быть этапным (а значит длительным) и комплексным. В клиниках, где проводится комплексное лечение пациентов по эстетическим показаниям обычно разработаны протоколы реабилитации и лечения разных видов рубцов, поэтому пациент после эстетической операции начинает работать с косметологом практически с первого дня после травмы.
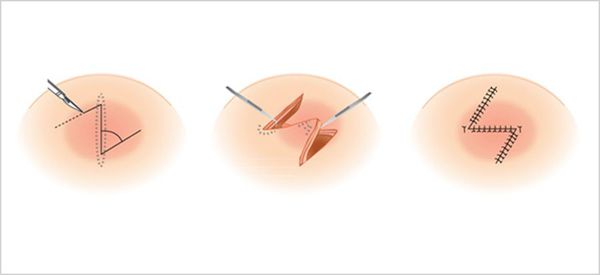
Возможно хирургическое и консервативное лечение. Хирургическое заключается в иссечение рубца, треугольной или другом виде пластики. Иногда достаточно выполнить пластику по Лимбергу. Метод основан на выкраивании и взаимном встречном перемещении двух смежных лоскутов треугольной формы, состоящих из кожи и подкожной жировой клетчатки. В этом случае нужно расположить линии рубца в большем соответствии с линиями натяжения кожи, чтобы перевести рубец из гипертрофического в длинный, но нормотрофический, не доставляющий беспокойства.
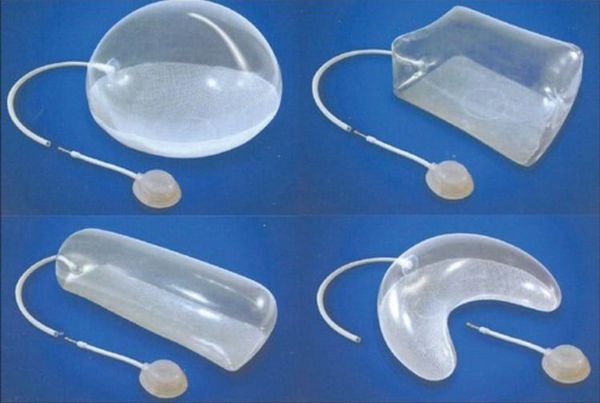
Обширные рубцы можно с успехом лечить методом экспандерной дермотензии, когда под рядом лежащий участок кожи укладывается экспандер. Экспандер представляет собой полый внутри силиконовый баллон, приспособленный к постепенному (в течение нескольких недель) введению в него физиологического раствора. Это приводит к постепенной дермотензии (растяжению) кожного покрова, который в дальнейшем используется для кожной пластики. Таким способом за несколько месяцев можно получить большое количество кожи, идентичной по цвету и текстуре (например, для закрытия волосистой части головы).
Также интересны методы лечения с помощью веропамиловой мази, ацемина, втирания витамина Е, применения препаратов цитокинов. Эти методы целесообразно развивать, так как они могут быть эффективны и полезны в выявлении процессов, происходящих в ране. Но на практике их бывает сложно применить ввиду длительности, трудозатратности или дороговизны лечения.
Атрофические рубцы лечатся долго, сложно и могут не давать выраженного эстетического результата. Используют пилинги, лазерное лечение, инъекции коллагена и гиалуроновой кислоты, а также дармабразию — сошлифовывание поверхности эпидермиса. Если при дермабразии действовать очень грубо, то она может привести к образованию новых рубцов. К хирургическим методам относится иссечение участка кожи с растяжками (ведь чаще всего это живот с множеством стрий).
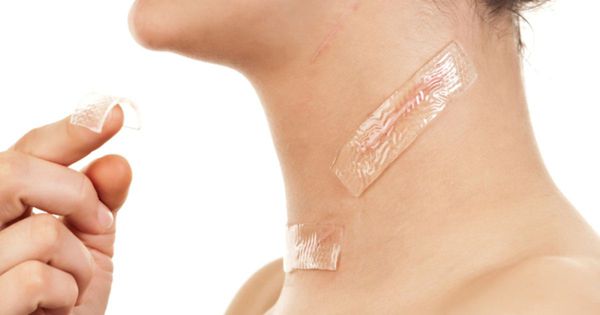
На нормотрофические рубцы можно достаточно эффективно воздействовать терапевтическими методами для улучшения качества, например, мазать силиконовыми гелями, иммоферазой. Эти средства ускорят созревание рубца и быстрее превратят его из красного в белый. Кроме того, через месяц после травмы можно обкалывать рубец собственной плазмой крови или «Сферогелем», что поможет сделать рубец максимально размытым. Если рубец белее окружающей кожи, с большим успехом применяют его татуаж.
Гипертрофические рубцы хорошо поддаются лечению с помощью инъекций гормональных препаратов, использования гормональных мазей, аппликаций силиконового геля, например «Кело-кот» или «Дерматикс». Действие этих препаратов основано на окклюзионном эффекте (блокируется испарение влаги), увлажнении рубца и уменьшении синтеза коллагена. Инъекции кортикостероидов помогают добиться быстрого улучшения состояния гипертрофического или келоидного рубца. Порой на практике для превращения гипертрофического рубца в нормотрофический необходимы 1-2 процедуры инъекции. Келоидный рубец уже после первой процедуры перестаёт зудеть, что значительно облегчает состояние пациента. Принцип действия кортикостероидов основан на мощном противовоспалительном эффекте, угнетении деления фибробластов и повышении активности собственной коллагеназы.
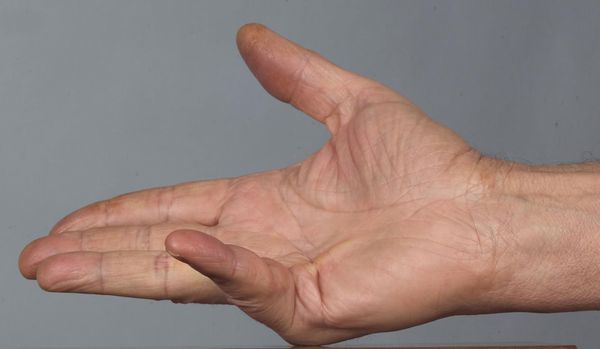
Инъекциями ферментных препаратов типа гиалуронидазы, лонгидазы лечат не только рубцы кожи, но и глубокие рубцовые деформации типа контрактуры Дюпюитрена. Это рубцовое перерождение ладонных сухожилий, при котором пальцы согнуты к ладони и их полное разгибание невозможно.
Улучшит состояние гипертрофического рубца не только инъекция, но и фонофорез с этими ферментными препаратами, что повышает доступность лечения. Хирургическое лечение заключается в треугольной пластике рубца — выполняется переориентирование линии рубца, чтобы его направление совпадало с линиями натяжения кожи.
Способов лечения келоидных рубцов очень много, это говорит о том, что на 100 % действенного метода не существует. Значительно улучшает качество рубца и снимает зуд инъекция гормонов, например «Кеналога». Прессотерапия в исследованиях даёт достаточно хорошие результаты. Это терапия постоянным давлением, например, с помощью эластической давящей повязки. Осуществлять её можно с помощью компрессионного белья или силиконовых пластин. Экспериментально выявлено, что давление в 25 мм рт. ст. на каждый сантиметр кожи сдавливает сосуды, ограничивает их рост и размягчает рубец, вплоть до полного его сглаживания. Силиконовые пластины высушивают поверхность рубца, гасят патологическое воспаление в рубце и тоже значительно облегчают состояние пациента.
Как и с гипертрофическими рубцами, хорошего результата можно ожидать от местного применения ферментных препаратов («Ферменкол») или их инъекций в ткань рубца. Не рекомендуется проводить первичное иссечение келоидного рубца. Иначе на месте иссечённой ткани в ответ на воспаление разрастётся рубец ещё больших размеров. Если у человека имеется такое состояние гомеостаза, при котором в ответ на травму формируется келоидный рубец, логично предположить, что удаляя существующий келоид врач нанесёт новую травму больше предыдущей, а значит практически со 100 % вероятностью рубец тоже станет келоидным и вовлечет в процесс какое-то количество здоровой кожи. Этот вид рубцов нуждается во внимательном отношении, спешки в лечении быть не должно.
Прогноз. Профилактика
Чем рубцы моложе, тем легче на них воздействовать консервативными методами. Зрелым рубец становится через год, после этого изменить качество рубца без хирургического воздействия уже очень сложно.
Послеоперационное обезболивание. Часть 4. Современные средства обеспечения послеоперационной анальгезии
Основными задачами применения анальгетических средств в послеоперационном периоде являются: устранение страдания, причиняемого болью, создание психологического комфорта и повышение качества жизни пациентов в послеоперационном периоде; ускорение послеоперационной функциональной реабилитации; снижение частоты послеоперационных осложнений; сокращение сроков госпитализации и стоимости лечения.
Нужно отметить, что в настоящее время в большинстве развитых стран неадекватное послеоперационное обезболивание рассматривается как нарушение прав человека и осуществляется в соответствии с принятыми национальными и международными стандартами. В нашей стране во многих клиниках внедрена формулярная система использования лечебных препаратов тех или иных групп, целесообразность применения которых подтверждена данными доказательной медицины, а также обусловлена потребностями и особенностями конкретного лечебного учреждения. Многие авторы полагают, что все хирургические подразделения, а также отделения анестезиологии, реанимации и интенсивной терапии должны иметь в своем арсенале только те анальгетики и анестетики, эффективность и безопасность назначения которых подтверждена доказательствами I (систематизированные обзоры и метаанализы) и II (рандомизированные контролируемые исследования с определенными результатами) уровня (табл. 1).
Таблица 1. Препараты, применение которых для послеоперационного обезболивания обосновано данными доказательной медицины (Acute Pain Management: Scientific Evidence, 2-nd edition, 2005).
Группа
Препараты
Дозы, путь введения
Неопиоидные анальгетики, НПВП
Диклофенак
Кетопрофен (Кетонал ®)
Кеторолак (Кеторол ®)
75 мг (150 мг суточная), в/м
50 мг (200 мг), в/м
30 мг (90 мг), в/м
Неопиоидные анальгетики, прочие
1 г (4 г), в/в инфузия в течение 15 минут
Опиоидные анальгетики, сильные
5-10 мг (50 мг), в/в, в/м
20 мг (160 мг), в/в, в/м
Опиоидные анальгетики, слабые
100 мг (400 мг), в/в, в/м
Лидокаин 2%
Бупивакаин (Маркаин®) 0, 25%, 0, 5%
Ропивакаин (Наропин®0, 2%, 0, 75%, 1%
(800 мг суточная) *
(400 мг суточная) *
(670 мг суточная) *
*инфильтрация краев раны, интраплевральное введение, продленная блокада периферических нервов и сплетений, продленная эпидуральная анальгезия.
Мировой опыт послеоперационного обезболивания позволяет выделить следующие основные современные тенденции в борьбе с ПБС:
— широкое применение неопиоидных анальгетиков – нестероидных противовоспалительных препаратов (НПВП) и парацетамола; в различных европейских клиниках частота назначения данных препаратов в качестве базиса послеоперационного обезболивания составляет от 45 до 99%;
— ограничение использования опиоидных анальгетиков, особенно внутримышечного варианта их введения, что обусловлено низкой эффективностью и значительным количеством побочных эффектов данной методики;
— мультимодальный характер послеоперационного обезболивания, т. е. одновременное назначение нескольких препаратов или методов обезболивания, способных воздействовать на различные механизмы формирования болевого синдрома.
Длительность проведения послеоперационного обезболивания является достаточно вариабельной величиной и зависит как от интенсивности болевой афферентации и, следовательно, от травматичности хирургического вмешателсьтва, так и от индивидуальной толерантности пациента к боли. Необходимость целенаправленного купирования ПБС возникает, как правило, в течение первых 4 суток послеоперационного периода (табл. 2).
Таблица 2. Потребность в обезболивании после различных по объему операций.
Хирургическое вмешательство
Продолжительность обезболивания, часы
Вмешательства на верхнем этаже брюшной полости и диафрагме
Вмешательства на нижнем этаже брюшной полости
Операции на тазобедренном суставе
Операции на конечностях
Лапароскопические операции среднего объема
Таблица 3. Методы и средства послеоперационного обезболивания.
1. Традиционное введение опиоидов: внутримышечные инъекции по требованию.
2. Опиоидные препараты агонисты/антагонисты:
а) парентеральное введение опиоидов: внутривенно болюсно, длительная внутривенная инфузия, контролируемая пациентом анальгезия.
б) непарентеральное введение опиоидов: щечное/подъязычное, пероральное, трансдермальное, назальное, ингаляционное, внутрисуставное
3. Неопиоидные анальгетики с системным введением:
а) нестероидные противоспалительные препараты
б) ацетаминофен (парацетамол)
4. Методы регионарной анестезии:
а) эпидуральное введение опиоидов;
б) нестероидные противовоспалительные препараты;
5. Нефармакологические методы:
6. Сочетанное использование представленных методов
Ниже приводятся основные используемые в современной хирургической клинике средства и методы обезболивания с позиций баланса их эффективности и безопасности.
Опиоидные анальгетики.
Данная группа лекарственных препаратов десятилетиями считалась средством выбора для купирования ПБС. Однако в настоящее время опиоидные анальгетики отнюдь не являются «золотым стандартом» в лечени пациентов с острой болью. Тем не менее, по оценкам целого ряда отечественных и зарубежных специалистов, эффективность обезболивания при традиционном назначении опиоидов в качестве монотерапии не превышает 25-30%. Однако постепенное отчуждение от чрезмерной приверженности опиоидам в послеоперационном периоде связана не столько с их недостаточной эффективностью, сколько с целым рядом серьезных побочных эффектов, возникающих при их использовании (табл. 4).
С точки зрения фармакодинамики опиоидные анальгетики являются агонистами или антагонистами различных видов опиоидных рецепторов ЦНС (мю-, дельта-, каппа-). Препараты опиоидной группы активируют эндогенную антиноцицептивную систему (центральная анальгезия), однако не влияют на периферические и сегментарные неопиоидные механизмы ноцицепции и не предотвращают центральную сенситизацию и гиперальгезию. Попытки увеличения эффективности обезболивания и снижения частоты побочных эффектов опиоидных анальгетиков основаны на варьировании способов их введения (в том числе и у одного пациента): внутривенный, внутримышечный, эпидуральный, трансдермальный, сублингвальный, ректальный. Наиболее распространенным, но при этом наиболее небезопасным и наименее эффективным способом введения опиоидов является внутримышечная инъекция. Данная методика наиболее часто приводит к неадекватному обезболиванию – более 60% пациентов отмечают неудовлетворительное качество послеоперационной анальгезии. Причины этого кроются в том, что всем пациентам вводятся фиксированные дозы через стандартные временные интервалы, без учета индивидуальной вариабельности фармакокинетики; часто инъекции опиоидов производятся с большими перерывами, то есть тогда, когда болевой синдром уже выражен и его купирование по определению становится малоэффективным. Именно при внутримышечном введении опиоидов наиболее часто развивается депрессия дыхания, связанная, возможно, с кумуляцией препарата.
Таблица 4. Опиоидные анальгетики при купировании послеоперационного болевого синдрома.
Препарат
Дозировка и пути введения
Относительная анальгетическая активность
Побочные эффекты
Возможны выраженные угнетение дыхания, тошнота, рвота, высокая степень привыкания и максимальный наркогенный потенциал
Угнетение дыхания, тошнота, рвота, высокая степень привыкания и наркогенный потенциал
Угнетение дыхания, тошнота, рвота, наличие привыкания и наркогенного потенциала
Необходимо отметить еще один важный аспект, ограничивающий применение опиоидных анальгетиков в отечественной клинической практике. Использование опиоидных анальгетиков для послеоперационного обезболивания в Российской Федерации строго регламентировано существующими приказами руководящих органов здравоозранения. Например, приказом № 257 Департамента здравоохранения г. Москвы от 2004 г. определяется, в частности, норматив потребления опиоидных препаратов в ампулах на 1 койку различных отделений хирургического профиля в год. Назначение опиоидного препарата как в хирургическом отделении, так и в отделении интенсивной терапии в большинстве ЛПУ сопровождается колоссальным количеством формальных сложностей, что нередко приводит к отказу медперсонала от использования ланных препаратов даже при необходимости назначения опиоидов. По тем же причинам самый современный метод применения опиоидов – контролируемая пациентом аналгезия, в наибольшей степени ориентированная на индивидуальные потребности пациента в обезболивании – в России не получила широкого распространения.
Неопиоидные анальгетики.
Термином «неопиоидные анальгетики» обозначается группа различных по химическому строению, фармакодинамике и, соответственно, механизму обезболивания лекарственных препаратов, применяемых для купирования ПБС с парентеральным, реже пероральным путем введения. Препараты данной группы, используемые как в моноварианте, так и в качестве средства адъювантной терапии, обладают различными анальгетическим потенциалом и совокупностью побочных эффектов (табл. 5).
Таблица 5. Неопиоидные анальгетики для купирования послеоперационной боли.
Класс
Препараты
Особенности терапии
Побочные эффекты
Антагонисты NMDA-рецепторов
Применяется как адъювант при введении опиоидов.
Малые дозы кетамина характеризуются опиоидсберегающим эффектом, повышением качества обезболивания
При использовании в малых дозах – не выражены. Сохраняют побочные эффекты опиоидов.
Антиконвульсанты
Используется как адъювантный препарат в комплексной терапии острой послеоперационной боли. Снижает потребность как в опиоидных, так и внеопиоидных анальгетиках.
Головокружение, сонливость, периферические отеки.
Ингибиторы протеаз
Ингибирование синтеза медиаторов боли на этапе трансдукции, используются как средство адъювантной терапии ПБС
Нерушения в системе гемостаза (гипокоагуляция) – послеоперационные кровотечения.
Центральные α-адреномиметики
Воздействие на трансмиссию и модуляцию боли. Адъювант при опиоидной анальгезии.
Гипотензия, брадикардия, психические нарушения.
Бензодиазепины
Комбинированная терапия с применением феназепама и тизанидина снижает выраженность фантомных болей.
Сонливость, головокружение, психические расстройства
Из приведенных данных становится очевидным, что перечисленные в таблице неопиоидные анальгетики используются лишь как возможное дополнение к базисной терапии опиоидами, использование данных препаратов для купирования ПБС в моноварианте не практикуется.
Формально к группе неопиоидных анальгетиков относятся также нестероидные противовоспалительные препараты (НПВП) и ацетаминофен (парацетамол). Однако вследствие значительной востребованности в современной хирургической клинике данные препараты рассматриваются сейчас как отдельные подклассы средств для купирования ПБС.
Парацетамол.
Несмотря на то, что ацетаминофен (парацетамол) имеет более чем полувековую историю применения в качестве анальгетика и антипиретика, точный механизм действия этого препарата до сих пор не известен. Предполагается наличие центрального механизма действия парацетамола, включающего: подавление активности циклооксигеназы 2 типа в ЦНС, с чем связана профилактика развития вторичной гиперальгезии; подавление активности циклооксигеназы 3 типа, существование которой предполагается и которая, видимо, обладает селективной чувствительностью к парацетамолу; усиление активности нисходящих тормозных серотонинергических путей на этапе модуляции боли.
Потенциально опасным побочным свойством парацетамола является гепатотоксическое и нефротоксическое действие, которое может проявляться при превышении дозы 4 г/сут, особенно при наличии у пациента исходного нарушения функции печени и почек. Ограничениями к применению парацетамола являются: печеночно-клеточная недостаточность с лабораторными проявлениями (повышение уровня трансаминаз), почечная недостаточность, алкоголизм, алиментарная недостаточность, дегидратация.
Местные анестетики.
Важнейшей задачей мультимодальной анальгезии является прерывание афферентного потока ноцицептивных стимулов от периферических болевых рецепторов в органах и тканях к сегментарным структурам ЦНС (задним рогам спинного мозга). Эта задача может быть успешно решена при помощи различных методов регионарной и местной анальгезии. Важную роль в расширении применения методов региональной анальгезии сыграло появление современных местных анестетиков (бупивокаин, ропивокаин), а также детальная отработка методики регионарных блокад.
Эпидуральная анальгезия занимает ключевую позицию среди всех регионарных методов послеоперационного обезболивания. В ходе данной процедуры в эпидуральное пространство на уровне грудного или поясничного отделов позвоночника устанавливается катетер, через который болюсно или путем непрерывной инфузии вводятся местные анестетики. Эпидуральная анестезия является как средством обеспечения анальгезии в ходе операции (в том числе и в моноварианте), так и средством купирования ПБС. Многочисленными исследованиями была доказана принципиально более высокая эффективность продленной послеоперационной эпидуральной анальгезии по сравнению с системным введением опиоидных анальгетиков. Как указывалось выше сами опиоидные анальгетики также могут быть использованы для проведения эпидуральной анестезии. Известно, что эпидуральное введение местных анестетиков и опиоидов достоверно превышает анальгетический эффект использования данных препаратов в отдельности. Тем не менее само по себе эпидуральное введение опиоидов чревато возникновением серьезных побочных эффектов от угнетения дыхания до выраженного кожного зуда. На сегодняшний день принято считать, что преимущества эпидурального введения опиоидных анальгетиков в абдоминальной хирургии не перевешивают риска осложнений самой методики эпидуральной анестезии по сравнению с парентеральным назначением аналогичных препаратов.
Помимо собственно анальгетического эффекта позитивное влияние прослеоперационной продленной эпидуральной анальгезии заключается в прерывании нисходящих симпатических эфферентных импульсов, следствием чего являются улучшение висцерального кровотока (активизация репаративных процессов в зоне вмешательства), повышение активности парасимпатической нервной системы (разрешение пареза пищеварительной трубки).
С точки зрения доказательной медицины (Acute Pain Management: Scientific Evidence, 2-nd edition, 2005) преимущества продленной эпидуралной анальгезии включают: более высокое качество обезболивания в сравнении с парентеральным введением опиоидов; улучшение показателей газообмена и снижение частоты послеоперационных легочных осложнений по сравнению с опиоидной анальгезией; ускорение восстановления функции желудочно-кишечного тракта после абдоминальных операций и снижение частоты местных осложнений.
Тем не менее и у эпидуральной анестезии есть ряд существенных ограничений. Сама по себе эпидуральная анестезия является сложной инвазивной процедурой, потенциально опасной в плане развития как местных (инфекционный процесс, повреждение нервных корешков, сосудов паутинной оболочки, твердой мозговой оболочки), так и системных осложнений (депрессия дыхания, кардиотоксические эффекты, артериальная гипотензия). В этой связи проведение эпидуральной анестезии требует наличия специальных навыков у врача-анестезиолога и постоянного мониторинга состояния пациента в отделении интенсивной терапии, реже – в хирургическом отделении.
В последние годы все большую популярность получает методика длительной инфузии местных анестетиков в полость операционной раны. В ходе ряда исследований было показано, что длительная инфузия местных анестетиков в течение 24-48 часов через катетер, установленный в ране, способна повысить качество обезболивания и снизить потребность в опиоидных анальгетиках. Работами отечественных авторов показано, что пролонгированная местная анестезия операционной раны за счет резорбции местного анестетика и присутствия его в плазме в низких концентрациях способна оказывать системный противовоспалительный эффект. Как и в случае эпидуральной анальгезии эффект местных анестетиков при этом обусловлен блокадой не только ноцицептивных путей, но и симпатической иннервации. Говоря о применении пролонгированной местной анестезии операционной раны, следует заметить, что данная методика в настоящее время находится на стадии клинической апробации и ее широкое внедрение изначально ограничивают очевидный риск экзогенного инфицирования раны и реальная опасность системных токсических эффектов местных анестетиков (артериальная гипотензия, аритмии, угнетение дыхания) вследствие их резорбции тканями.
Мультимодальная периоперационная анальгезия.
Из приведенных выше характеристик и, что важнее, недостатков средств и методов купирования ПБС следует очевидное заключение о том, что в настоящее время не существует идеального анальгетика или метода лечения острой послеоперационной боли. Однако приблизиться к решению проблемы адекватности послеоперационного обезболивания вполне возможно, реализуя в клинике концепцию мультимодальной периоперационной анальгезии, предусматривающей одновременное назначение двух и более анальгетиков и/или методов обезболивания, обладающих различными механизмами действия и позволяющих достичь адекватной анальгезии при минимизации побочных эффектов до, во время и после хирургического вмешательства (см. рис. ).
Таблица 6. Варианты схем мультимодальной периоперационной анальгезии, ориентированных на травматичность хирургических вмешательств.