Болит бабочка на ноге что делать
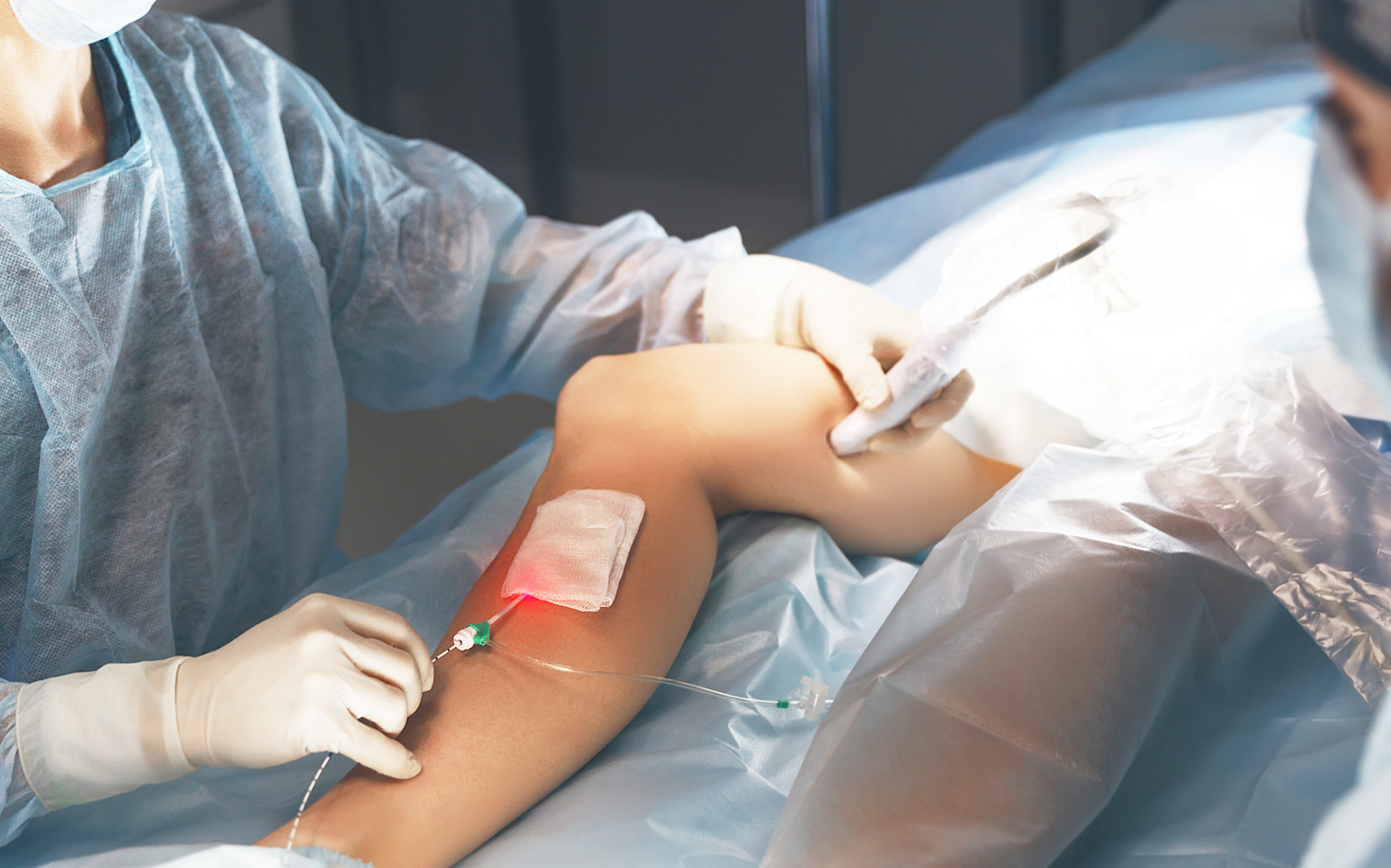
Боли в области икры: дифференциальный диагноз
В статье представлен дифференциальный диагноз болевого синдрома в области икроножной мышцы, развивающегося вследствие хронической венозной недостаточности, острой венозной недостаточности, хронической артериальной недостаточности, острой артериальной недостаточности, остеохондроза, остеоартроза, полинейропатии, дерматомиозита, миозита, фибромиалгии, травмы мышц.
Боли в области икроножной мышцы (икры) – универсальный симптом, который может наблюдаться при большом количестве заболеваний.
Основной мышечный массив задней поверхности голени (икра) образован двумя мышцами – располагающейся поверхностно икроножной мышцей и более глубоко расположенной камбаловидной мышцей. Сухожилия этих мышц объединяются вместе и прикрепляются к пяточной кости, образуя т.н. ахиллово сухожилие. Мышцы икры обеспечивают движение в голеностопном суставе (сгибание и разгибание), что необходимо для обеспечения ходьбы, удержания равновесия тела в вертикальном положении и амортизации при движениях.
Артериальное кровоснабжение икроножной мышцы происходит из собственных артерий, берущих начало из подколенной артерии. Венозный отток осуществляется по сопровождающим артерии венам, которые в толще мышцы образуют широкие выстланные эндотелием полости – суральные синусы. Иннервируются вышеуказанные мышцы из большеберцового нерва (L3-4).
Хроническая венозная недостаточность.
На сегодняшний день в генезе боли при хронических заболеваниях вен выделяют три основных компонента: дистензионный, ишемический и воспалительный.
Дистензионный компонент возникает вследствие перерастяжения венозной стенки избытком крови при нарушении механизмов ее оттока. Подобные нарушения могут быть следствием дисфункции мышечно-венозной помпы, играющей ведующую роль в обеспечении венозного оттока в вертикальном положении тела. Застой крови в венах голени может возникать в результате снижения активности мышц икры, например вследствие длительного пребывания в неподвижном вертикальном или сидячем положении, в результате поражения клапанного аппарата поверхностных (варикозная болезнь) или глубоких (посттромботический синдром) вен, что сопровождается нарушением нормального центростремительного движения крови и ее забросом в дистальные отделы при каждом мышечном сокращении (рефлюкс), а также при поражении соответствующих мышц и смежных с ними суставов. Подобные боли часто возникают после длительных статических нагрузок и легко купируют ночным отдыхом и/или путем придания конечностям возвышенного положения.
Воспалительный компонент является отражением общепринятой на сегодняшний день концепции лейкоцитарной агрессии, как ведующего компонента патогенеза хронических заболеваний вен. Суть ее заключается в том, что при уменьшении скорости венозного оттока и появлении признаков венозного стаза в венах голени происходит лейкоцитарно-эндотелиальное взаимодействие с экспрессией ссответвующих адгезивных молекул на поверхности клеток, что приводит к миграции белых кровяных телец в толщу сосудистой стенки и их дегрануляции. Освобожденные свободные радикалы кислорода, протеолитические ферменты и цитокины оказывают не только повреждающее воздействие на структурные компоненты венозной стенки, в первую очередь, коллагеновый каркас, но и активируют безмиелиновые С-ноцицепторы, отвечающие за передачу болевого импульса. Таким образом, воспалительный компонент венозной боли отражает не только застой крови в венах голени, но и процесс активного развития хронических заболеваний вен, который может в итоге привести к появлению варикозной трансформации. Присоединение воспалительного компонента делает венозную боль более стойкой и не купирующейся возвышенным положением конечности и ночным отдыхом.
Ишемический компонент связан с тяжелыми воспалительными изменениями венозной стенки с запустеванием vasa vasorum, что приводит к серьезной морфологической перестройке страдающих вен. Следует предполагать, что ишемический компонент встречается при тяжелых формах хронических заболеваний вен и может обеспечивать постоянную болезненность самих варикозных узлов.
Классические боли при венозной недостаточности носят тупой распирающий характер, усиливаются после длительного пребывания в положении стоя или сидя, уменьшаются или полностью проходят после ночного отдыха или придания конечности возвышенного положения. Часто боли сопровождаются преходящим отеком мягких тканей в области нижней трети голени и судорогами икроножной мышцы в ночные часы.
Острая венозная недостаточность – тромбоз глубоких вен голени. В результате внезапного затруднения венозного оттока из нижних конечностей и развития острого венозного полнокровия могут наблюдаться весьма интенсивные постоянные распирающие боли в области икроножной мышцы, незначительно уменьшающиеся при придании конечности возвышенного положения, сопровождающиеся увеличением объема мышцы и ее уплотнением, цианозом кожи и усилением подкожного сосудистого рисунка. Степень выраженности симптомов будет зависеть от локализации тромбоза – чем больше вен окажется вовлечено в процесс, тем более острыми будут проявления. При изолированном тромбозе суральных синусов могут наблюдаться умеренной интенсивности четко локализованные боли, усиливающиеся при подошвенном сгибании голеностопного сустава и при надавливании в место проекции синуса на кожу.
Хроническая артериальная недостаточность развивается вследствие окклюзии артерий атеросклеротическим или аутоиммунно-воспалительным процессом. В подобных случаях мышцы испытывают кислородное голодание, переходят на анаэробный путь метаболизма, что приводит к накоплению кислых продуктов, раздражающих болевые рецепторы. При артериальной недостаточности боли в икроножных мышцах наблюдаются при ходьбе и вынуждают человека остановиться (синдром «перемежающейся хромоты»), на начальных стадиях процесса в покое боли не беспокоят. Боли сопровождаются похолоданием конечностей, зябкостью, кожа становится бледной, шелушащейся, легко ранимой, теряется волосяной покров. При прогрессировании заболевания мышцы и подкожная клетчатка истончаются.
Острая артериальная недостаточность – внезапная закупорка артерий вследствие ее тромбоза или эмболии приводит к остро возникшей ишемии конечности. В этом случае боли в икроножной мышцы будут наблюдаться в покое, носить интенсивные характер, сопровождаться нарушениями чувствительности и двигательной функции вплоть до развития паралича и мышечной контрактуры.
Остеохондроз поясничного отдела позвоночника (корешковый синдром) – вторая по частоте причина появления болей в области икроножных мышц. В основе лежит сдавление корешка спинномозгового нерва в месте его выхода из позвоночного канала. В результате возникают проецированные боли в том месте, куда идут нервные волокна – в том числе в область икры. При этом боли могут быть связаны как с компрессией нервов и генерацией в них болевых импульсов, так и с тоническим мышечным сокращением и последующим развитием фиброзно-дистрофических изменений в мышечной ткани. При корешковом синдроме боли связаны с определенными движениями и изменением положения тела (например, наклон туловища вперед, в стороны, сгибание конечности в тазобедренном суставе). Как правило, боли усиливаются при длительном пребывании в провоцирующем положении и уменьшаются после разминки, лечебной физкультуры, массажа, тепловых воздействий. При мышечно-тоническом синдроме возможно обнаружить участки повышенного тонуса в воде плотных болезненных очагов в тоще мышцы. Со временем мышца может диффузно уплотняться в связи с развитием в ней фиброзных изменений. Впоследствии в связи с нарушением вегетативной иннервации может происходить присоединение застойного (вазодилатация) или ишемического (вазоконстрикция) компонента болевого синдрома.
Периферическая полинейропатия может быть осложнением сахарного диабета, следствием токсического воздействия на организм этилового спирта и пр. Для диабетической полинейропатии характерно сочетание ночных или утренних болей в покое, локализующихся в дистальных отделах нижних конечностей, с ощущениями ползанья мурашек, жжения, онемения, мышечной слабостью и снижением кожной и (в первую очередь) вибрационной чувствительности. При этом боли могут носить очень интенсивный характер. Поражение вегетативных нервов может приводить к трофическим нарушениям и присоединению сосудистого компонента болевого синдрома.
Неврит большеберцового нерва характеризуется болями приступообразного характера, возникающими по ходу нервных волокон. При этом в промежутках между приступами боль полностью отсутствует.
Патология коленных суставов – в первую очередь, остеоартроз – характеризуется болями в околосуставной области при нагрузке. Боли локализуются преимущественно в области передней и внутренней поверхностей коленного сустава, усиливаются при длительном пребывании в вертикальном положении тела, при долгой ходьбе. Особенно характерно усиление болей при подъеме и особенно спуске по лестнице. На начальных стадиях заболевания в покое боли полностью проходят (при этом не требуется придавать конечности возвышенное положение). При развитии активного воспаления могут появляться боли в начале движения и утренняя скованность в суставах. В процессе развития заболевания возможно присоединение мышечно-тонического компонента болевого синдрома, при котором икроножная мышца находится в постоянном напряжении и становится плотной и болезненной при пальпации. При скоплении выпота в полости сустава могут образовываться ограниченные ее скопления в заворотах суставной капсулы – кисты Беккера, которые могут усугублять болевой синдром, сдавливать нервы и вены с развитием нейропатического и сосудистого компонента.
Дерматомиозит, полимиозит – аутоиммунное воспаление мышечной ткани, характеризующиеся постоянными тупыми упорными болями, усиливающимися при движениях в голеностопном суставе, в сочетании с мышечной слабостью и симптомами интоксикации. Мышцы становятся отечными, болезненными при пальпации, со временем может наблюдаться их уплотнение, тяжистость, узловатость, фиброз, образование кальцинатов вплоть до полной атрофии. При аутоиммунных заболеваниях, как правило, выявляются поражения других органов и систем, в первую очередь кожи: эритема и отек периорбитальной области, шелушащаяся эритема пальцев и кистей, покраснение околоногтевых валиков, очаги гиперпигментации-депигментации кожи – при дерматомиозите; отек-индурация-атрофия кожи при склеродермии, эритема на лице, поражение почек, сердца при волчанке и пр. Между тем, поражение икроножных мышц при аутоиммунных миозитах встречается нечасто.
Миозиты также могут быть проявлением онкологических, паразитарных заболеваний (трихинеллез, токсоплазмоз, цистицеркоз) или являться осложнением простуды, травмы или перенапряжения икроножной мышцы.
Перенапряжение, растяжение, разрыв мышцы могут сопровождаться выраженными интенсивными болями в зоне повреждения, резко усиливающимися при попытках движений. Могут присоединяться явления воспаления (миозит).
Статья добавлена 24 июля 2014 г.
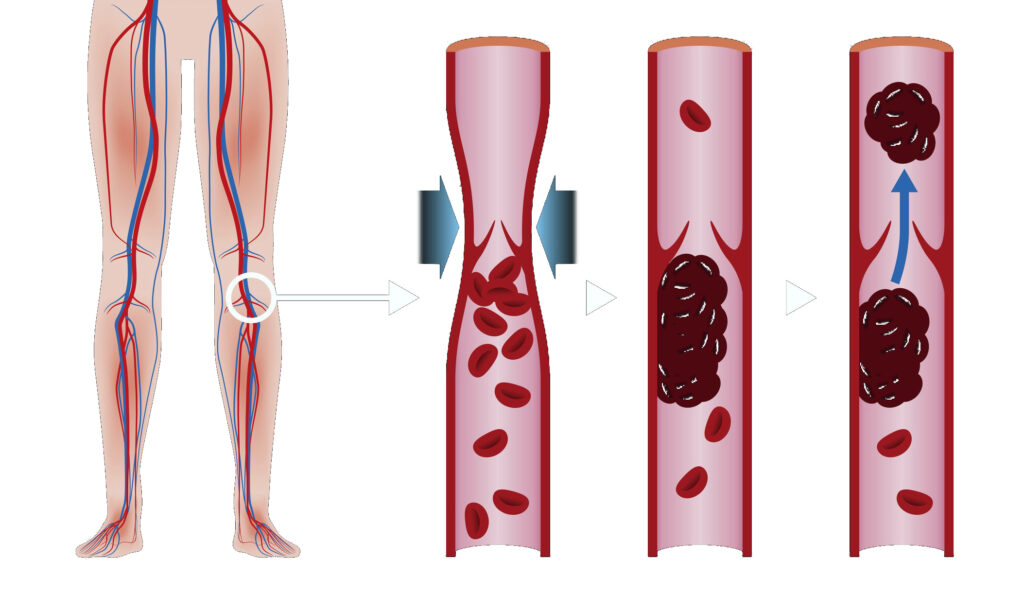
Признаки и симптомы тромбоза глубоких вен
Тромбоз глубоких вен (ТГВ) возникает, когда сгусток крови (тромб) образуется в одной или нескольких глубоких венах вашего тела, обычно в ногах. Тромбоз глубоких вен может вызвать боль в ногах или их отек, но может протекать бессимптомно.
ТГВ может быть связан с заболеваниями, которые влияют на процесс свертывания крови. Тромб в ногах также может образоваться, если вы не двигаетесь долгое время, например, после операции или несчастного случая. Но и ходьба на экстремально большие расстояния может приводить к образованию тромбов.
Тромбоз глубоких вен – серьезное заболевание, потому что сгустки крови в ваших венах могут перемещаться по кровотоку и застревать в легких, блокируя кровоток (тромбоэмболия легочной артерии). Однако тромбоэмболия легочной артерии может возникать без признаков ТГВ.
Когда ТГВ и тромбоэмболия легочной артерии возникают одновременно, это называется венозной тромбоэмболией (ВТЭ).
Симптомы
Признаки и симптомы ТГВ:
Тромбоз глубоких вен может протекать без заметных симптомов.
Когда обратиться к врачу
Если у вас признаки или симптомы ТГВ, обратитесь к врачу.
При появлении признаков или симптомов тромбоэмболии легочной артерии (ТЭЛА) – опасного для жизни осложнения тромбоза глубоких вен – обратитесь за неотложной медицинской помощью.
Предупреждающие признаки и симптомы тромбоэмболии легочной артерии включают:
Подозреваете тромбоз глубоких вен? Обратитесь к профессионалам.
Причины
Все, что препятствует нормальному течению или свертыванию крови, может вызвать образование тромбов.
Основными причинами ТГВ являются: повреждение вены в результате хирургического вмешательства или травмы, а также в связи воспалением от инфекции или травмы.
Факторы риска
Многие факторы могут увеличить риск развития ТГВ, которые включают:
Осложнения
Осложнения ТГВ могут включать:
Профилактика
Меры по предотвращению тромбоза глубоких вен включают следующее:
Воспаление мышц стопы — тендовагинит: признаки, диагностика, лечение
Тендовагинит стопы — воспалительный процесс, происходящий во внутренней части сухожилий голеностопного сустава. Подразделяется на первичный, вторичный, стерильный, инфекционный, аллопатический и пронизывающий. В большинстве случаев проблема решается массажем и ЛФК.
ДОСТУПНЫЕ ЦЕНЫ НА КУРС ЛЕЧЕНИЯ
Мягко, приятно, нас не боятся дети
ДОСТУПНЫЕ ЦЕНЫ НА КУРС ЛЕЧЕНИЯ
Мягко, приятно, нас не боятся дети
Абсцесс внутреннего эпидермиса соединительных волокон стопы, которые находятся со стороны подошвы и оборотной стороны ступни, называется тендовагинитом стопы. В медицинской практике встречаются два вида: основной и второстепенный. Основной случается как у спортсменов-любителей, так и у первоклассных спортсменов, в то время как второстепенный наблюдается вследствие возникновения сепсиса (от нагноения или заразной болезни) либо же от уже имеющихся болезней ревматического характера.
Этиология
Основным поводом для возникновения воспалительного процесса в первичном его виде является небольшой травматизм соединительных тканей стоп, который может появиться от чрезмерных нагрузок или же в результате анатомических особенностей организма. Под первую категорию тендовагинита подводят людей с искривлением ног, врожденным или приобретенным, танцоров, актеров балета, грузчиков, а также занимающихся конькобежным и лыжным спортом.
Обостренные воспаления могут возникнуть в результате контакта с инфицированным участком или же через кровь (гнойный артрит стопы, гнойно-некротический процесс). Тендовагинит стопы может развиться до хронического, если у человека есть какое-либо из инфекционных заболеваний — гонорея, грипп, бруцеллез или сифилис.
В случае если человек страдает болезнями ревматического характера (спондилит анкилозирующий, ревматоидный артрит, синдром Фиссенже—Леруа), продолжительность тендовагинита стопы определяется моментальной интоксикацией организма.
Типология
Исходя из причин возникновения тендовагинита, современная медицина определила несколько подвидов:
Помимо этой классификации, заболевание также разделяется по формам развития воспалительных процессов внутри соединительных тканей:
Признаки возникновения тендовагинита
Существует вероятность перехода острой формы воспаления в хроническую. А это означает, что человека будут мучить болезненные ощущения и нормально ходить он не сможет. Поверхностный осмотр показывает растяжимые новообразования, в некоторых случаях прощупываются небольшие уплотнения, так называемые «рисовые тела». Они же часто обнаруживаются при туберкулезном тендовагините.
Как диагностировать
Если существуют подозрения насчет заболевания, необходимо проконсультироваться у врача-ортопеда. Он может дать направление к хирургу или же ревматологу.
Для постановки диагноза врачу требуется выполнить некоторые манипуляции:
Назначаемое лечение тендовагинита
В случае если болезнь только проявила себя, пациенту рекомендуется покой. В остром периоде пациенту противопоказано ходить, конечность фиксируется с помощью эластичного бинта или лонгеты и находится в подвешенном состоянии. Также назначают иммуностимулирующие и противобактериальные препараты.
Когда причины острого воспаления устранены, назначаются процедуры с УФ-лучами, электрофорез с гидрокортизоном, лечебная физкультура, ультразвук.
При выявлении острого гнойного воспаления проводят срочную операцию, вскрывают сухожилие, дренируют его. При это назначают антибиотики, подавляющие возбудителя инфекции.
Если воспаление началось на фоне заболевания туберкулезом или сифилисом, то первостепенной задачей становится избавление от основного заражения с помощью противотуберкулезных лекарств (стрептомицин, ПАСК).
В случае хронического протекания болезни используют всё те же методы, что указаны выше — ЛФК, массаж, электрофорез с лидазой, парафин. Также пациенту прописывают нестероидные противовоспалительные средства и инъекции в место поражения. В крайних случаях применяют рентген в качестве терапии.
Невропатия седалищного нерва. Синдром грушевидной мышцы
Болезни периферической нервной системы — одна из наиболее частых причин инвалидизации пациентов трудоспособного возраста. В структуре этих болезней преобладающее место занимают болевые синдромы (Н. Н. Яхно, 2003; Г. Р. Табеева, 2004).
Болезни периферической нервной системы — одна из наиболее частых причин инвалидизации пациентов трудоспособного возраста. В структуре этих болезней преобладающее место занимают болевые синдромы (Н. Н. Яхно, 2003; Г. Р. Табеева, 2004). Причины развития невропатического болевого синдрома могут быть различными: сахарный диабет, паранеопластические процессы, ВИЧ, герпес, хронический алкоголизм (А. М. Вейн, 1997; И. А. Строков, А. Н. Баринов, 2002).
При поражении периферической нервной системы выделяют два типа боли: дизестезическую и трункальную. Поверхностная дизестезическая боль обычно наблюдается у пациентов с преимущественным поражением малых нервных волокон. Трункальная боль встречается при компрессии спинно-мозговых корешков и туннельных невропатиях.
У пациентов с этим видом болевого синдрома невозможно выбрать оптимальную стратегию лечения без идентификации патофизиологических механизмов. Поэтому при определении тактики терапии необходимо учитывать локализацию, характер и выраженность клинических проявлений болевого синдрома.
Под компрессионно-ишемической (туннельной) невропатией понимают невоспалительные поражения периферического нерва, развивающиеся под влиянием компрессии или ишемических воздействий.
В зоне компрессии соответствующего нерва нередко находят болезненные уплотнения или утолщения тканей, приводящие к существенному сужению костно-связочно-мышечных влагалищ, через которые проходят нервно-сосудистые стволы.
В настоящее время известно множество вариантов компрессионных невропатий. Их клиническая картина складывается из трех синдромов: вертебрального (в случаях участия одноименного фактора), неврального периферического, рефлекторно-миотонического или дистрофического. Вертебральный синдром на любом этапе обострения, и даже в стадии ремиссии, может вызывать изменения в стенках «туннеля». Миодистрофический очаг, выступающий в качестве реализующего звена, обусловливает невропатию на фоне своего клинического пика. Неврологическая картина компрессионных невропатий складывается из симптомов поражения той или иной выраженности в соответствующих мио- и дерматомах. Диагноз компрессионных невропатий ставится при наличии болей и парестезий в зоне иннервации данного нерва, двигательных и чувствительных расстройств, а также болезненности в зоне рецепторов соответствующего канала и вибрационного симптома Тинеля. При затруднениях в диагностике используются электронейромиографические исследования: определяются поражения периферического нейрона, соответствующего данному нерву, и степень уменьшения скорости проведения импульса по нерву дистальнее места его компрессии. Синдром грушевидной мышцы — самая распространенная туннельная невропатия. Патологическое напряжение грушевидной мышцы при компрессии корешка L5 или S1, а также при неудачных инъекциях лекарственных веществ ведет к сдавливанию седалищного нерва (или его ветвей при высоком отхождении) и сопровождающих его сосудов в подгрушевидном пространстве.
Для выбора правильной стратегии терапии необходимо четко знать основные клинические симптомы поражения той или иной области. Основные клинические проявления поражения нервов крестцового сплетения:
Наиболее трудны в плане диагностики поражения в области таза или выше ягодичной складки — из-за наличия соматической или гинекологической патологии у пациентов. Клинические симптомы поражения в области таза или выше ягодичной складки складываются из следующих вариантов нарушений двигательных и чувствительных функций.
Поражение седалищного нерва на уровне подгрушевидного отверстия может наблюдаться в двух вариантах:
Для компрессии седалищного нерва и идущих рядом сосудов характерны следующие клинические проявления: ощущение постоянной тяжести в ноге, боли тупого, «мозжащего» характера. При кашле и чихании усиления болей не наблюдается. Отсутствует атрофия ягодичной мускулатуры. Зона гипестезии не распространяется выше коленного сустава.
Синдром грушевидной мышцы встречается не менее чем у 50% больных дискогенным пояснично-крестцовым радикулитом. Если пациенту поставлен данный диагноз, предположение о наличии синдрома грушевидной мышцы может возникнуть при наличии упорных болей по ходу седалищного нерва, не уменьшающихся при медикаментозном лечении. Гораздо труднее определить наличие данного синдрома, если имеются только болевые ощущения в области ягодицы, носящие ограниченный характер и связанные с определенными положениями (перемещениями) таза или при ходьбе. Часто синдром грушевидной мышцы регистрируется в гинекологической практике. При синдроме грушевидной мышцы возможно:
Клиническая картина синдрома грушевидной мышцы состоит из локальных симптомов и симптомов сдавления седалищного нерва. К локальным относится ноющая, тянущая, «мозжащая» боль в ягодице, крестцово-подвздошном и тазобедренном суставах, которая усиливается при ходьбе, в положение стоя, при приведении бедра, а также в полуприседе на корточках; несколько стихает в положении лежа и сидя с разведенными ногами. При хорошем расслаблении большой ягодичной мышцы под ней прощупывается плотная и болезненная при натяжении (симптом Бонне–Бобровниковой) грушевидная мышца. При перкуссии в точке грушевидной мышцы появляется боль на задней поверхности ноги (симптом Виленкина). Клиническая картина сдавления сосудов и седалищного нерва в подгрушевидном пространстве складывается из топографо-анатомических «взаимоотношений» его больше- и малоберцовых ветвей с окружающими структурами. Боли при компрессии седалищного нерва носят тупой, «мозжащий» характер с выраженной вегетативной окраской (ощущения зябкости, жжения, одеревенения), с иррадиацией по всей ноге или преимущественно по зоне иннервации больше- и малоберцовых нервов. Провоцирующими факторами являются тепло, перемена погоды, стрессовые ситуации. Иногда снижаются ахиллов рефлекс, поверхностная чувствительность. При преимущественном вовлечении волокон, из которых формируется большеберцовый нерв, боль локализуется в задней группе мышц голени. В них появляются боли при ходьбе, при пробе Ласега. Пальпаторно отмечается болезненность в камбаловидной и икроножной мышцах. У некоторых больных сдавление нижней ягодичной артерии и сосудов самого седалищного нерва сопровождается резким переходящим спазмом сосудов ноги, приводящим к перемежающейся хромоте. Пациент вынужден при ходьбе останавливаться, садиться или ложиться. Кожа ноги при этом бледнеет. После отдыха больной может продолжать ходьбу, но вскоре у него повторяется тот же приступ. Таким образом, кроме перемежающейся хромоты при облитерирующем эндартериите существует также подгрушевидная перемежающаяся хромота. Важным диагностическим тестом является инфильтрация грушевидной мышцы новокаином с оценкой возникающих при этом положительных сдвигов. Рефлекторное напряжение в мышце и нейротрофические процессы в ней вызваны, как правило, раздражением не пятого поясничного, а первого крестцового корешка. Распознать указанный синдром помогают определенные мануальные тесты.
Поскольку болезненное натяжение грушевидной мышцы чаще всего связано с ирритацией первого крестцового корешка, целесообразно поочередно проводить новокаиновую блокаду этого корешка и новокаинизацию грушевидной мышцы. Значительное уменьшение или исчезновение болей по ходу седалищного нерва может рассматриваться как динамический тест, показывающий, что боли обусловлены компрессионным воздействием спазмированной мышцы.
Поражения седалищного нерва
Поражения седалищного нерва ниже выхода из малого таза (на уровне бедра и ниже) или в полости малого таза характеризуют следующие признаки.
Кроме вышеописанных клинических симптомов, вероятно развитие вазомоторных и трофических расстройств: повышение кожной температуры на пораженной ноге. Голень и стопа становятся холодными и цианотичными. Часто на подошве обнаруживаются гипергидроз или ангидроз, гипотрихоз, гиперкератоз. Появляются изменения цвета и формы ногтей, трофические нарушения на пятке, тыльной поверхности пальцев, наружном крае стопы, регистрируется снижение силы, а также атрофия мышц стопы и голени. Больной не может встать на носки или на пятки. Для определения начального поражения седалищного нерва можно использовать тест на определение силы полусухожильной, полуперепончатой и двуглавой мышц бедра.
Синдром седалищного нерва (ишемически-компрессионная невропатия седалищного нерва). В зависимости от уровня (высоты) поражения возможны разные варианты синдрома седалищного нерва.
Очень высокий уровень поражения (в тазу или выше ягодичной складки) характеризуется: параличом стопы и пальцев, утратой ахиллова и подошвенного рефлексов; анестезией (гипестезией) почти всей голени и стопы, кроме зоны n. sapheni; выпадением функций двуглавой мышцы бедра, полусухожильной, полуперепончатой мышц; гипестезией (анестезией) по задненаружной поверхности бедра; невозможностью вращения бедра кнаружи; наличием положительных симптомов натяжения (Ласега, Бонне); наличием вазомоторных и трофических расстройств (гипер- или гипотрихоз, гипо- или гипергидроз, изменение роста ногтей, образование трофических язв в области пятки и наружного края стопы).
Поражение на уровне подгрушевидного отверстия складывается из двух групп симптомов — поражения самой грушевидной мышцы и седалищного нерва. К первой группе симптомов относят: болезненность при пальпации верхневнутренней части большого вертела бедра (места прикрепления грушевидной мышцы к капсуле этого сочленения); болезненность при пальпации в нижней части крестцово-подвздошного сочленения; симптом Бонне (пассивное приведение бедра с ротацией его внутрь, вызывающее боли в ягодичной области, реже — в зоне иннервации седалищного нерва); болезненность при пальпации ягодицы в точке выхода седалищного нерва из-под грушевидной мышцы. Ко второй группе относятся симптомы сдавления седалищного нерва и сосудов. Болезненные ощущения при компрессии седалищного нерва характеризуются чувством постоянной тяжести в ноге, тупым, «мозжащим» характером боли, отсутствием усиления болей при кашле и чихании, а также атрофии ягодичной мускулатуры, зона гипестезии не поднимается выше коленного сустава.
Поражение на уровне бедра (ниже выхода из малого таза) и до уровня деления на мало- и большеберцовый нервы характеризуется: нарушением сгибания ноги в коленном суставе; специфической походкой; отсутствием активных движений в стопе и пальцах, которые умеренно отвисают; присоединяющейся через 2–3 нед атрофией парализованных мышц, часто маскирующей пастозность ноги; гипестезией (анестезией) по задненаружной поверхности голени, тылу стопы, подошве и пальцам; нарушением суставно-мышечной чувствительности в голеностопном суставе и в межфаланговых суставах пальцев стопы; отсутствием вибрационной чувствительности на наружной лодыжке; болезненностью по ходу седалищного нерва — в точках Валле и Гара; положительным симптомом Ласега; исчезновением ахиллова и подошвенного рефлексов.
Синдром неполного повреждения седалищного нерва характеризуется наличием болей каузалгического характера («жгучие» боли, усиливаются при опускании ноги, провоцируются легким прикосновением); резкими вазомоторными и трофическими расстройствами (первые 2–3 нед кожная температура на больной ноге на 3–5 °С выше («горячая кожа»), чем на здоровой, в дальнейшем голень и стопа становятся холодными и цианотичными). Часто на подошвенной поверхности обнаруживаются гипергидроз или ангидроз, гипотрихоз, гиперкератоз, изменения формы, цвета и темпа роста ногтей. Иногда возникают трофические язвы на пятке, наружном крае стопы, тыльной поверхности пальцев. На рентгенограммах выявляются остеопороз и декальцификация костей стопы.
Синдром начального поражения седалищного нерва может быть диагностирован путем использования тестов для определения силы полусухожильной и полуперепончатых мышц.
Синдром грушевидного, внутреннего запирательного нервов и нерва квадратной мышцы бедра. Полный синдром грушевидного, внутреннего запирательного нервов и нерва квадратной мышцы бедра характеризуется нарушением ротации бедра кнаружи. Синдром частичного поражения указанной группы нервов может диагностироваться на основании использования тестов для определения объема движений и силы обследуемого.
Синдром верхнего ягодичного нерва. Полный синдром верхнего ягодичного нерва характеризуется нарушением отведения бедра с частичным нарушением ротации последнего, затруднением поддержания вертикального положения туловища. При двустороннем параличе указанных мышц больному трудно стоять (стоит неустойчиво) и ходить (появляется так называемая «утиная походка» с переваливанием с бока на бок). Синдром частичного поражения верхнего ягодичного нерва можно выявить с помощью теста, определяющего силу ягодичных мышц. По степени снижения силы по сравнению со здоровой стороной делается заключение о частичном поражении верхнего ягодичного нерва.
Синдром нижнего ягодичного нерва. Полный синдром нижнего ягодичного нерва характеризуется затруднением разгибания ноги в тазобедренном суставе, а в положении стоя — затруднением выпрямления наклоненного таза (таз наклонен вперед, при этом в поясничном отделе позвоночника наблюдается компенсаторный лордоз). Затруднены вставание из положения сидя, подъем по лестнице, бег, прыжки. При длительном поражении указанного нерва отмечаются гипотония и гипотрофия ягодичных мышц. Синдром частичного поражения нижнего ягодичного нерва может диагностироваться с помощью теста для определения силы большой ягодичной мышцы. По степени снижения объема и силы указанного движения (и в сравнении их со здоровой стороной) делают заключение о степени нарушения функций нижнего ягодичного нерва.
Лечение
Терапия невропатии седалищного нерва требует знания этиологических и патогенетических механизмов развития заболевания. Тактика лечения зависит от тяжести и скорости прогрессирования заболевания. Патогенетическая терапия должна быть направлена на устранение патологического процесса и его отдаленных последствий. В остальных случаях лечение должно быть симптоматическим. Его цель — продление стойкой ремиссии и повышение качества жизни пациентов. Основным критерием оптимального лечебного воздействия на пациента является сочетание медикаментозных и немедикаментозных методов. Среди последних лидируют физиотерапевтические методики и методы постизометрической релаксации.
При нарушении функции мышц тазового пояса и нижней конечности рекомендуется использовать одну из техник мануальной терапии — постизометрическое расслабление (ПИР), т. е. растяжение спазмированной мышцы до ее физиологической длины после максимального напряжения. Основными принципами медикаментозной терапии поражений периферической нервной системы являются раннее начало лечения, снятие болевого синдрома, сочетание патогенетической и симптоматической терапии. Патогенетическая терапия направлена в первую очередь на борьбу с оксидантным стрессом, воздействием на микроциркуляторное русло, улучшение кровоснабжения пораженного участка, снятие признаков нейрогенного воспаления. С этой целью применяются антиоксидантные, вазоактивные и нестероидные противовоспалительные препараты (НПВП). Сложность медикаментозной терапии связана в большинстве случаев с запутанной анатомо-физиологической иерархией структур, вовлеченных в патологический процесс. Отчасти это обусловлено строением и функционированием структур пояснично-крестцового сплетения. В то же время базисным механизмом, лежащим в основе развития невропатии, является четкая корреляция между компрессией и ишемией нерва и развитием оксидантного стресса.
Оксидантный стресс — нарушение равновесия между продукцией свободных радикалов и активностью антиоксидантных систем. Развившийся дисбаланс приводит к усиленной продукции соединений (нейротрансмиттеров), выделяющихся поврежденными тканями: гистамин, серотонин, АТФ, лейкотриены, интерлейкины, простагландины, окись азота и т. д. Они приводят к развитию нейрогенного воспаления, увеличивая проницаемость сосудистой стенки, а также способствуют высвобождению тучными клетками и лейкоцитами простагландина E2, цитокинов и биогенных аминов, повышая возбудимость ноцицепторов.
В настоящее время появились клинические работы, посвященные использованию препаратов, улучшающих реологические свойства крови и эндотелийзависимые реакции стенки сосудов у пациентов с компрессионными невропатиями. Такие препараты, как производные тиоктовой кислоты (тиогамма, тиоктацид) и гинкго билоба (танакан), успешно применяются с целью уменьшения проявлений оксидантного стресса. Однако патогенетически более обосновано применение лекарственных средств, обладающих поливалентным механизмом действия (церебролизин, актовегин).
Приоритетность использования актовегина обусловлена возможностью его назначения для проведения лечебных блокад, хорошей сочетаемостью с другими лекарственными средствами. При компрессионно-ишемических невропатиях, как в острой, так и в подострой стадиях заболевания, целесообразно применение актовегина, особенно при отсутствии эффекта от других способов лечения. Назначается капельное введение 200 мг препарата в течение 5 дней, с последующим переходом на пероральное применение.
В механизмах развития заболеваний периферической нервной системы важное место занимают нарушения гемодинамики в структурах периферической нервной системы, ишемия, расстройство микроциркуляции, нарушения энергообмена в ишемизированных нейронах со снижением аэробного энергообмена, метаболизма АТФ, утилизации кислорода, глюкозы. Патологические процессы, протекающие в нервных волокнах при невропатиях, требуют коррекции вазоактивными препаратами. С целью улучшения процессов микроциркуляции и активизации процессов обмена и гликолиза у пациентов с туннельными невропатиями применяются кавинтон, галидор, трентал, инстенон.
Инстенон — комбинированный препарат нейропротекторного действия, включающий вазоактивный агент из группы пуриновых производных, влияющий на состояние восходящей ретикулярной формации и корково-подкорковые взаимоотношения, а также процессы тканевого дыхания в условиях гипоксии, физиологические механизмы ауторегуляции церебрального и системного кровотока. При невропатиях инстенон применяют внутривенно капельно 2 мл в 200 мл физиологического раствора, в течение 2 ч, 5–10 процедур на курс. Затем продолжается пероральный прием инстенона форте по 1 таблетке 3 раза в день в течение месяца. При невропатиях с симпатологическим синдромом показано применение инстенона по 2 мл внутримышечно 1 раз в сутки в течение 10 дней. При компрессионно-ишемических (туннельных) невропатиях используется аналогичная методика. Это способствует улучшению микроциркуляции и метаболизма в ишемизированном нерве. Особенно хороший эффект отмечается при сочетанном применении актовегина (капельно) и инстенона (внутримышечные инъекции или пероральное применение).
Галидор (бенциклана фумарат) — препарат, имеющий широкий спектр действия, что обусловлено блокадой фосфодиэстеразы, антисеротониновым эффектом, кальциевым антагонизмом. Галидор назначается в суточной дозе 400 мг в течение 10–14 дней.
Трентал (пентоксифиллин) применяют по 400 мг 2–3 раза в сутки внутрь или 100–300 мг внутривенно капельно в 250 мл физиологического раствора.
Назначение комбинированных препаратов, включающих большие дозы витамина В, противовоспалительных средств и гормонов, нецелесообразно.
Средствами первого ряда для снятия болевого синдрома остаются НПВП. Основной механизм действия НПВП — ингибирование циклооксигеназы (ЦОГ-1, ЦОГ-2) — ключевого фермента каскада метаболизма арахидоновой кислоты, приводящего к синтезу простагландинов, простациклинов и тромбоксанов. В связи с тем, что метаболизм ЦОГ играет главную роль в индукции боли в очаге воспаления и передаче ноцицептивной импульсации в спинной мозг, НПВП широко используются в неврологической практике. Имеются данные о том, что их принимают 300 млн пациентов (Г. Я. Шварц, 2002).
Все противовоспалительные средства оказывают собственно противовоспалительное, анальгезирующее и жаропонижающее действие, способны тормозить миграцию нейтрофилов в очаг воспаления и агрегацию тромбоцитов, а также активно связываться с белками сыворотки крови. Различия в действии НПВП носят количественный характер (Г. Я. Шварц, 2002), но именно они обусловливают выраженность терапевтического воздействия, переносимость и вероятность развития побочных эффектов у больных. Высокая гастротоксичность НПВП, коррелирующая с выраженностью их саногенетического действия, связана с неизбирательным ингибированием обеих изоформ циклооксигеназы. В связи с этим для лечения выраженных болевых синдромов, в том числе длительного, необходимы препараты, обладающие противовоспалительным и анальгезирующим действиями при минимальных гастротоксических реакциях. Наиболее известное и эффективное лекарственное средство из этой группы — ксефокам (лорноксикам).
Ксефокам — препарат с выраженным антиангинальным действием, которое достигается за счет сочетания противовоспалительного и сильного обезболивающего эффектов. Он является на сегодняшний день одним из наиболее эффективных и безопасных современных анальгетиков, что подтверждено клиническими исследованиями. Эффективность перорального применения по схеме: 1-й день — 16 и 8 мг; 2–4-й дни — 8 мг 2 раза в день, 5-й день — 8 мг/сут — при острых болях в спине достоверно доказана. Анальгетический эффект в дозе 2–16 мг 2 раза в сутки в несколько раз выше, чем у напраксена. При туннельных невропатиях рекомендуется использование препарата в дозе 16–32 мг. Курс лечения составляет не менее 5 дней при одноразовой ежедневной процедуре. Рекомендуется применение препарата ксефокам для лечения синдрома грушевидной мышцы по следующей методике: утром — внутримышечно 8 мг, вечером — 8–16 мг внутрь, в течение 5–10 дней, что позволяет добиться быстрого и точного воздействия на очаг воспаления при полном обезболивании с минимальным риском развития побочных реакций. Возможно проведение регионарных внутримышечных блокад в паравертебральную область по 8 мг на 4 мл 5% раствора глюкозы ежедневно в течение 3–8 дней. Симптоматическая терапия — метод выбора для купирования алгических проявлений. Наиболее часто для лечения туннельных невропатий используются лечебные блокады с анестетиками. Стойкий болевой синдром длительностью более 3 нед свидетельствует о хронизации процесса. Хроническая боль — сложная терапевтическая проблема, требующая индивидуального подхода.
В первую очередь необходимо исключить другие причины возникновения боли, после чего целесообразно назначение антидепрессантов.
М. В. Путилина, доктор медицинских наук, профессор
РГМУ, Москва