Болезнь лебера что это такое
Атрофия зрительного нерва Лебера
OMIM 535000
Наша команда профессионалов ответит на ваши вопросы
Наследственная оптическая нейропатия Лебера (Leber hereditary optic neuropathy, LHON), или наследственная атрофия зрительных нервов Лебера, или болезнь Лебера (не путать с амаврозом Лебера. – названия похожи, но клинические проявления различаются) –митохондриальное заболевание, манифестирующее, как правило, в возрасте 15-35 лет (однако возраст начала заболевания может варьировать от 1 до 70 лет). Леберовская атрофия зрительного нерва характеризуется острым или подострым двусторонним медленным снижением остроты центрального зрения, при этом не сопровождается болью в глазных яблоках. Глаза могут поражаться как одновременно, так и последовательно, с интервалом в несколько месяцев. Как правило, снижение зрения остается выраженным и постоянным, но описаны случаи, когда спустя несколько лет происходит спонтанное улучшение зрения, иногда значительное. На ранних стадиях заболевания часто отмечается поражение цветового зрения. В ряде семей кроме снижения остроты зрения выявляются и неврологические симптомы: тремор, атаксии, дистония, судороги, а в некоторых случаях – заболевания, не отличимые от рассеянного склероза. Характерными особенностями наследственной оптической нейропатии Лебера являются неполная пенетрантность (до 50% у мужчин и 10% у женщин) и большая частота заболевания среди мужчин (мужчины болеют в 3-5 раз чаще женщин), возможно, связанная с действием Х-сцепленного модифицирующего гена, расположенного в районе Xp21. Показано, что важное влияние на начало и развитие заболевания оказывают факторы риска – стрессы, курение, употребление алкоголя, действие токсинов, лекарств и инфекций.
Как и для других заболеваний с митохондриальным наследованием, для наследственной оптической нейропатии Лебера характерны передача по материнской линии, а также явление гетероплазмии (присутствие в клетке более одного типа митохондрий), которым в ряде случаев можно объяснить неполную пенетрантность.
Причиной развития наследственной оптической нейропатии Лебера являются мутации в митохондриальной ДНК. Выделяют 18 аллельных вариантов заболевания, связанных с миссенс-мутациями в ряде митохондриальных генов. Большинство этих мутаций являются редкими (встречаются в одной или нескольких семьях в мире), однако в 95% случаев выявляется одна из трех мажорных мутаций: m.3460G>A, m.11778G>A или m.14484T>C. Все они изменяют структуру генов, кодирующих белки первого комплекса дыхательной цепи митохондрий.
Показано, что степень тяжести заболевания и возможность восстановления зрения коррелируют с выявленными мутациями. Так, считается, что мутация m.11778G>A вызывает наиболее тяжелые формы, m.3460G>A – более легкие, а m.14484T>C дает наиболее благоприятный прогноз.
Нами разработан набор для ДНК-диагностики Атрофии зрительного нерва Лебера. Наборы предназначены для использования в диагностических лабораториях молекулярно-генетического профиля.
В Центре Молекулярной Генетики проводится диагностика основных трех мажорных мутаций m.11778G>A, m.14484T>C, m.3460G>A, а также 9 более редких первичных мутаций: m.3733G>A, m.4171C>A, m.10663T>C, m.14459G>A, m.14482C>G, m.14482C>A, m.14495A>G, m.14502T>C, m.14568C>T.
Болезнь лебера что это такое
Наследственная нейрооптикопатия Leber (Leber’s hereditary optic neuropathy, LHON) — одно из первых заболеваний, для которых была установлена этиологическая связь со специфическими дефектами мтДНКЛ. Минимальная моментальная распространенность составляет 1 на 31000 на Северо-Западе Англии, 1 на 39000 в Нидерландах и 1 на 50000 в Финляндии. Возраст дебюта заболевания обычно составляет от 15 до 35 лет, но может варьировать от одного года до 87 лет. Наследственная нейрооптикопатия Leber поражает преимущественно мужчин, что не характерно для митохондриального типа наследования.
У 25-50% мужчин и 5-10% женщин — носителей наследственной нейрооптикопатии Leber в течение жизни развивается ухудшение зрения. Отмечается двустороннее безболезненное обычно внезапное ухудшение центрального зрения. Примерно в 50% случаев наблюдается последовательное ухудшение зрения обоих глаз, поражение второго глаза развивается в течение нескольких недель или месяцев после поражения первого. В течение года неизбежно поражаются оба глаза. Зрение каждого глаза ухудшается в течение нескольких недель или месяцев, острота зрения обычно снижается до значений 20/200 или ниже. Рано развиваются тяжелые нарушения цветового зрения; при периметрии как правило выявляются центральные или центроцекальные дефекты. Аномалии глазного дна выявляются как у самих больных наследственной нейрооптикопатией Leber, так и у их здоровых родственников по материнской линии.
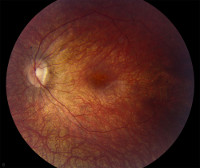
Наблюдаются гиперемия диска зрительного нерва, расширение и извитость сосудов, кровоизлияния, окружающие диск телеангиэктатические микроангиопатии или отек слоя нервных волокон (псевдозастой); эти изменения особенно выражены в острую фазу ухудшения зрения. Со временем единственной аномалией, выявляемой на глазном дне, остается атрофия зрительного нерва и дефекты слоя нервных волокон, особенно в зоне папилломакулярного пучка. Может встречаться неглаукоматозная экскавация ДЗН и сужение артерий. У большинства пациентов с наследственной нейрооптикопатией Leber ухудшение зрения является единственным проявлением болезни. В некоторых семьях у больных наблюдались сопутствующие нарушения сердечной проводимости, особенно часто — синдромы преждевременного возбуждения. У нескольких пациентов были описаны небольшие неврологические нарушения и скелетные аномалии, наподобие наблюдающихся при рассеянном склерозе.
Клиническое значение дополнительных методов исследования при наследственной нейрооптикопатии Leber ограничено. Флюоресцентная ангиография может помочь отдифференцировать изменения диска зрительного нерва при наследственной нейрооптикопатии Leber от истинного отека ДЗН. При электрокардиографии могут выявляться нарушения проводимости сердца. При оптической когерентной томографии на начальных стадиях заболевания выявляется утолщение перипапиллярного слоя нервных волокон, после чего, по мере развития атрофии зрительного нерва, наблюдается его истончение. При ухудшении зрения регистрируются ожидаемо аномальные зрительные вызванные потенциалы. При стандартной электроретинографии при стимуляции вспышкой, электроэнцефалографии, исследовании спинномозговой жидкости, КТ и МРТ головного мозга обычно не выявляется аномалий. Изредка при МРТ у больных с наследственной нейрооптикопатией Leber выявляется резкое увеличения контрастности передних отделов зрительного пути, а в поздние фазы в режиме Т2 — яркие изменения.
У нескольких пациентов с наследственной нейрооптикопатией Leber при магнитной резонансной спектроскопии с фосфором-31 были выявлены признаки нарушения митохондриального метаболизма мышц конечностей и затылочных долей. У тех же пациентов с наследственной нейрооптикопатией Leber при анализе крови выявлена недостаточность комплекса I дыхательной цепи.
Наследственная нейрооптикопатия Leber передается по материнской линии; было выяснено, что причиной заболевания являются точечные мутации митохондриальной ДНК. Три точечные мутации митохондриальной ДНК, известные как «основные мутации наследственной нейрооптикопатии Leber», вызывают примерно 90% случаев этого заболевания во всем мире. Они локализуются в нуклеотидных позициях 11778 (69% случаев), 3460 (13% случаев) и 14484 (14% случаев).
Описаны другие точечные мутации, которые чаще встречаются у больных наследственной нейрооптикопатией Leber, чем в контрольных группах, но выводы о значении этих «второстепенных» мутаций в развитии заболевания следует делать с осторожностью. Некоторые из этих мутаций и в самом деле могут являться основными мутациями, но каждая из них была обнаружена лишь в нескольких семьях по всему миру. Роль других мутаций в патогенезе заболевания остается неясной. Скрининг на предмет наследственной нейрооптикопатии Leber пациентам с ухудшением зрения должен начинаться с поиска трех основных мутаций. Отрицательные результаты анализов на основные мутации и сохраняющиеся сильные подозрения, возможно, являются показанием к исследованию на предмет наличия других связанных с наследственной нейрооптикопатией Leber мутаций митохондриальной ДНК, особенно тех, которые, как считается, вызывают заболевание в нескольких семьях. Или же, поскольку большинство этих «второстепенных» мутаций митохондриальной ДНК локализуются в кодирующих субъединицы комплекса I генах, может быть выполнено полное секвенирование комплекса I, возможно, начиная с так называемой «горячей точки» — гена ND6. Наконец, выполнимо секвенирование всего митохондриального генома, хотя этот анализ трудоемок.
Эти исследования следует выполнять только при наличии стойких подозрений, результаты должны интерпретироваться специалистом, разбирающимся в тонкостях митохондриальной генетики.
Среди пациентов с наследственной нейрооптикопатией Leber, вызванной основными мутациями, наблюдаются очень сходные клинические фенотипы. Единственным существенным различием является более благоприятный прогноз для зрения у пациентов с мутацией 14484. Почти у 70% пациентов с мутацией 14484 отмечается некоторое улучшение зрительных функций, по сравнению со всего лишь 5% пациентов с мутацией 11778. Возможно, у пациентов с мутацией 3460 шансы на восстановление зрения выше, чем при наличии мутации 11778, но для обоснованного анализа количество пациентов слишком мало. У пациентов с дебютом ухудшения зрения в возрасте младше двадцати, а особенно — младше десяти лет, прогноз для зрения гораздо более благоприятный.
Однако нельзя объяснить экспрессию заболевания только генетическими дефектами. Наличие мутации митохондриальной ДНК обязательно, но не достаточно для фенотипической экспрессии. Одним из факторов экспрессии может являться гетероплазмия (наличие одновременно мутантных и нормальных митохондриальных ДНК). В семьях с гетероплазмией у индивидов с большим количеством мутантной митохондриальной ДНК, вероятно, более высокий риск ухудшения зрения. Однако у многих пациентов со 100% мутантной мтДНК зрение так никогда и не ухудшается. Взаимодействие генетических (митохондриальных или ядерных) факторов и окружающей среды осложняет определение роли отдельных мутаций мтДНК в патогенезе заболевания. На экспрессию заболевания, вероятно, влияют и другие факторы митохондриальной или ядерной ДНК, в том числе сцепленные с Х-хромосомой, что объясняет экспрессию заболевания преимущественно у мужчин. Высказывались предположения о различных факторах среды, провоцирующих ухудшение зрения у пациентов с наследственной нейрооптикопатией Leber.
Системные заболевания, недостаточность питания, медикаменты и токсические воздействия, вызывающие нарушения выработки энергии митохондриями, могут оказаться губительными для индивидов, генетически предрасположенных к недостаточности энергопродукции митохондриями. Курение, вероятно, из-за своего пагубного воздействия на функцию митохондрий, связано с более выраженной экспрессией ухудшения зрения среди носителей основных мутаций наследственной нейрооптикопатии Leber; аналогичная связь установлена только для тяжелого алкоголизма.
Патофизиология наследственной нейрооптикопатии Leber остается неизвестной. Может иметь место аномальное окислительное фосфорилирование и недостаточная продукция АТФ, напрямую или опосредованно связанные с выработкой свободных радикалов, что приводит к необратимому повреждению ганглиозных клеток и их аксонов. Почему эти нарушения приводят к селективному повреждению зрительного нерва, остается неясным. При гистохимических исследованиях зрительного нерва животных была выявлена высокая дыхательная активность митохондрий безмиелиновых волокон преламинарной части зрительного нерва, что свидетельствует о высокой потребности в функционирующих митохондриях в этой зоне. Большой интерес представляет собой недавно открытая на модели грызунов генетическая индукция недостаточности комплекса I; при этом гистологические признаки дегенерации зрительного нерва аналогичны наблюдаемым у пациентов с наследственной нейрооптикопатией Leber. Дальнейшее развитие моделирования митохондриальных болезней на животных поможет лучше изучить патогенез митохондриальных болезней человека.
Методы лечения, применяемые при наследственной нейрооптикопатии Leber, включают в себя терапию коэнзимом Q10, идебеноном, L-карнитином, сукцинатом, дихлороацетатом, витамином К1, витамином КЗ, витамином С, тиамином, витамином В2 и витамином Е. По результатам рандомизированного контролируемого исследования применения идебенона для лечения наследственной нейрооптикопатии Leber у пациентов с ухудшением зрения в течение пяти лет при различных зрительных функциях двух глаз (т.е. тех пациентов, у которых заболевание манифестировало недавно), исход для зрения на фоне лечения может быть лучше. Однако из-за необратимых повреждений маловероятно, что при атрофии зрительного нерва какая-либо терапия будет иметь выраженный эффект. Общая рекомендация — избегать приема веществ, вызывающих нарушение митохондриальной энергопродукции, однако эффективность этих мер не доказана.
Но мы все же рекомендуем пациентам с наследственной нейрооптикопатией Leber и их родственникам по материнской линии, входящим в группу риска, избегать табакокурения, употребления содержащих цианиды продуктов, чрезмерного употребления алкоголя и внешних токсических воздействий. Симптоматическое лечение заключается в применении кардиостимуляторов у пациентов с сердечными блокадами или тяжелыми нарушениями сердечной проводимости, а также в помощи слабовидящим при тяжелом снижении зрительных функций. По мере изучения специфических генетических и биохимических аномалий, вероятно, будут разработаны новые методы лечения, направленные на замещение или создание путей обхода генетических и метаболических дефектов у больных и их находящихся в группе риска родственников. Возможно, перспективный метод генной терапии, известный под названием аллотипической экспрессии, в будущем будет играть роль при лечении наследственной нейрооптикопатии Leber и других митохондриальных болезней, а пока не следует недооценивать важность информированного генетического консультирования членов семьи при материнском типе наследования.
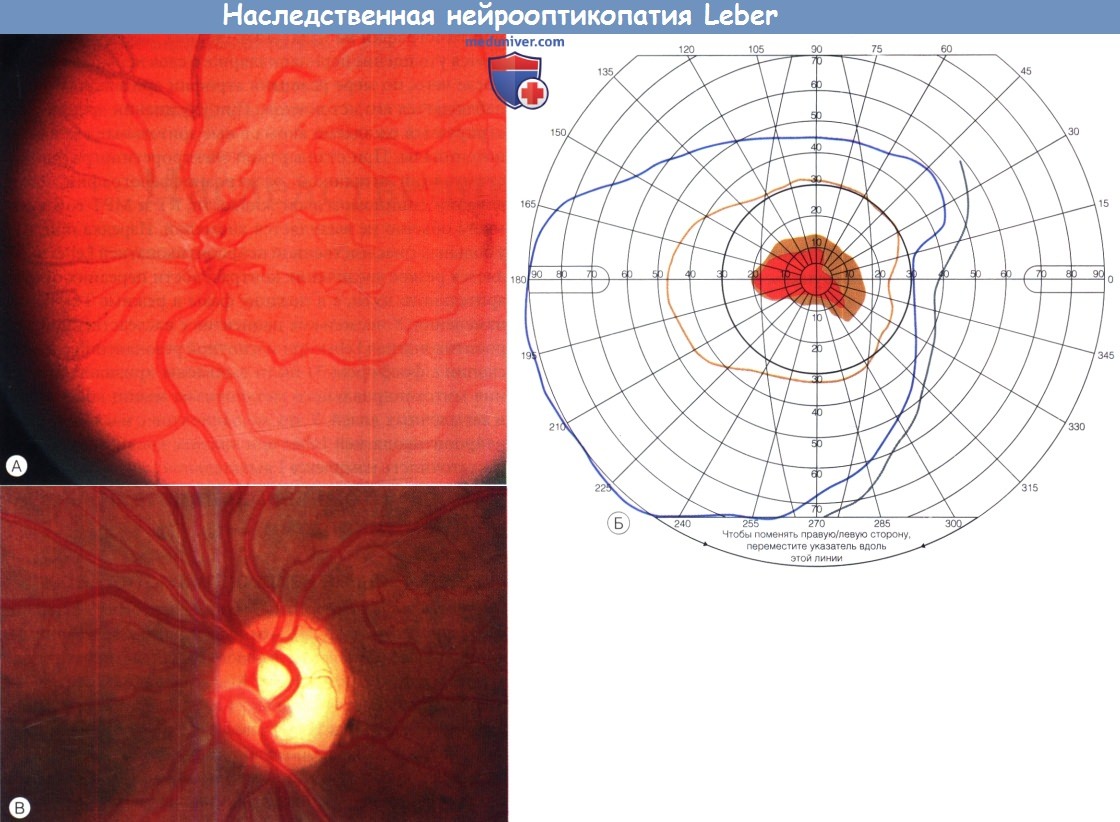
(А) Глазное дно левого глаза в период ухудшения зрения; отмечается легкая гиперемия диска зрительного нерва и перипапиллярные телеангиэктазии.
(Б) При периметрии по Goldmann выявляется центральная скотома левого глаза.
(В) Бледный диск зрительного нерва с экскавацией через пять месяцев после ухудшения зрения у пациента с наследственной нейрооптикопатией Leber. 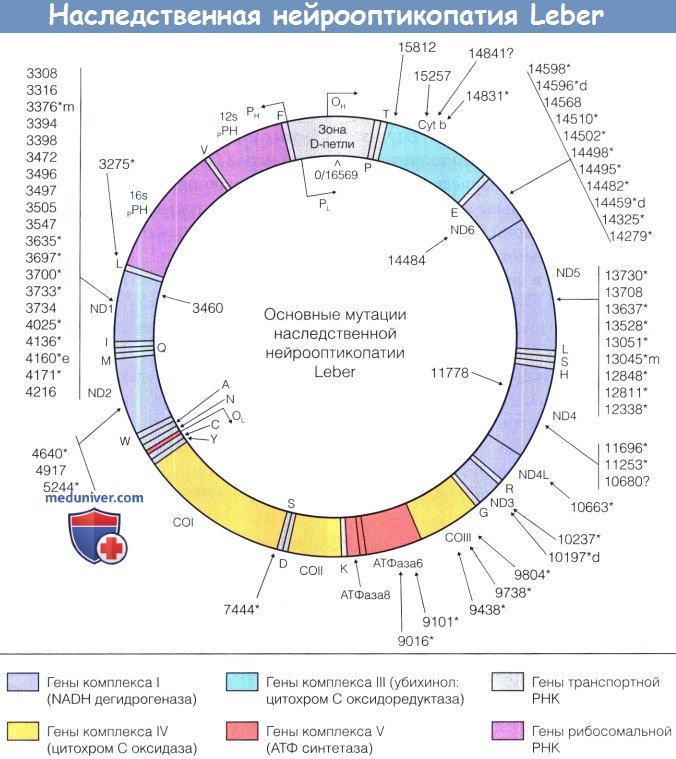
Более 90% всех случаев наследственной нейрооптикопатии Leber вызываются одной из трех основных мутаций, отмеченных внутри генома (кольца); другие мутации отмечены снаружи от генома.
Последние значительно различаются по встречаемости, степени эволюционного консерватизма измененной кодируемой аминокислоты и встречаемости в контрольной группе.
Мутации, отмеченные символом * также, возможно, могут быть отнесены к основным, но каждая из них во всем мире выявлена только в одной или в единичных семьях.
Мутации, отмеченные символом ** — основные мутации, вызывающие наследственную нейрооптикопатию Leber и дистонию.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Что такое оптическая нейропатия Лебера и можно ли ее вылечить?
Если у молодого мужчины резко ухудшается центральное зрение, а в зрительном поле возникают «слепые» пятна, это веский повод для обращения к офтальмологу. В ряде случаев подобные симптомы указывают на болезнь Лебера. Подробнее о клинических признаках, причинах развития и возможном лечении данного заболевания расскажем в статье.
Во второй половине 19 века немецкий врач Теодор Лебер описал глазную патологию, получившую название LHON — наследственная оптическая нейропатия Лебера. Это заболевание представляет собой атрофию оптического нерва, которая обусловлена мутациями в митохондриальных ДНК. Считается, что болезнь передается от матери и родственников по материнской линии. При этом в подавляющем большинстве случаев она проявляется у мужчин. Симптомы LHON впервые дают о себе знать в молодом возрасте — от 18 до 30 лет. Гораздо реже патология проявляются у детей или мужчин более старшего возраста.
Несмотря на то, что заболевание известно уже давно, ученые до сих пор не до конца понимают механизм и причины его развития. Однако после ряда исследований было установлено, что провоцирующим фактором для проявления наследственной патологии могут быть курение и употребление алкоголя.
Какими симптомами характеризуется оптическая нейропатия Лебера?
Сложность диагностики
Болезнь Лебера сложно поддается диагностике. Чтобы выявить данное заболевание, врач должен провести большой перечень диагностических мероприятий, который включает офтальмоскопию, изучение анамнеза (в частности наследственного), нейроофтальмологическое обследование, консультацию врача-генетика.
Зачастую главная сложность состоит в том, чтобы дифференцировать LHON от других заболеваний с похожей клинической картиной. В частности аналогичными симптомами могут сопровождаться невриты при рассеянном склерозе, болезнь Либмана-Сакса и другие заболевания. Поставить правильный диагноз помогает дифференциальная диагностика.
Лечение существует?
Сегодня эту болезнь лечат исключительно симптоматически. Специфических способов терапии до сих пор не существует, потому что ученым не известны механизмы развития патологии. Прогноз в большинстве случаев предполагает стойкое снижение зрения обоих глаз.
Время от времени исследователи предлагают новые способы лечения оптической нейропатии Лебера, но все существующие методики пока носят экспериментальный характер, проходят стадию испытаний или не подтвердили свою эффективность.
Амавроз Лебера
Амавроз Лебера – это наследственное заболевание, характеризующееся врожденным поражением светочувствительных клеток сетчатки глаза и в некоторых случаях другими общими нарушениями (аномалии почек, ЦНС). При этой патологии в первые месяцы жизни ребенка или сразу после рождения появляется нистагм, ослабление или отсутствие реакции зрачка на свет. В дальнейшем ребенок может тереть глаза (симптом Франческетти), возникает дальнозоркость и светобоязнь, возможна полная потеря зрения. Диагностика основывается на данных осмотра пациента врачом-офтальмологом, электроретинографии, исследования наследственного анамнеза и генетических анализов. Специфическое лечение амавроза Лебера на сегодняшний день не разработано.
МКБ-10
Общие сведения
Врожденный амавроз Лебера представляет собой гетерогенную группу заболеваний, причиной которых выступают мутации в 18 генах, кодирующих различные белки сетчатки, в том числе опсин. Впервые амавроз был описан еще в XIX веке (в 1867 году) Т. Лебером, указавшим основные проявления этого заболевания – маятниковый нистагм, слепота, появление пигментных пятен и включений на глазном дне. Средняя распространенность заболевания составляет 3:100000 населения.
Амавроз Лебера в равной мере поражает как мужчин, так и женщин. Заболевание составляет примерно 5% от всех наследственных ретинопатий. Современная генетика разрабатывает методики лечения данной патологии, имеются обнадеживающие результаты генной терапии одной из форм амавроза Лебера, обусловленной мутацией в гене RPE65. Отдельно выделяют атрофию зрительных нервов Лебера, которая также характеризуется постепенной потерей остроты зрения и впоследствии полной слепотой. Однако это заболевание совершенно другой генетической природы и обусловлено повреждением митохондриальной ДНК, которая имеет свой уникальный тип наследования (по материнской линии).
Причины
Основной механизм расстройства зрения при амаврозе Лебера – нарушение метаболизма в палочках и колбочках, которое ведет к летальным повреждениям фоторецепторов и их разрушению. Однако непосредственная причина таких изменений различается в зависимости от того, мутация какого именно гена вызвала заболевание.
Один из наиболее распространенных типов амавроза Лебера (тип 2, LCA2) обусловлен наличием мутантного гена RPE65 на первой хромосоме. Известно более 80-ти мутаций этого гена, некоторые из которых, помимо амавроза Лебера, вызывают и определенные формы пигментной абиотрофии сетчатки. Белок, кодируемый PRE65, отвечает за метаболизм ретинола в пигментном эпителии сетчатой оболочки глаза, поэтому при наличии генетического дефекта этот процесс нарушается с развитием побочных метаболических путей. В результате этого синтез родопсина в фоторецепторах прекращается, что и приводит к характерной клинической картине заболевания. Мутантные формы гена наследуются по аутосомно-рецессивному механизму.
Менее распространенная форма амавроза Лебера (тип 14) вызвана мутацией гена LRAT на 4-й хромосоме. Он кодирует белок лецитин-ретинол-ацилтрансферазу, который располагается в микросомах гепатоцитов и обнаружен в сетчатке глаза. Этот фермент участвует в метаболизме ретиноидов и витамина А, из-за наличия мутаций в гене полученный протеин не может полноценно выполнять свои функции, из-за чего развивается дегенерация фоторецепторов, которая клинически проявляется амаврозом Лебера или ювенильной пигментной абиотрофией сетчатки. Имеет аутосомно-рецессивный характер наследования.
Амавроз Лебера тип 8 наиболее часто приводит к врожденной слепоте, ответственный за развитие этой формы заболевания ген CRB1 располагается на 1-й хромосоме и имеет аутосомно-рецессивный характер наследования. При этом выяснено, что кодируемый данным геном белок принимает непосредственное участие в эмбриональном развитии фоторецепторов и пигментного эпителия сетчатки. Более точных данных по патогенезу данной формы амавроза Лебера на сегодняшний день не накоплено. Аналогичная ситуация с мутацией гена LCA5, расположенного в 6-й хромосоме и ассоциированного с 5-м типом амавроза. В настоящее время выявлен только белок, кодируемым данным геном – леберцилин, но его функции в сетчатке непонятны.
Также выявлено две формы амавроза Лебера, которые наследуются по аутосомно-доминантному механизму – тип 7, обусловленный мутацией гена CRX, и тип 11, ассоциированный с нарушением гена IMPDH1. Ген CRX кодирует белок, который обладает множеством функций – контроль развития фоторецепторов в эмбриональный период, поддержание их адекватного уровня во взрослом возрасте, участие в синтезе других протеинов сетчатки (является фактором транскрипции). Поэтому в зависимости от характера мутации гена CRX клиника амавроза Лебера 7-го типа может быть разнообразной – от врожденной слепоты до относительно позднего и вялотекущего ухудшения зрения.
Инозин-5′-монофосфатдегидрогеназа 1, кодируемый геном IMPDH1, представляет собой фермент, регулирующий рост клеток и образование нуклеиновых кислот, однако это пока не позволяет прояснить патогенез того, как нарушения этого белка приводят к 11-му типу амавроза Лебера.
Классификация амавроза Лебера
В настоящее время полностью доказана взаимосвязь между клиническими проявлениями и мутациями определенных генов для 16-ти типов амавроза Лебера. Также имеются указания об открытии еще двух генов, повреждения в которых приводят к такому заболеванию, но пока в этом отношении проводятся дополнительные исследования.
Кроме того, иногда в клинической классификации выделяют не только название поврежденного гена, но и характер мутации, поскольку это имеет значительное влияние на течение амавроза Лебера. Более того, различные типы мутаций в одном и том же гене могут приводить к совершенно разным заболеваниям – например, некоторые разновидности делеций в гене CRX могут приводить не к амаврозу, а к палочко-колбочковой дистрофии. Некоторые мутации генов RPE65, LRAT и CRB1 являются причиной различных форм пигментной абиотрофии сетчатки.
Симптомы амавроза Лебера
Симптоматика амавроза Лебера достаточно вариабельна и зависит от типа заболевания и характера мутации гена. В большинстве случаев при рождении ребенка патология не определяется – даже при осмотре глазного дна изменения наблюдаются лишь в нескольких процентах случаев. По мере его роста родители могут замечать, что ребенок не задерживает взгляд на предметах и окружающих, а в более старшем возрасте может болезненно реагировать на свет (появляется фотофобия), часто тереть глаза и указывать на них пальцем (симптом Франческетти, окулопальцевый синдром). Обнаруживается нистагм, который возникает еще в первые 2-3 месяца жизни и часто является одним из первых проявлений амавроза Лебера, замедленная реакция зрачка на свет или ее полное отсутствие.
В ряде случаев наблюдается врожденная слепота. Если же ребенок родился с относительно сохранной функцией зрения, то в первые годы жизни, помимо указанных симптомов, у его также развивается дальнозоркость, косоглазие, сильно страдает острота зрения. Обычно к 10-ти годам большинство больных с амаврозом Лебера полностью слепнут. В дальнейшем у них могут возникать и другие нарушения зрительного аппарата – кератоконус, катаракта, глаукома. При некоторых типах заболевания могут наблюдаться и сопутствующие нарушения – поражения ЦНС, глухота.
Диагностика
В современной офтальмологии диагностика амавроза Лебера производится на основании осмотра глазного дна, мониторинга динамики изменений в нем, данных электроретинографии. Немаловажную роль играет также изучение наследственного анамнеза, а для некоторых типов заболевания – генетическое секвенирование последовательности ключевых генов.
Дифференциальную диагностику производят с различными формами пигментной абиотрофии сетчатки (при ней сохраняется нормальная или немного сниженная амплитуда волн на электроретинограмме) и некоторыми типами атрофии зрительных нервов.
Лечение амавроза Лебера
На сегодняшний день специфического лечения любого типа амавроза Лебера не существует. На этапе клинических испытаний находится генно-инженерное введение гена RPE65 в сетчатую оболочку глаза больных амаврозом 2-го типа, имеются первые данные о значительном улучшении зрения подопытных больных. В случае же остальных форм заболевания такого прогресса пока нет. Поддерживающее лечение сводится к витаминной терапии, внутриглазным инъекциям сосудорасширяющих средств. При дальнозоркости назначается ношение очков.
Прогноз
В плане сохранения зрения прогноз крайне неблагоприятный, практически 95% больных полностью теряют способность видеть к 10-му году жизни. Кроме того, это наследственное заболевание может осложняться проблемами с ЦНС, почками, эндокринной системой, что требует более тщательного медицинского мониторинга для своевременного выявления подобных нарушений.