Болезнь грейвса что это
Диффузный токсический зоб (Болезнь Грейвса)
Впервые эту болезнь описали сразу два ученых: ирландец Тринити Роберт Джеймс Грейвс и немец Карл Адольф фон Базедов. Поэтому в англоязычной литературе она известна как болезнь Грейвса, а в немецкой литературе – как Базедова болезнь, именно этот термин получил распространение и в России.
Болезнь Грейвса или диффузный токсический зоб – это аутоиммунное заболевание, которое связано с появлением в организме антител к рецептору тиреотропного гормона.
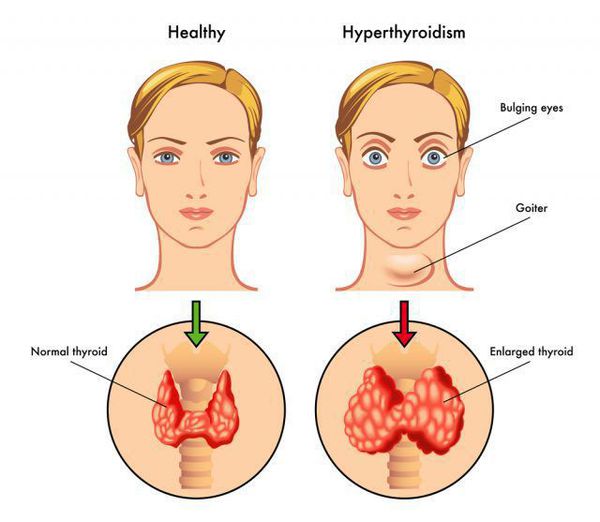
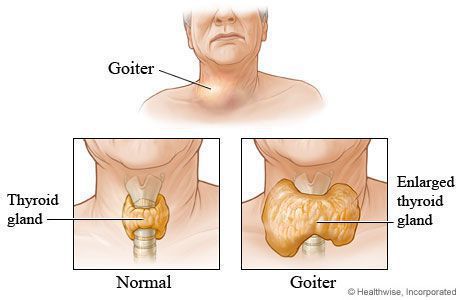
В норме на щитовидной железе есть рецепторы тиреотропного гормона (ТТГ), который вырабатывается гипофизом и регулирует работу щитовидной железы. При болезни Грейвса организмом начинают вырабатываться антитела, которые связываются с этими рецепторами подобно самому ТТГ. Это приводит к гиперстимуляции щитовидной железы и её гиперфункции, она начинает активно вырабатывать гормоны. У пациента развивается тиреотоксикоз. При этом степень увеличения щитовидной железы и тяжесть тиреотоксикоза – это два фактора, которые не связаны между собой. Пораженная щитовидная железа может увеличиваться в размерах, а может быть и нормального объёма. Причины болезни пока не определены. Известно, что существует генетическая предрасположенность, а также тот факт, что болезнь чаще возникает у людей с другими заболеваниями эндокринной системы (сахарный диабет, болезнь Аддисона).
Ситуация тиреотоксикоза, возникающая на фоне гиперфункции железы, потенциально опасна для жизни. Гормоны щитовидной железы регулируют обмен веществ. Высокая концентрация этих гормонов в организме человека сравнима с ситуацией выполнения тяжёлой физической работы или больших нагрузок. Человек с тиреотоксикозом испытывает высокие нагрузки на все органы и системы даже пребывая в покое. Это приводит к тому, что организм начинает истощаться, многие больные теряют вес, жалуются на появление патологической утомляемости и усталости, повышенную потливость, нарушение работы пищеварительного тракта (рвота, диарея), нервной системы (раздражительность, нарушения сна). Интенсивная нагрузка приводит к декомпенсации сердечной деятельности. Появляются отёки, может повышаться температура тела, нарушается сердечный ритм. Человеческий организм не в силах «постоянно бежать стометровку», пациент может погибнуть.
Более чем в половине всех случаев болезнь Грейвса сопровождается так называемой эндокринной офтальмопатией или эндокринной орбитопатией. Это два разных заболевания, которые имеют один пусковой механизм. Нарушение работы щитовидной железы способствует разрастанию ретробульбарной клетчатки, которая приводит к тому, что глаза у пациента как бы выкатываются наружу. Поражаются глазодвигательные мышцы, ухудшается трофика глаз, процесс может закончиться полной потерей зрения.
Болезнь Грейвса является ограничением для роботических и эндоскопических операций. Удалять щитовидную железу при болезни Грейвса гораздо сложнее, чем удалять железу, поражённую раком. При болезни Грейвса щитовидная железа гипертрофирована за счёт увеличения клеток в размерах. Чем больше железа в размерах, тем сложнее хирургу выделять возвратные гортанные нервы, искать и сохранять околощитовидные железы. Поэтому при болезни Грейвса применяются открытые операции на щитовидной железе.
Гигантские объёмы щитовидной железы порой могут быть связаны с неадекватным назначением тиреостатиков, которые полностью блокируют работу щитовидной железы и вводят человека в состояние гипотиреоза. Щитовидная железа не работает, её гормоны снижаются, а ТТГ повышается, приводя к гипертрофии щитовидной железы. За несколько месяцев нерациональная консервативная терапия у пациента с болезнью Грейвса может привести к росту щитовидной железы до очень больших размеров, значительно осложнив работу хирурга.
При болезни Грейвса щитовидная железа – это мишень аутоиммунной агрессии, поэтому основное лечение направлено на подавление синтеза гормонов или удаление органа. На первом этапе лечения проводят консервативную терапию. Пациентам назначают тиреостатики – препараты, которые блокируют синтез гормонов в самой щитовидной железе. Обычно, в ходе консервативного лечения у 10-15% пациентов происходит спонтанная ремиссия. Тиреостатиками лечат не более 12-18 месяцев. Если ремиссии за это время не произошло, то переходят к радикальным мерам.
Болезнь Грейвса – это аутоиммунное заболевание, при котором можно удалить орган-мишень, сохранив достойное качество жизни. Существует два метода радикального лечения диффузного токсического зоба: хирургический и радиойодтерапия. Ключевым моментом в выборе метода является объём щитовидной железы. Терапия радиоактивным йодом, однократно может разрушить железу примерно на 50-60 мл. Если щитовидная железа значительно увеличена в размерах и требуется разрушить большой объем, то радиоактивный йод назначается ступенчато, либо выбор делается в пользу операции.
После удаления железы пациенту назначается заместительная терапия, компенсирующая возникший гормональный дефицит. Иногда после удаления щитовидной железы и начала заместительной терапии пациенты начинают прибавлять в весе. Однако, этот момент не связан с негативным влиянием гормональных препаратов. Прибавка в весе происходит потому, что на фоне тиреотоксикоза пациенты сильно теряли в весе, а в стабильном состоянии, на фоне заместительной терапии, они возвращаются к нормальной массе тела.
Важно! Если уже при первом обращении пациенту установлен диагноз «болезнь Грейвса», и у него регистрируются высокие титры антител, напряжённый аутоиммунный статус, то в данном случае ремиссия на фоне консервативной терапии маловероятна. Следует прибегнуть к оперативному лечению или терапии радиоактивным йодом в более ранние сроки.
Пациенты с болезнью Грейвса часто интересуются, можно ли с заболеваниями щитовидной железы ездить в страны с жарким климатом. В настоящее время диффузный токсический зоб, как и рак щитовидной железы, не является противопоказанием к пребыванию в жарком климате. Доказано, что факторы внешней среды никак не влияют на течение болезни. Кроме этого, определенный процент людей с болезнью Грейвса постоянно проживает в южных широтах.
Не менее частый вопрос связан с возможностью планировать беременность после терапии радиоактивным йодом. После лечения радиоактивным йодом не рекомендовано планировать беременность в течение полугода. В меньшей степени это ограничение связано с радиацией, а в большей степени с тем, что имеется высокий процент невынашивания плода в эти полгода. Точная причина невынашивания до сих пор неизвестна.
Мнение, что пациенткам, которые были прооперированы по поводу рака щитовидной железы или диффузного токсического зоба, нельзя беременеть в течении 10 лет является заблуждением. Есть пациентки, у которых заболевание выявляется на фоне уже имеющейся беременности. Операция, выполненная на фоне беременности и после родов, никак не влияет на прогноз.
Если пациентке уже была проведена резекция щитовидной железы и назначена заместительная терапия, то на период беременности врач увеличит дозу препарата, а после родов вернет его к исходной дозе.
Мужчинам не рекомендуется участвовать в зачатии в течение 120 дней с момента окончания лечения радиоактивным йодом. Это связано с периодом жизни сперматозоидов.
Тиреотоксикоз с диффузным зобом (E05.0)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
* термин, традиционно используемый в России и Казахстане
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
(Фадеев В.В.,Мельниченко Г.А., 2007)
Классификация зоба, рекомендованная ВОЗ (2001)
| Степень | Характеристики |
| 0 | Зоба нет (объем каждой доли не превышает объем дистальной фаланги большого пальца руки обследуемого) |
| 1 | Зоб пальпируется, но не виден при нормальном положении шеи; сюда же относят узловые образования, не приводящие к увеличению ЩЖ |
| 2 | Зоб четко виден при нормальном положении шеи |
| Степень | Характеристики |
|---|---|
| 0 | ЩЖ не пальпируется |
| I | Пальпаторно определяется увеличение перешейка ЩЖ |
| II | Пальпаторно определяются увеличенные боковые доли |
| III | Визуально определяется увеличение ЩЖ («толстая шея») |
| IV | Значительное увеличение ЩЖ (зоб ясно виден) |
| V | Зоб огромных размеров |
Патоморфологическая классификация ДТЗ
Этиология и патогенез
Эпидемиология
По данным литературы, 80-85% случаев синдрома тиреотоксикоза, диагностируемого во всем мире, вызвано диффузным токсическим зобом. В США и Англии частота новых случаев этой патологии варьирует от 30 до 200 случаев на 100 тыс. населения в год, соотношение больных женщин к мужчинам составляет 7:1.
Факторы и группы риска
Реализации генетической предрасположенности к диффузному токсическому зобу способствуют эмоциональные, стрессорные и экзогенные (курение) факторы.
Клиническая картина
Cимптомы, течение
Клиническая картина диффузного токсического зоба (ДТЗ) определяется синдромом тиреотоксикоза.
Характерные проявления тиреотоксикоза:
1. Поражение центральной и периферической нервной системы:
— возбудимость, повышенная раздражительность, плаксивость, суетливость, расстройство сна;
— тремор пальцев вытянутых рук (симптом Мари) и всего тела (симптом «телеграфного столба»);
— повышение сухожильных рефлексов;
— мышечная слабость, нарастающая при отсутствии лечения;
— в тяжелых случаях возможно развитие тиреотоксического психоза.
5. Синдром эктодермальных нарушений: ломкость ногтей, выпадение волос, горячая, бархатистая на ощупь кожа
Синдром тиреотоксикоза в 2/3 случаев развивается примерно на один год раньше ЭОП, которая у 50% больных имеет различную степень выраженности. При наличии выраженной ЭОП возможно практически безошибочно установить диагноз. Это связано стем, что уже по клинической картине среди заболеваний, протекающих с тиреотоксикозом, ЭОП сочетается преимущественно с ДТЗ.
Диагностика
Основные методы обследования
1. Анамнез: наличие аутоиммунной патологии щитовидной железы (ЩЖ) среди родственников, «короткая» история заболевания: симптомы развиваются и прогрессируют, как правило, быстро и в большинстве случаев приводят пациента к врачу через 6-12 месяцев от начала заболевания.
2. Физикальное обследование:
— определение веса, роста;
— исследование кожных покровов, волос, ногтей;
— определение АД, частоты и ритмичности пульса;
— определение тремора кончиков пальцев вытянутых рук, тела.
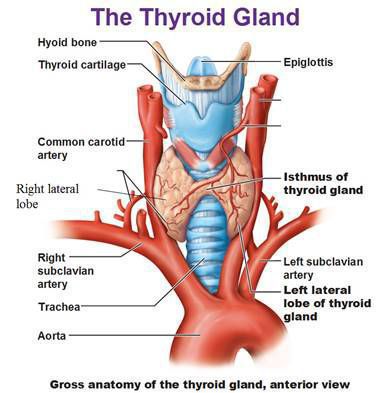
3. Осмотр и пальпация ЩЖ: определение размеров ШЖ, наличия пальпируемых узлов.
4. Офтальмологическое обследование: наличие экзофтальма, глазных симптомов, состояние глазного дна. Согласно рекомендациям тиреоидологической секции Немецкого эндокринологического общества по диагностике болезни Грейвса-Базедова, при наличии эндокринной офтальмопатии (ЭОП) диагноз иммуногенного тиреотоксикоза (диффузного токсического зоба) можно считать подтвержденным, поэтому дальнейший диагностический поиск, направленный на определение причины тиреотоксикоза, как правило, нецелесообразен.
5. УЗИ ЩЖ: диффузное увеличение объема ЩЖ, гипоэхогенность ткани, усиление ее кровотока.
6. Определение содержания ТТГ и свободного Т4 (св.Т4):
— уровень ТТГ снижен менее 0,2 МЕ/л или не определяется (подавлен);
— уровень св.Т4 повышен (при манифестной форме);
— если уровень св.Т4 определяется в пределах нормы, то показано определение св. Т3 для диагностики Т3-тиреотоксикоза.
Если содержание свободных фракций тиреоидных гормонов в пределах референсных значений, то имеет место субклинический тиреотоксикоз.
Дополнительные методы обследования (применяются по показаниям)
1. Изотопная сцинтиграфия (с 131I или 99mТс) позволяет выявить диффузное усиление захвата изотопа ЩЖ. Применяется в диагностически неясных случаях, а также при наличии в ЩЖ пальпируемых или превышающих в диаметре 1 см узловых образований.
Кормящим женщинам (при дифференциальной диагностике ДТЗ и послеродового тиреоидита) исследование проводят с изотопом 99mТс; после введения обычной дозы технеция кормление грудью безопасно для ребенка уже через 12 часов.
3. Тонкоигольная пункционная биопсия (ТАБ)
6. Общий анализ крови: возможны признаки нормоцитарной или железодефицитной анемии.
7. Биохимический анализ крови: возможно снижение уровня холестерина и триглицеридов в результате повышенного клиренса, повышение печеночных трансаминаз, ЩФ, гипергликемия, гиперкальциемия.
Лабораторная диагностика
1. Определение содержания ТТГ и свободного Т4 (св.Т4):
— уровень ТТГ снижен менее 0,2 МЕ/л или не определяется (подавлен);
— уровень св.Т4 повышен (при манифестной форме);
— если уровень св.Т4 определяется в пределах нормы, то показано определение св. Т3 для диагностики Т3-тиреотоксикоза.
Если содержание свободных фракций тиреоидных гормонов в пределах референсных значений, то имеет место субклинический тиреотоксикоз.
4. Общий анализ крови: возможны признаки нормоцитарной или железодефицитной анемии.
5. Биохимический анализ крови: возможно снижение уровня холестерина и триглицеридов в результате повышенного клиренса, повышение печеночных трансаминаз, ЩФ, гипергликемия, гиперкальциемия.
Дифференциальный диагноз
2. Хронический лимфоцитарный тиреоидит. При данном заболевании тиреотоксикоз встречается менее чем в 5% случаев и, как правило, бывает преходящим. ЩЖ может быть совсем не увеличена или очень сильно увеличена, но чаще всего имеется небольшой плотный зоб.
При пальпации ЩЖ безболезненна.
Наблюдается повышение общего T4, что связано с повреждением ткани железы.
Основные дифференциально-диагностические признаки хронического лимфоцитарного тиреоидита и ДТЗ:
На уровень тиреоидных гормонов в крови могут значительно повлиять изменения в связывании их с протеинами плазмы на фоне беременности, под влиянием некоторых медикаментов, при тяжелых нетиреоидных заболеваниях.
Наиболее частые причины сниженного уровня ТТГ в крови, не связанные с заболеваниями ЩЖ:
1.1 Тяжелые соматические заболевания.
1.2 Острый психоз. Общий T4 и свободный T4 (расчетный свободный T4) повышены почти у трети больных, госпитализированных с острым психозом. У 50% пациентов с повышенным уровнем T4 увеличен и уровень T3. Данные показатели нормализуются через 1-2 недели без лечения антитиреоидными средствами.
Предположительно повышение уровней тиреоидных гормонов вызвано выбросом ТТГ. Однако при первичном обследовании госпитализированных больных с психозом уровень ТТГ, как правило, снижен или находится на нижней границе нормы. Вероятно, уровень ТТГ может повышаться на ранней стадии психоза (до госпитализации). Действительно, у некоторых больных с пристрастием к амфетаминам, госпитализированных с острым психозом, находят недостаточное снижение уровня ТТГ на фоне повышенного уровня T4.
1.3 Высокий уровень хорионического гонадотропина (I триместр беременности, токсикоз беременных, беременность с пузырным заносом, хорионкарцинома).
У всех женщин во время беременности повышение уровня общего Т4 связано с повышением уровня ТСГ (тироксинсвязывающего глобулина) под действием избытка эстрогенов. В связи с этим для оценки функции ЩЖ во время беременности должен использоваться уровень свободного Т4 и ТТГ.
2. Лекарственные средства:
— прием высоких доз левотироксина натрия;
— лечение ГКС;
— прием бромокриптина.
Осложнения
Лечение
Цели лечения диффузного токсического зоба (ДТЗ):
1. Купирование проявлений тиреотоксикоза.
2. Нормализация лабораторных показателей уровня тиреоидных гормонов в крови.
3. Достижение иммунологической ремиссии заболевания.
Алгоритм лечения ДТЗ (Национальное руководство. Эндокринология, стр. 527)
Немедикаментозное лечение:
1. Ограничение поступления йодсодержащих препаратов (йодсодержащие контрастные вещества, витамины, содержащие йод и др.).
2. Исключение кофеина, курения, физических нагрузок.
3. Полноценное питание с достаточным количеством витаминов и микроэлементов.
4. Для восстановления нормального сна и снижения повышенной раздражительности пациента назначают седативные препараты.
Консервативная терапия
У пациентов с небольшим увеличением ЩЖ (объем менее 30 мл), при отсутствии в ней клинически значимых узловых образований, возможно проведение длительной (12-18 месяцев) консервативной терапии, которая в 30-40% случаев приводит к стойкой ремиссии заболевания.
Следует иметь в виду, при развитии рецидива заболевания после одного курса терапии тиреостатиками, назначение второго курса бесперспективно.
В медикаментозном лечении ДТЗ тиреостатиками выделяют две основные фазы.
Для предотвращения рецидивов тиреотоксикоза поддерживающие дозы тиреостатических препаратов рекомендовано применять в течение длительного времени (12-18 месяцев) без перерыва, под контролем общего анализа крови (лейкоциты и тромбоциты) 1 раза в месяц.
Начиная от момента нормализации концентрации Т4 или несколько позже, параллельно пациенту назначают левотироксин натрия в дозе 50-100 мкг/сут. Такая схема получила название «блокируй и замещай»: один препарат блокирует железу, другой замещает формирующийся дефицит тиреоидных гормонов. Поддерживающую терапию по данной схеме (10-15 мг тиамазола и 50-100 мкг левотироксина натрия) необходимо проводить от 12 до 24 месяцев.
Пациентам с высоким риском тиреотоксикоза (большой размер зоба, высокий титр антитиреоидных антител и тиреоидных гормонов при диагностике заболевания) может быть рекомендована комбинированная терапия, если по каким-либо причинам у них невозможно проведение более радикального лечения (хирургического или радиоактивным йодом).
В случае, если пациент не может регулярно контроль функции ЩЖ, ему также можно предложить данную схему лечения.
После окончания курса лечения препараты отменяют. Рецидив заболевания чаще всего развивается в течение первого года после отмены препаратов.
При лечении тиреотоксикоза по возможности следует ограничиться минимальной дозой для поддержания эутиреоидного состояния, поскольку высокие дозы тиреостатиков не снижают частоту рецидивов, но могут повышать частоту побочных реакций (аллергические реакции, гепатит, артрит, агранулоцитоз ).
Препараты йода (в дозе более чем 0,1 мг/кг массы тела) угнетают интратиреоидный транспорт йода и биосинтез тиронинов по принципу ультракороткой обратной связи, а также снижают скорость высвобождения тиреоидных гормонов в кровь.
В настоящее время их применение ограничено вследствие непродолжительного тиреостатического действия (не более 14-16 суток).
Йодиды, как правило, применяются для предоперационной подготовки больных ДТЗ в сочетании с тиреостатиками, а также в комплексе с другими лекарственными средствами для лечения тиреостатичсекого криза. Используется йод/калия йодид в дозе 3-5 капель 3 раза в сутки, 10-14 суток.
Терапия ß-адреноблокаторами
Применяется в качестве симптоматического лечения, которое направлено на ослабление симптомов тиреотоксикоза, вызванных действием катехоламинов:
— неселективные ß-блокаторы: пропраналол;
— селективные ß-блокаторы: атенолол, метопролол.
Данные препараты обладают способностью быстро смягчать симптомы тиреотоксикоза и обеспечивают быстрый положительный эффект от начала лечения, что делает их жизненно необходимыми в лечении ДТЗ.
Селективные ß-блокаторы предпочтительнее, поскольку они также уменьшают периферическую конверсию Т4 в Т3.
После достижения эутиреоза, ß-блокаторы отменяют.
Дозировка:
— атенолол внутрь 50 мг 1-2 раза/сут., до ликвидации клинических проявлений или
— метопролол внутрь 50 мг 2-3раза/сут., до ликвидации клинических проявлений или
— пропранолол внутрь 20-40 мг 3-4 раза/сут., до ликвидации клинических проявлений.
Хирургический метод
Оперативное лечение оптимально в следующих ситуациях:
— неэффективность консервативного лечения (наличие рецидивов, тяжелое течение ДТЗ);
— невозможность консервативного лечения (аллергия к антитиреоидным препаратам, агранулоцитоз и др.);
— беременность;
— детский возраст;
— большие размеры зоба с признаками сдавления близлежащих органов или узловая его форма, в том числе тиреотоксическая аденома и многоузловой токсический зоб;
— загрудинное расположение зоба.
Терапия радиоактивным йодом применяется в следующих случаях:
— рецидив тиреотоксикоза после оперативного лечения ДТЗ на фоне медикаментозного лечения;
— невозможность консервативного лечения;
— наличие выраженных сердечно-сосудистых нарушений у пациентов с небольшими размерами ЩЖ.
Сравнительная характеристика хирургического лечения и терапии радиоактивным йодом
| Хирургическое лечение | Терапия радиоактивным йодом |
| Предельно субтотальная резекция ЩЖ | Доза 150-200 гр. с расчетом активности на объем всей ЩЖ |
| Быстрая ликвидация тиреотоксикоза (несколько часов) | Ликвидация тиреотоксикоза в течение нескольких недель |
| Проводится на фоне эутиреоза, достигнутого тиреостатиками | Не требует подготовки; более дешевый метод |
| Крайне нежелательно при послеоперационном рецидиве тиреотоксикоза | Метод выбора при послеоперационном рецидиве тиреотоксикоза |
| Специфические осложнения: парез гортани и гипопаратиреоз | Абсолютное противопоказание: беременность и лактация |
| Предпочтительно при зобе большого размера | При большом размере зоба (более 60 мл) метод менее предпочтителен |
И при хирургическом лечении, и при терапии радиоактивным йодом возникающий гипотиреоз рассматривается не как осложнение, а как цель этих методов лечения. Как следствие, прием левотироксина натрия в индивидуальной дозе с заместительной целью назначается пожизненно.
После терапии радиоактивным йодом и хирургического лечения: контроль функции ЩЖ необходимо выполнять через 3 месяца, 6 месяцев, затем ежегодно.
Что такое зоб диффузный токсический (Базедова болезнь)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Родионова Е. А., терапевта со стажем в 13 лет.
Определение болезни. Причины заболевания
Диффузный токсический зоб — это аутоиммунное поражение щитовидной железы.
В англоязычных странах это заболевание называют болезнью Грейвса, а немецкоязычных — Базедовой болезнью. Диффузный токсический зоб развивается из-за нарушенной функции СД8+-лимфоцитов и выработки антитиреоидных антител, среди которых особое значение придаётся тем, которые имеют сродство к рецепторам тиреотропного гормона в щитовидной железе. Эти антитела выявляются в среднем у 50% пациентов с диффузным токсическим зобом. С этими рецепторами в норме связывается тиреотропный гормон (ТТГ), что стимулирует выработку и выделение тиреоидных гормонов (ТГ). Антитела при связывании с рецепторами ТТГ увеличивают секрецию тироксина (Т4) и трийодтиронина (Т3) «в обход» регуляции ТТГ. Повышенный уровень тиреотропного гормона обуславливает развитие тиреотоксикоза. До конца не ясна причина такого дефекта иммунной системы. Имеются данные, позволяющие говорить о роли генетической предрасположенности, в частности, более широкой распространённости аллелей HLA-B8 и BW-35 у пациентов с этой болезнью. [4] Однако не выявлено какой-то одной аллели, ответственной за болезнь Грейвса. Вероятно, здесь имеет место взаимодействие нескольких аллелей.
Симптомы диффузного токсического зоба
При Базедовой болезни могут появляться признаки эндокринной офтальмопатии, возникающей из-за поражения периорбитальной клетчатки: выраженный экзофтальм (не всегда симметричный), диплопия, отечность век, ощущение «инородного тела в глазах». Это сильно облегчает работу врача в плане диагностики, так как среди всех состояний с тиреотоксикозом эндокринная офтальмопатия характерна именно для диффузного токсического зоба. Не следует путать эндокринную офтальмопатию с глазными симптомами тиреотоксикоза, среди которых можно выделить синдром Грефе и синдром Кохера (верхнее веко отстаёт при взгляде вверх и вниз соответственно), синдром Мебиуса (взгляд не фиксируется вблизи), синдром Штельвага (уменьшение частоты морганий). Стоит отметить, что выраженность глазных симптомов не зависит от тяжести дисфункции щитовидной железы. [4]
Некоторые авторы в развитии диффузного токсического зоба выделяют четыре стадии:
Патогенез диффузного токсического зоба
Классификация и стадии развития диффузного токсического зоба
Согласно классификации тиреотоксикоза по Фадееву В.В. и Мельниченко Г.А., выделяется:
Также существует классификация зоба (патологического увеличения щитовидной железы), в которой выделяется три степени зоба, в зависимости от данных осмотра и пальпации щитовидной железы.
Классификация зоба, рекомендованная ВОЗ (2001)
Осложнения диффузного токсического зоба
Развившийся при диффузном токсическом зобе тиреотоксикоз поражает все системы организма. Если надлежащим образом не лечить это заболевание, то оно грозит тяжёлой инвалидизацией, а аритмии и сердечная недостаточность даже могут привести к летальному исходу.
Наиболее опасным осложнением болезни Грейвса является тиреотоксический криз, развитие которого связывают с неблагоприятными факторами (стресс, различные заболевания, выраженная физическая нагрузка, операция и др.). Появляется резкое возбуждение, температура повышается до 40 о С, частота сердечных сокращений достигает 200 ударов в минуту, может развиться фибрилляция предсердий, усиливаются явления диспепсии (тошнота, рвот, понос, жажда), повышается пульсовое артериальное давление. Затем могут появиться признаки недостаточности надпочечников (гиперпигментация, нитевидный пульс, нарушение микроциркуляции). Состояние ухудшается за несколько часов. Это ургентная ситуация, требующая неотложных мер, направленных на снижение концентрации ТГ, борьбу с надпочечниковой недостаточностью, дегидратацией, гипертермией, метаболическими нарушениями и недостаточностью кровообращения. В/в вводится гидрокортизон, проводится дезинтоксикационная и тиреостатическая терапия. К осложнениям диффузного токсического зоба также можно отнести осложнения хирургического его лечения: гипопаратиреоз, повреждение n. laryngeus recurrens (при повреждении одного нерва появляется осиплость голоса, при повреждении двух может возникнуть асфиксия), кровотечения, аллергические реакции на препараты. Об осложнениях тиреостатической терапии будет сказано ниже. [5]
Диагностика диффузного токсического зоба
При наличии у пациента признаков тиреотоксикоза ему определяют уровень тиреотропного гормона (ТТГ) высокочувствительным методом (чувс. 0,01 мЕд/л). Если уровень ТТГ меньше нормы, то исследуют концентрацию св. Т4 (тетрайодтиронин, тироксин) и Т3 (трийодтиронин). Существует понятие о так называемом субклиническом тиреотоксикозе, когда уровни Т4 и Т3 оказываются в норме. Среди антител наибольшее клиническое значение имеет уровень антител к рецепторам ТТГ (АТ-рТТГ). Высокие их титры с большой долей вероятности указывают на то, что мы имеем дело именно с болезнью Грейвса. Другие антитела, такие, как антитела к тиреоидной пероксидазе и тиреоглобулину (АТ-ТПО и АТ-ТГ), выявляются и при других состояниях, поэтому имеют значение только в комплексной оценке, и их определение может помочь в некоторых ситуациях.
Лечение диффузного токсического зоба
Лечение болезни Грейвса может проводиться эндокринологом или терапевтом. К сожалению, в настоящее время лечение диффузного токсического зоба направлено только на орган-мишень, то есть щитовидную железу, а не на выработку антител, являющуюся непосредственной причиной развития болезни. Даже после удаления щитовидной железы продолжают синтезироваться антитела к рецепторам тиреотропного гормона, хотя тиреотоксикоза уже не возникает (при адекватной заместительной терапии). [9]
Итак, существует три способа лечения диффузного токсического зоба:
Выбор метода зависит от возраста, сопутствующих заболеваний, степени увеличения щитовидной железы, желания пациента и возможностей лечебного учреждения. Консервативный метод лечения диффузного токсического зоба заключается в назначении тиреостатиков. В некоторых случаях (до 30%) курс такого лечения способен привести к стойкой ремиссии, в некоторых — является подготовкой к использованию другого, более радикального метода (хирургическое лечение или терапия йодом-131). Считается, что консервативная терапия неэффективна при выраженном увеличении щитовидной железы (более 40 см 3 ) и с признаками сдавления окружающих тканей, при наличии крупных узлов в ней, а также при наличии осложнений (фибрилляция предсердий, остеопороз и др.). При рецидиве после курса терапии тиреостатиком, повторный длительный курс не назначается. [5] В подобных случаях проводится курс медикаментозной подготовки к радиойодтерапии или операции.
Важным условием адекватного проведения консервативного лечения является приверженность пациента к лечению и доступность лабораторного контроля. Тиреостатики блокируют синтез тиреоидных гормонов и купируют тиреотоксикоз. По прошествии 4-6 недель тиреостатической терапии, при наступлении эутиреоидного состояния, обычно к лечению добавляют левотироксин. [4] В период тиреотоксикоза (до нормализации Т4) также целесообразно назначение препаратов из группы β-адреноблокаторов: они подавляют тканевое превращение Т4 в Т3, снижают частоту сердечных сокращений. Критерием адекватности лечения является нормальный уровень Т4 и ТТГ. Курс лечения продолжается 12-18 месяцев. Во время лечения необходимо контролировать показатели общего анализа крови. Это необходимо для контроля грозных осложнений тиреостатической терапии — агранулоцитоза и тромбоцитопении, требующих немедленной отмены препаратов. Симптомы агранулоцитоза: лихорадка, боль в горле, жидкий стул. [4] При их появлении пациенту необходимо экстренно сдать кровь на общий анализ и прекратить приём тиреостатиков до получения результатов анализа. Рецидив чаще всего наступает в первые 12 месяцев после завершения курса.
Под хирургическим лечением подразумевается удаление всей или большей части щитовидной железы. [8] Операция проводится только в состоянии эутиреоза. В настоящее время удаление этого органа не является фатальным для человека, так как имеются все возможности адекватной и недорогой заместительной терапии левотироксином. С другой стороны, при оставлении даже небольшого фрагмента железы, сохраняется вероятность рецидива заболевания, это орган-мишень для антитиреоидных антител, выделяемых иммунной системой. Таким образом, послеоперационный гипотиреоз теперь не рассматривается в качестве осложнения операции, а является её целью. Доза левотироксина после операции подбирается индивидуально и обычно составляет 1,7 мкг/кг в сутки.