Блд у детей что
Бронхолегочная дисплазия у недоношенных детей
Нередко у недоношенных детишек после применения искусственной вентиляции легких (ИВЛ) развивается бронхолегочная дисплзия (БЛД). Возникает она благодаря нескольким факторам: это и собственно незрелость легких недоношенных детей, и интенсивный режим ИВЛ. Заболевание характеризуется полной ремиссией к 3-м годам жизни ребенка.
Почему возникает БЛД?
БЛД может возникать в результате дефицита сурфактанта (пленки, выстилающей альвеолы и препятствующей их спадению), отека легких, длительного применения высоких концентраций кислорода (повреждение свободными разикалами кислорода и т.д.), ИВЛ, воспаления, воздействия бактерий и вирусов и др. В результате действия вышепепречисленных факторов повреждаются практически все структурные компоненты незрелой легочной ткани, что приводит к хроническому нарушению функции легких и замещению здоровой ткани участками фиброза.
Как проявляется БЛД?
При наличии бронхолегочной дисплазии у ребенка отмечается бледность кожи и цианоз, учащается дыхание до 80-100 в мин, дыхание происходит с помощью дополнительной мускулатуры (межреберные мышцы). При выслушивании фонендоскопом: ослабленное дыхание, хрипы, либо жесткое дыхание. Если развивается тяжелая форма БЛД, то повреждаются и другие органы: сердце, почки, печень (ввиду перегрузки малого круга кровообращения).
Как наблюдаться у специалистов после выписки из стационара и на что обращать внимание?
Обязательно наблюдение участкового педиатра, с целью подбора терапии в периоды обострения, своевременного лечения рахита, коррекции анемии. Наблюдение пульмонолога, с целью подбора лечения, либо коррекции терапии БЛД, оценки функции внешнего дыхания.
Также важно следить за питанием малыша. Необходима прибавка в весе, избегание задержки роста. (достигается за счет повышенной каллорийности питания 140-150 ккал/кг/сутки, у матерей кормящих грудным молоком за счет обогащения молока усилителями, либо подбор специальной смеси).
Как часто наблюдаться у специалистов?
В зависимости от тяжести БЛД наблюдение специалистов происходит:
С чем связаны периоды обострения заболевания?
Бронхолегочная дисплазия
Общая информация
Краткое описание
Союз педиатров России
Год утверждения (частота пересмотра): 2016 (пересмотр каждые 3 года)
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Диагноз «бронхолегочная дисплазия» правомерен в качестве самостоятельного у детей до 3-летнего возраста, у детей после 3 лет БЛД указывается как заболевание, имевшее место в анамнезе. При ведении медицинской документации для оценки степени тяжести БЛД необходимо указывать вид респираторной терапии и состояние кислородозависимости ребенка в значимые для определения тяжести заболевания сроки.
***NCPAP (nose continious positive airway pressure) – постоянное положительное давление в дыхательных путях через носовые катетеры
Этиология и патогенез
Эпидемиология
Диагностика
У доношенных зрелых новорожденных факторами, предрасполагающими к развитию БЛД, являются синдром аспирации мекония, сепсис, нозокомиальная пневмония, персистирующая легочная гипертензия, гипоплазия легкого, диафрагмальная грыжа, пролонгированная ИВЛ, проводимая в связи с хирургические вмешательствами.
Клиническая картина новой формы БЛД характеризуется длительной кислородозависимостью и, в то же время, сравнительно редким возникновением БОС. Тогда как БЛД доношенных часто протекает с длительными, стойкими, резистентными к терапии бронхообструктивными эпизодами.
Уменьшение суммы баллов происходит, преимущественно, за счет снижения гиперинфляции и распространённости фиброзных проявлений. Вместе с тем, рентгенологические изменения при проведении ВРКТ в той или иной степени остаются у всех больных с БЛД до 2-х-летнего возраста и далее, независимо от степени тяжести заболевания.
Дифференциальный диагноз
Лечение
Комментарий: ранее допускалось в режиме «off label» после получения информированного согласия родителей при стойкой ЛГ, рефрактерной к стандартной терапии, в особенности при отсутствии возможностей для проведения ингаляций NO и экстракорпоральной мембранной оксигенации, согласия Локального этического и Формулярного комитетов в условиях специализированного стационара, с вариабельностью дозы от 1 до 8 мг/кг/сут. [25]. В настоящее время это назначение дискутабельно.
Прогноз
Профилактика
(Сила рекомендации 1; уровень доказательств B).
Бронхолегочная дисплазия
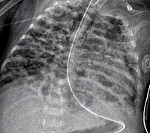
Бронхолегочная дисплазия (БЛД) – это хроническое заболевание дыхательной системы у новорожденных, которое возникает при проведении ИВЛ с использованием высоких концентраций кислорода на фоне респираторных нарушений. Основные проявления – синдром дыхательной недостаточности (ДН) и бронхиальной обструкции, деформация грудной клетки. Основа диагностики бронхолегочной дисплазии – рентгенография ОГК. Лечение при данной патологии включает в себя неспецифические терапевтические меры: рациональное питание и режим, адекватную респираторную поддержку, симптоматические медикаментозные препараты.
Общие сведения
Бронхолегочная дисплазия (БЛД) – это гетерогенная патология периода новорожденности, которая возникает при проведении ИВЛ с высокими концентрациями кислорода, сопровождается дыхательной недостаточностью, бронхообструктивным синдромом и гипоксемией. Впервые ввел этот термин, а также описал его рентгенологическую картину по стадиям американский педиатр и радиолог Нортвей в 1967 году. По своей сути БЛД является не врожденным, а ятрогенным заболеванием, что противоречит его названию, однако другого термина на данный момент не предложено. Она возникает у 16-40% новорожденных с массой тела менее 1500 г, которым необходима ИВЛ по поводу РДС. Общий показатель летальности при бронхолегочной дисплазии в течение первых 12 месяцев жизни составляет 10-25%.
Причины бронхолегочной дисплазии
Бронхолегочная дисплазия – это полиэтиологическое заболевание, которое формируется на фоне воздействия нескольких потенциальных этиологических факторов. К таковым относятся баротравма при нерациональной ИВЛ, морфологическая незрелость паренхимы легкого, системы сурфактанта и антиоксидантной системы, токсическое воздействие высоких концентраций кислорода, инфекции (микоплазмы, пневмоцисты, уреаплазмы, хламидии, ЦМВ), отек легких различного генеза, легочная гипертензия, ГЭРХ, гиповитаминозы А и Е, генетическая склонность.
Морфологически бронхолегочная дисплазия проходит четыре стадии. На I стадии развивается классический РДС. На II стадии происходит деструкция эпителия альвеол и его последующая регенерация, формируются персистирующие гиалиновые мембраны. Также возникает отек интерстиция, некроз бронхиол. III стадия характеризуется образованием ограниченных эмфизематозных изменений, ателектазов и фиброза. На IV стадии в альвеолах накапливаются ретикулярные, эластические и коллагеновые волокна – окончательно формируются ателектазы, эмфизема, участки фиброза легкого.
Классификация бронхолегочной дисплазии
Согласно общепринятой классификации, существует две основные формы бронхолегочной дисплазии:
Также в отечественной педиатрии и неонатологии клинически выделяют три степени тяжести бронхолегочной дисплазии:
Симптомы бронхолегочной дисплазии
Специфических проявлений бронхолегочной дисплазии не существует. Заболевание характеризуется выраженной дыхательной недостаточностью на фоне высоких концентраций кислорода при ИВЛ. Общее состояние зависит от степени тяжести, однако, в большинстве случаев оно среднетяжелое или тяжелое. Грудная клетка приобретает характерный для эмфизематозных заболеваний вид: «бочкообразная форма» и горизонтальный ход ребер, увеличение размера в переднезаднем направлении, выпячивание межреберных промежутков и их втяжение при выдохе-вдохе. Также при бронхолегочной дисплазии возникает тахипноэ до 90-100 в 1 мин, наблюдается акро- или диффузный цианоз. При попытках перевести ИВЛ на более щадящий режим развивается острая недостаточность дыхательной системы, которая сопровождается выраженной гиперкапнией и гипоксемией. При прекращении респираторной поддержки на фоне спонтанного дыхания сохраняются признаки бронхиальной обструкции.
У детей с бронхолегочной дисплазией также отмечается пневмомедиастинум, эмфизема и пневмоторакс, брадикардия и приступы апноэ, рецидивирующие бронхиты и пневмонии, дефицитные состояния (дефицит витаминов D, А, Е, анемия), частая рвота, гастроэзофагеальный рефлюкс и аспирация пищевых масс. Нередко наблюдаются неврологические расстройства, поражения сетчатки. К основным осложнениям бронхолегочной дисплазии относятся правожелудочковая недостаточность и «легочное сердце», ограниченные или долевые ателектазы легких, рецидивирующие бронхиты, бронхиолиты и воспаления легких, хроническая дыхательная недостаточность, атопическая бронхиальная астма, артериальная гипертензия, анемия, задержка психофизического развития.
Диагностика
Диагностика бронхолегочной дисплазии включает в себя сбор анамнестических данных, объективный осмотр, лабораторные и инструментальные методы исследования. При сборе анамнеза неонатолог или педиатр обращает внимание на сроки, в которые произошли роды, наличие возможных этиологических и способствующих факторов. При объективном обследовании выявляются характерные клинические проявления бронхолегочной дисплазии: дыхательная недостаточность, деформация грудной клетки и т. д. В ОАК определяется нормохромная гипорегенераторная анемия, увеличение числа нейтрофилов и эозинофилов. В биохимическом анализе крови могут быть обнаружены гипокалиемия, гипонатриемия, гипохлоремия, уменьшение рН, повышение креатинина и мочевины. Одним из характерных признаков бронхолегочной дисплазии является низкое парциальное давление кислорода в крови (РаО2) – 40-55 мм.рт.ст.
Среди инструментальных методов диагностики при бронхолегочной дисплазии наиболее информативными считаются рентгенография ОГК, компьютерная и магнитно-резонансная томография. Чаще всего используется именно рентгенологический метод исследования, который позволяет выявить характерные признаки БЛД, определить степень тяжести и стадию морфологических изменений легких. КТ и МРТ дают возможность выявить аналогичные проявления и детально оценить структуру паренхимы легких. Однако они применяются не так часто в связи с отсутствием выраженных преимуществ перед рентгенографией и высокой стоимостью.
Лечение бронхолегочной дисплазии
Специфического лечения бронхолегочной дисплазии не существует. Основные терапевтические средства при данном заболевании включают в себя кислородную поддержку, рациональное питание, режим, симптоматические медикаментозные препараты. Несмотря на то, что ИВЛ – это основная причина развития БЛД, она является одним из наиболее важных аспектов лечения. Ее основная цель – поддержание показателей крови в допустимых пределах: рН крови на уровне 7,25, сатурация – 90% и более, парциальное давление крови – 55-70 мм.рт.ст.
Также важную роль в лечении бронхолегочной дисплазии играет питание ребенка. У больных детей имеется высокая метаболическая потребность на фоне необходимости адекватного роста легких. В таких условиях наиболее благоприятной считается суточная калорийность в пределах 115-150 ккал/кг/день. Суточный режим ребенка должен включать максимальный покой, многоразовое кормление, поддержание температуры тела на уровне 36,5 °C. Среди медикаментозных препаратов, которые могут применяться при БЛД, наиболее часто используются бронхолитики, муколитические и диуретические средства, глюкокортикостероиды, β2-агонисты, антибиотики и витамины А, Е.
Прогноз и профилактика бронхолегочной дисплазии
Прогноз при бронхолегочной дисплазии всегда серьезный. Показатель смертности в первые 3 месяца жизни колеблется в пределах 15-35%, за 12 месяцев – 10-25%. У выживших с возрастом происходит восстановление функции легких, однако морфологические изменения сохраняются в 50-75% случаев. У таких детей уже в дошкольном возрасте отмечается повышенная резистентность бронхиального дерева, после 7 лет появляется склонность к гиперреактивности. Адекватно проведенное лечение существенно снижает уровень летальности в первые 1-2 года, позволяет добиться клинического выздоровления до четырехлетнего возраста.
Профилактика бронхолегочной дисплазии подразумевает антенатальную охрану плода, предотвращение преждевременных родов, использование щадящих режимов ИВЛ и сведение длительности ее проведения к минимуму, витаминотерапию, использование препаратов сурфактанта. При угрозе преждевременного рождения ребенка показано введение матери глюкокортикостероидов с целью профилактики СДР и БЛД в дальнейшем.
БЛД, или бронхолегочная дисплазия – хроническое заболевание, которое развивается у недоношенных детей в связи с проведением искусственной вентиляции легких. В результате у ребенка происходит повреждение слаборазвитых бронхов и легких кислородом высокой концентрации, что проявляется стойкими обструктивными нарушениями.
Возникает вопрос: Почему недоношенный ребенок не может дышать сам и его необходимо подключать к аппарату искусственного вентилирования легких (ИВЛ)?
Мое мнение: акт дыхания безусловный и начинается с движения мышцы, которая называется диафрагмой, создающей в легких вакуум и туда, как в насос, под давлением поступает воздух. Объем поступающего воздуха зависит от того, могут ли межреберные мышцы растянуться полностью или нет.
У доношенных детей межреберные мышцы растягиваются полностью, альвеолы в легких полностью заполняются воздухом, слизь в них не скапливается.
У недоношенных детей межреберные мышцы полностью растянуться не могут, поэтому часть альвеол не заполняется воздухом.
Чтобы в этом убедиться, я посмотрел в электронный микроскоп на срез межреберной мышцы недоношенного ребенка, умершего от отека легких, возникшего от бронхолегочной дисплазии или БЛД.
В электронный микроскоп виден отек в межреберной мышце.
Пояснение к представленному выше фото:
Чтобы ребенок не умер от удушья, его подключают к аппарату искусственного дыхания.
Лечение бронхолегочной дисплазии у новорожденных без лекарств
Вы можете задать вполне объективный вопрос: “Почему у меня получается избавить недоношенного ребенка от бронхолегочной дисплазии?”. Я врач-миолог и подхожу к лечению БЛД с точки зрения специалиста по мышцам. Когда у ребенка после моего воздействия на мышцы методом Никонова проходят хрипы, перестают возникать бронхиты и он начинает восстанавливаться, тогда становиться понятна правильность моих объяснений.
Посмотрите, как уменьшается отек в межреберных мышцах у детей с бронхолегочной дисплазией во время воздействия на мышцы методом Никонова:
Это результат лечения новорожденного ребенка с бронхолегочной дисплазией воздействием на мышцы по методу Никонова с фиксацией проблемной мышцы.
Причины возникновения отека в межреберных мышцах
В данной части статьи я расскажу о причинах возникновения отека межреберных мышц у недоношенных детей с точки зрения знаний 21 века.
Профессор Kiyotoshi Sekiguchi, университет Осаки, Япония:
Примитивная (до 9 недель развития эмбриона) лимфатическая система перестает расти и не ветвиться из-за того, что белок-строитель полидом не вырабатывается эндотелиальными клетками и клетками мезенхимы.
Мышечные клетки растут, а лимфатические сосуды не растут.
Лимфа забирает отходы жизнедеятельности клеток и выводит их из организма ребенка. Но так как лимфатических сосудов становиться меньше по отношению к мышечным волокнам, то не все отходы выводятся лимфой. Так начинается отек в межреберных мышечных волокнах.
В незрелых легких недоношенных детей имеется дефицит сурфактанта – естественного поверхностного-активного вещества, которое препятствует слипанию альвеол на выдохе и необходимого для удаления слизи реснитчатым эпителием. Поверхностно-активное вещество начинает синтезироваться на 20-24 недели гестации, необходимый уровень сурфактанта достигается к 35-36 неделе.
Неврологи отмечают, что БЛД, т.е. бронхолегочная дисплазия, имеет ятрогении.
Искусственная вентиляция легких особенно в жестких режимах приводит к баротравме бронхиальной и легочной тканей, про этом токсическое действие высоких концентраций кислорода вдыхаемой смеси также приводит к повреждению эпителия, развитию отека легочной ткани и пропитыванию ее белком. В результате оба фактора приводят к снижению растяжимости альвеол.
Мое мнение: у недоношенного ребенка с одной стороны не растягиваются межреберные мышцы, а с другой стороны большая концентрация кислорода сжигает слизистую внутри альвеол. Как только ребенку перестают давать кислород, развивается инфекция в альвеолах в сожженных кислородом местах.
Стадии БЛД
Заключение по результатам патологоанатомических исследований легочной ткани и альвеол у умерших от пневмонии недоношенных детей, которая началась после отстранения ребенка от дыхания кислородом, позволили установить стадии развития БЛД.
Различают 4 стадии формирования диагноза бронхолегочная дисплазия:
В 4 стадии особенно сильно наблюдается гипертрофия мышечного слоя бронхиол, уменьшение количества легочных артериол с гипертрофией мышечного слоя артериол и венул.
Неонатологи лечат недоношенных детей с диагнозом бронхолегочная дисплазия симптоматически: продолжают кислородотерапию.
Мое мнение: неонатологи еще больше сжигают слизистую альвеол. Они применяют бронхолитики, диуретики, глюкокортикостероиды, антиоксиданты и антибиотики.
В острый период при тяжелой степени БЛД, когда стоит вопрос жизни, назначения оправданы. После устранения воспалительного процесса назначение лекарств не решит проблему отека межреберных мышц.
Существует один способ устранения отека из межреберных мышц – воздействие на мышцы по методу Никонова с фиксацией проблемной мышцы.
Последствия и осложнения при бронхолегочной дисплазии
Преимущественное число детей, перенесших на ранних сроках жизни БЛД, страдают нарушениями дыхательной функции в старшем возрасте, при достижении подросткового возраста. Проявлениями нарушений дыхания являются следующие симптомы:
Все это приводит к следующим заболеваниям:
Описанные сочетания бронхолегочной дисплазии с синдромом крупа, врожденными пороками развития легких, трансформация в хронический бронхиолит с облитерацией (ХбсО), бронхиальную астму, рецидивирующий обструктивный бронхит (РОБ).
Бронхолегочная дисплазия, возникшая в перинатальном периоде
Общая информация
Краткое описание
Бронхолегочная дисплазия, возникшая в перинатальном периоде –хроническое заболевание легких преимущественно недоношенных детей, характеризующееся повреждением всех структурных компонентов легкого и формирующееся в процессе комбинированного воздействия первичного респираторного заболевания и интенсивной терапии дыхательных расстройств на незрелые легкие, с основными проявлениями в виде дыхательной недостаточности и сохраняющейся зависимости от кислорода более 28 дней жизни в сочетании с патологическими изменениями на рентгенограмме легких [1].
Название протокола: Бронхолегочная дисплазия, возникшая в перинатальном периоде
Код протокола:
Код (ы) МКБ-10:
P27.1– Бронхолегочная дисплазия, возникшая в перинатальном периоде
Сокращения, используемые в протоколе:
Дата разработки протокола: 2015 год.
Категория пациентов: новорожденные, дети раннего возраста от 0 до 2-х месяцев.
Пользователи протокола: неонатологи, реаниматологи,пульмонологи, педиатры, врачи общей практики.
Оценка на степень доказательности приводимых рекомендаций.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с не высоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию. |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+). Результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++или+), результаты которых не могут быть непосредственно распространены на соответствующую популяцию. |
| D | Описание серии случаев или неконтролируемое исследование, или мнение экспертов. |
| GPP | Наилучшая фармацевтическая практика. |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
| Степень тяжести БЛД | Диагностические критерии, определяющие БЛД | |
| Гестационный возраст | ||
| ˂ 32 недель | ≥32 недель | |
| Время и условия оценки | ||
| С 36 недель постконцептуального периода, до выписки домой при первичном поступлении | С 28 до 56 дней постнатального периода до выписки домой при первичном поступлении | |
| Оксигенотерапия > 21% более 28 дней* | ||
| Легкая БЛД | Дыхание комнатным воздухом до 36 недель постконцептуального периода, при первичной выписке | Дыхание комнатным воздухом до 56 дней постнатального периода при первичной выписке |
| Среднетяжелая БЛД | Потребность в кислороде ˂ 30% до 36 недель постконцептуального периода при первичной выписке | Потребность в кислороде ˂ 30% до 56 дней постнатального периода при первичной выписке |
| Тяжелая БЛД | Потребность в кислороде ≥30% и/или РРV, NCPAP до 36 недель постконцептуального периода, при первичной выписке | Потребность в кислороде ≥30% и/или РРV, NCPAP до 56 дней постнатального периода, при первичной выписке |
Примечание: *за 1 сутки лечения принимают кислородотерапию, продолжающуюся не менее 12 час. **PPV (positivepressureventilation) ─ вентиляция под положительным давлением. *** NCPAP (nosecontinuouspositiveairwaypressure) – положительное давление в дыхательных путях через носовые канюли.
Диагностика
II. МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ
Перечень основных и дополнительных диагностических мероприятий
Основные (обязательные) диагностические обследования, проводимые на стационарном уровне:
Диагностические мероприятия, проводимые на этапе скорой неотложной помощи: нет.
Диагностические критерии
Жалобы, анамнез:
Доминирующие факторы риска развития БЛД:
Примечание:
* Число задних отрезков ребер выше диафрагмы билатерально.
** Фокальные области линейной или узловой плотности в пределах зоны (1/2 легкого с каждой стороны).
***Прозрачные интрапаренхиматозные поражения с четким контуром.
Дифференциальный диагноз
Дифференциальный диагноз [1,2,3,4,5,6]
В таблице 3 приведены основные клинические дифференциально-диагностические критерии БЛД.
Таблица 3. Дифференциальная диагностика БЛД у новорожденных
Продолжение таблицы 3
Лечение
Тактика лечения:
После установления диагноза БЛД медицинская помощь оказывается на следующих этапах:
I этап – ОРИТ новорожденных: применение профилактических и терапевтических мероприятийнаправленных на сокращение длительности ИВЛ и кислородозависимости.
II этап– Выхаживание:
1) Отлучение ребенка от кислорода под контролем газов крови;
2) Ингаляционная терапия: бронхолитическая и/или ИКГС.
III этап – Амбулаторный: врач пульмонолог –определяет индивидуальную тактику ведения и ингаляционную терапию в зависимости от степени тяжести БЛД и проведения профилактики РСВ
IV этап – Стационарный: пульмонологическое отделение многопрофильной детской больницы – терапия обострения БЛД и коррекцией сопутствующих заболеваний.
Немедикаментозное лечение:
Медикаментозное лечение
Медикаментозное лечение, оказываемое на этапе скорой неотложной помощи:
Небулайзерная терапия ингаляционными бронхолитиками: беродуал 1 капля на кг массы тела растворяется в 1,5 – 2,0 мл 0,9% раствор натрия хлорида, или доза 75-175мкг однократно[44] (УД-C).
Медикаментозное лечение, оказываемое на стационарном уровне:
Терапия обострения БЛД зависит от ведущего клинического синдрома.
Кофеин в/в 20-25 мг/кг – в первые сутки жизни (доза насыщения), 5-10мг/кг – поддерживающая доза (при частоте сердечных сокращений более 180 уд/мин снизить поддерживающую дозу кофеина с 10 до 5 мг/кг, при сохраняющейся тахикардии отменить его). Кофеин отменяют полностью при достижении пациентом ПКВ 33-35 недель при отсутствии апноэ.
Системные глюкокортикостероиды [18,35,38] (УД-А).
Новорожденным с ОНМТ и ЭНМТ в возрасте более 7 суток жизни, находящимся на ИВЛ более 7 суток дексаметазон в/в: 0,15 мг/кг в сутки – с 1 по 3 день; 0,1 мг/кг в сутки – с 4 по 6 день; 0,05 мг/кг в сутки – с 7 по 8 сутки; 0,02 мг/кг в сутки – с 9-10–е сутки. Курс – 10 дней.
Ингаляционные бронхолитики включают β2-агонисты (сальбутамол), антихолинергетики (ипратропия бромид) Небулайзерная терапия: ипратропия бромид 1 капля на кг массы тела растворяется в 1,5 – 2,0 мл 0,9% раствор натрия хлорида или доза 75-175мкг каждые 6-8 часов. Курс лечения– до 2-х недель и больше[44] (УД-C).
Диуретики. Фуросемид раствор 1%-1,0 в дозе 0,5-1,0 мг/кг 1-2 раза в сутки в/в. Курс лечения – 7 дней.
Медикаментозное лечение, оказываемое на амбулаторном уровне:
Небулайзерная терапия ингаляционными бронхолитиками вне обострения: будесонида раствор для ингаляций небулы по 2мл; 1мл – 500мкг или 250мкг. Доза 400- 500 мкг/сут (1 мл или 20 капель) через компрессионный небулайзер. Курс лечения – до 2-х недель и больше по показаниям.
Индикаторы эффективности лечения:
Препарат «Паливизумаб», по 50 или 100мг, лиофилизат для приготовления раствора 100мг/мл. Представляет собой гуманизированные моноклональные антитела класса G, специфичные к белку с выраженным ингибирующим действием на штаммы РСВ. Вводится препарат внутримышечно, предпочтительно в наружную боковую область бедра в стандартных асептических условиях. Разовая доза препарата составляет 15 мг/кг массы тела. Схема применения состоит из 5 инъекций препарата, проводимых с интервалом 1 месяц в течение сезонного подъема заболеваемости, вызываемой RSV (с октября–декабря до марта–апреля). Предпочтительно, чтобы первая инъекция была произведена до начала подъема заболеваемости.
Питание— улучшение состояния детей с БЛД происходит по мере роста и развития легких. Достаточные темпы роста обеспечиваются повышенной калорийностью питания и достаточным содержанием белка (140 ккал/кг/сут.). До достижения массы тела 2500–3000 г рекомендуется калорийность питания не менее 130 ккал/кг/сут. Предпочтительно питание грудным молоком с «усилителями», при его отсутствии используют смеси для недоношенных детей.
Дальнейшее ведение
Диспансерный учет по месту жительства у пульмонолога (табл.4).
Таблица 4 – Частота осмотров пульмонологом детей с БЛД
| Тяжесть БЛД | Возраст | |
| до 1 года | до 3 лет | |
| Легкая | 1 раз в 3–6 мес | по необходимости |
| Среднетяжелая/тяжелая | ежемесячно | 1 раз в 3–6 мес |
Препараты (действующие вещества), применяющиеся при лечении
| Будесонид (Budesonide) |
| Дексаметазон (Dexamethasone) |
| Ипратропия бромид (Ipratropium bromide) |
| Кофеин (Caffeine) |
| Натрия хлорид (Sodium chloride) |
| Паливизумаб (Palivizumab) |
| Сальбутамол (Salbutamol) |
| Фенотерол (Fenoterol) |
| Фуросемид (Furosemide) |
Госпитализация
Показания для госпитализации с указанием типа госпитализации
Показания к экстренной госпитализации в родовспомогательное учреждение 3 уровня регионализации (согласно приказу МЗ по регионализации перинатальной помощи):
Информация
Источники и литература
Информация
III. ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ВНЕДРЕНИЯ ПРОТОКОЛА
Список разработчиков протокола:
Конфликт интересов: отсутствует.
Рецензенты:
Абдрахманова Сагира Токсанбаенва – доктор медицинских наук, профессор, АО «Медицинский университет Астана», заведующая кафедрой детских болезней №2.
Условия пересмотра протокола: пересмотр протокола через 3 года после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.