Билиарный холангит что это
Билиарный холангит что это
Первичный билиарный холангит (более привычное для нас название — первичный билиарный цирроз) представляет собой иммуноопосредованное холестатическое заболевание печени, характеризующееся негнойным воспалением и прогрессирующим разрушением внутрипеченочных желчных протоков малого и среднего размера, которое в конечном итоге прогрессирует до развития терминальной стадии цирроза.
Дебаты вокруг термина
Эпидемиология
Этиопатогенез
Патогенез РВС остается неизвестным. Точная причина развития болезни, лежащая в основе повреждения внутрипеченочных желчных эпителиальных клеток, приводящая к холестазу, фиброзу и билиарному циррозу, остается неясной, но, скорее всего, является многофакторной, включая генетическую предрасположенность и триггерное воздействие факторов окружающей среды. Различные исследования постоянно находят связь между РВС и инфекциями мочевыводящих путей, вызываемыми E.coli. Другая бактерия, которая может быть вовлечена в этиологию РВС посредством перекрестной реактивности, — Novosphingobium aromaticivorans. Исследования «случай — контроль» с анализом различных факторов образа жизни пациентов с РВС показали связь повышенной восприимчивости к РВС с химическими веществами, широко распространенными в повседневной жизни, такими как лак для ногтей, краска для волос, курение, токсические отходы.
Клиника
При кожном зуде используется рифампицин, при его неэффективности — сертралин, который международные эксперты рекомендуют как средство первой линии, несмотря на некоторые недостатки. Кроме того, назначается холестирамин.
Холангит: причины, симптомы, лечение
Содержание
Исходным пунктом отправления желчи служит место ее образования — клетки печени. Конечным — двенадцатиперстная кишка, где желчь и осуществляет свою основную работу. Между ними — транспортные магистрали разной протяженности и калибра, проходящие как внутри, так и вне печени. Называются они — желчные протоки или сосуды. На древнегреческом «χολή» — жёлчь и «ἀγγεῖον» — сосуд. Отсюда и принятое наименование их воспаления — холангит.
Причины холангита
В роли главного предрасполагающего фактора часто выступает застой желчи. В роли пускового механизма — инфекция (преимущественно, бактериальная). Застой становится следствием закупорки желчных путей камнями, сдавлением опухолью, рубцовыми изменениями стенок сосудов, дискинезии, стеноза фатерова сосочка, воспалительных процессов в близлежащих органах и др. Реже в роли причинного фактора воспаления желчных магистралей выступают гельминты, аутоиммунные реакции, попадание в протоки секрета поджелудочной железы.
Холангит редко выступает в качестве самостоятельной патологии. Чаще он сопровождает и/или сопровождается нарушениями со стороны других органов желудочно-кишечного тракта.
Симптомы (признаки) холангита
Острый холангит
Начало внезапное, ярко выраженное. Первые признаки не специфичны только для холангита:
Со временем добавляются новые признаки:
При агрессивном течении холангита состояние продолжает ухудшаться и характеризуется:
Гнойный холангит
Разновидность острого. Название отражает тяжесть и характер воспаления и сопутствующих органических изменений.
Симптомы аналогичны вышеперечисленным. Течение тяжелое с прогрессирующей интоксикацией и признаками поражения нервной системы. Часты осложнения, угрожающие жизни пациента (перитонит, эмпиема плевры, абсцесс и др.).
Билиарный холангит
Редкая форма деструктивного воспалительного поражения всех желчных магистралей, причина которого до конца не ясна. Название происходит от латинского термина «bilis», обозначающего желчь.
Коварство данного недуга заключается в отсутствии ранних симптомов. Желчные протоки постепенно разрушаются, замещаясь соединительной тканью. Настораживающие признаки очень неспецифичны (слабость, боль в правом подреберье, чувство тяжести в желудке и др.) В острой фазе клинические проявления аналогичны описанным выше.
Первичный билиарный холангит относят к воспалительным патологиям протоков аутоиммунного характера.
Хронический холангит
В период обострения характерны «острые» симптомы. В целом характеризуется стертыми, но неуклонно прогрессирующими симптомами. Основные — боль или дискомфорт справа под ребрами, незначительно повышенная температура, слабость, тенденция к увеличению печени, слабо выраженная желтушность склер, возможен кожный зуд. Со временем возможно присоединение симптома «барабанных палочек» (утолщение концевых фаланг), свидетельствующего о склеротических изменениях, которые могут вылиться в цирроз печени.
Лечение холангита
Направлено на устранение причин и следствий воспалительного поражения желчных путей. Ликвидация причин, ведущих к застою желчи, иногда осуществляется хирургическими методами. Большую роль играет своевременное купирование болевого синдрома, детоксикационные мероприятия, противовоспалительная терапия.
В острой фазе важен голод и покой. Вне обострений — диета, посильная физическая нагрузка, лечение сопутствующих патологий.
Лечении пациентов с хроническим холециститом возможно методами традиционной медицины: фитотерапией, гомеопатией, остеопатией, иглотерапией, цигун-терапией.
Первичный билиарный холангит/цирроз печени: руководящие принципы лечения
Резюме. Практические рекомендации для врачей, медицинских сестер и пациентов
Первичный билиарный холангит/цирроз

Терапия при первичном билиарном холангите включает урсодезоксихолевую кислоту и обетихолевую кислоту наряду с экспериментальными и ранее одобренными фармацевтическими средствами. Лечение ориентировано на применении урсодезоксихолевой кислоты и стратификации риска на основе исходных и терапевтических факторов, включая ответ на лечение. При непереносимости урсодезоксихолевой кислоты или высоком риске заболевания, о чем свидетельствует неэффективность лечения с применением урсодезоксихолевой кислоты (обычно проявляющаяся повышением уровня щелочной фосфатазы >1,67 × верхнюю границу нормы и/или повышением концентрации билирубина в крови), возможна терапия второй линии, включающая обетихолевую кислоту.
В марте 2018 г. в журнале «Gut» опубликованы новые руководящие принципы лечения и подробные рекомендации по ведению пациентов с первичным билиарным холангитом, разработанные Британским обществом гастроэнтерологов (British Society of Gastroenterology), Великобритания. Руководящие принципы подготовлены с использованием систематического обзора публикаций в базах данных PubMed, Medline и Cochrane. При составлении рекомендаций использована классификация оценки, разработки и анализа GRADE, в соответствии с которой они подразделены на сильные и слабые с уровнем доказательности от высокого до умеренного, низкого и очень низкого. Данные будут полезны для врачей, медсестер и самих пациентов, хотя преимущественно ориентированы на гастроэнтерологов и гепатологов.
Характеристиками первичного билиарного холангита являются устойчивое повышение (продолжительностью более 6 мес) уровня щелочной фосфатазы в сыворотке крови, довольно часто наличие гранулематозного воспаления портальных трактов, сопутствующим лимфоцитарно опосредованным повреждением (и деструкцией) мелких внутрипеченочных желчных протоков, холестазом и типичным набором сывороточных и секреторных аутоантител. У большинства пациентов описанное состояние прогрессирует с развитием билиарного фиброза и, в конечном счете — цирроза. Скорость цирротических изменений вариабельна и поддается модификации путем применения урсодезоксихолевой кислоты.
Эпидемиология
Первичный билиарный холангит соответствует критериям редких заболеваний (распространенность менее 50 на 100 тыс. населения) во всех изученных популяциях. Осведомленность об этой патологии коррелирует с распространенностью, показатель которой обычно стабилизируется после нескольких лет роста. Заболеваемость характеризуется асимметричностью с более высокими показателями среди женщин (в 10 раз выше, чем среди мужчин). Первичный билиарный холангит чаще наблюдается у пациентов пожилого возраста (средний возраст выявления заболевания — 65 лет). Самый молодой пациент с зарегистрированным первичным билиарным холангитом — девочка в возрасте 15 лет. Существуют потенциально важные различия в клиническом проявлении первичного билиарного холангита между мужчинами и женщинами и между пациентами пожилого и более молодого возраста, хотя базовый подход к управлению одинаков во всех демографических группах. Семейная история первичного билиарного холангита характерна для прочих аутоиммунных процессов. Более половины пациентов имеют еще одно аутоиммунное состояние (целиакию, склеродермию, заболевание щитовидной железы, синдром Шегрена и др.), что отражает общую генетическую предрасположенность.
Этиология
Первичный билиарный холангит этиологически является иммуноопосредованным повреждением билиарных путей в результате взаимодействия иммуногенетических и экологических триггеров с наличием точек кластеризации болезни. Подтвержденными факторами риска являются курение и рецидивирующие инфекции мочевыводящих путей. Холестаз и/или зуд в период предыдущей беременности также связан с повышением риска развития первичного билиарного холангита. Необходимо документировать рецидивирующие инфекции мочевыводящих путей и связанные с беременностью холестазы, а также рекомендовать прекращение курения, учитывая его прямую взаимосвязь с прогрессированием заболевания.
Диагностика
Диагностическая точность сочетания холестатических сывороточных тестов и специфических серологических маркеров достигает >95% по своей чувствительности и специфичности, поэтому анализ крови лежит в основе диагностики первичного билиарного холангита. Подозрение на первичный билиарный холангит справедливо по отношению к пациентам с иначе необъяснимым повторным повышением щелочной фосфатазы в сыворотке крови, а также гамма-глутамилтрансферазы.
Во всех подобных случаях следует проверять наличие аутоантител с помощью теста ELISA в соответствии с местной практикой, что является достаточным для подтверждения диагноза у большинства пациентов без применения биопсии. При подозрении на альтернативное аутоиммунное заболевание тест ELISA может обладать большей чувствительностью и менее подвержен неспецифичной реактивности, возникающей в результате высокого титра поликлональных иммуноглобулинов IgM, наблюдаемого при первичном билиарном холангите. Наличие специфических антинуклеарных или антицентромерных антител чаще всего бывает достаточным для диагностики серонегативного первичного билиарного холангита, однако достоверно о наличии серонегативного заболевания можно судить лишь при наличии материалов биопсии.
Учитывая доброкачественный прогноз при наличии антимитохондриальных антител и нормальных результатов печеночных проб, для таких пациентов не рекомендуется ни биопсия, ни применение урсодезоксихолевой кислоты. Однако рекомендуется ежегодно на первичном медико-санитарном уровне проводить повторные печеночные пробы.
Нет никаких доказательств того, что концентрация антимитохондриальных антител, превышающая диагностический порог, имеет какое-либо прогностическое значение. Поэтому после установления четкого диагноза повторное измерение не рекомендуется. Кроме того, титр аутоантител может снижаться под влиянием урсодезоксихолевой кислоты. Иммунофлуоресцентный метод, также используемый для диагностики первичного билиарного холангита, позволяет выявить тонкие вариации специфичности аутоантител.
Роль визуализации в диагностике первичного билиарного холангита в значительной степени исключает альтернативные диагнозы. Для большинства пациентов достаточно скрининга ультразвуковой визуализации. Особое внимание уделяется исключению первичного склерозирующего холангита и похожих на него заболеваний у пациентов с серонегативным холангитом при помощи магнитно-резонансной холангиопанкреатографии. Наличие желчных камней у пациентов с первичным билиарным холангитом довольно часто является потенциальной причиной задержки диагностики. На терминальной стадии первичного билиарного холангита визуализация цирротических осложнений выполняется так же, как при циррозе печени любой другой этиологии.
Гистологические особенности
Адекватность любой биопсии обусловлена клинической задачей, но в целом биопсийный материал печени должен иметь достаточный объем для визуализации паренхимы и количества портальных трактов (предлагается более 11). Картина первичного билиарного холангита включает деструктивный гранулематозный лимфоцитарный холангит, ведущий к прогрессирующей потере желчных протоков, а также хроническому холестазу, фиброзу и циррозу. Другие видимые особенности включают лимфоцитарную активность, паренхиматозное некротизирующее воспаление и узловатую регенеративную гиперплазию. Точные критерии прогностической биопсии печени при первичном билиарном холангите еще предстоит установить, равно как и роль конкретных систем оценки.
Биопсия периферических лимфатических узлов, увеличение которых довольно часто отмечают при первичном билиарном холангите (и вообще при заболеваниях печени), обычно выявляет наличие реактивно-воспалительных изменений, которые предположительно являются частью основного патологического процесса.
Дифференциальная диагностика
Определение диагноза первичного билиарного холангита обычно вызывает небольшую путаницу из-за специфичности и чувствительности аутоантител. Следует проявлять осторожность при серонегативном типе холангита, для которого основным дифференцируемым заболеванием является первичный склерозирующий холангит. Другие возможные диагнозы включают саркоидоз, болезнь трансплантата против хозяина, идиопатическое нарушение кровообращения, вызванное лекарственным повреждением печени, и варианты генетических холестатических синдромов. Также следует осторожно интерпретировать низкий титр антимитохондриальных антител из-за возможности ложной позитивности аутоантител при воспалительных состояниях, в частности неалкогольной жировой болезни печени.
Сопутствующие заболевания
Первичный билиарный холангит в основном ассоциирован с другими аутоиммунными состояниями, отражающими общую иммуногенетическую восприимчивость (наиболее сильная ассоциация с синдромом Шегрена). У пациентов с выраженной слабостью следует учитывать наличие заболеваний щитовидной железы (присутствует у 25% пациентов) или анемии с иммунной/аутоиммунной этиологией (включая пернициозную анемию, аутоиммунную гемолитическую анемию и целиакию).
Остеопороз также часто отмечают при первичном билиарном холангите, хотя его правильнее рассматривать в качестве осложнения метаболических изменений, наблюдаемых при холестазе, включая снижение абсорбции жирорастворимых витаминов.
До сих пор не установлено, связаны ли повторные инфекции мочевыводящих путей при первичном билиарном холангите с основным заболеванием или агрессивное лечение инфекции мочевыводящих путей оказывает влияние на естественную историю первичного билиарного холангита. Однако рецидивирующие инфекции мочевыводящих путей являются потенциальной причиной снижения качества жизни.
Руководящие принципы
Наличие у пациента антимитохондриальных или специфических антиядерных антител в титре 1:40 или выше (при соответствующих признаках холестаза по биохимическим показателям и отсутствии альтернативного объяснения) обычно является достаточным основанием для установления диагноза первичного билиарного холангита (сильные рекомендации с высоким уровнем доказательности).
Все пациенты с первичным билиарным холангитом нуждаются в пожизненном наблюдении, причем различное течение болезни у разных пациентов может потребовать различной интенсивности наблюдения (сильные рекомендации, умеренный уровень доказательности).
Оценка риска должна учитывать тяжесть заболевания и его активность в начальном и последующих этапах, молодой возраст наступления болезни (младше 45 лет) и мужской пол. При этом рекомендуется комплексное исследование: печеночные пробы, ультразвуковая визуализация для выявления открытого цирроза и спленомегалии, переходная эластография (сильная рекомендация, умеренный уровень доказательности).
Выявление пациентов с наибольшим риском прогрессирования заболевания осуществляется на основании показателей биохимического анализа после одного года терапии с применением урсодезоксихолевой кислоты (сильная рекомендация, высокий уровень доказательности).
Подписывайтесь на наш Telegram-канал, Viber-сообщество, Instagram, страничку Facebook, а также Twitter, чтобы первыми получать самые свежие и актуальные новости из мира медицины.
Первичный билиарный холангит в эпоху урсодезоксихолевой кислоты: достижения и проблемы терапии
Цель обзора: обобщить текущие знания об этиопатогенезе и клинические особенности первичного билиарного холангита (ПБХ), осветить актуальные вопросы диагностики, лечения и стратификации рисков у пациентов с ПБХ.
Основные положения. ПБХ (ранее — первичный билиарный цирроз) — хроническое воспалительное аутоиммунное заболевание, при котором первоначально поражаются холангиоциты междольковых желчных протоков. ПБХ наблюдается в первую очередь у женщин среднего возраста. Без лечения ПБХ обычно прогрессирует до цирроза печени и печеночной недостаточности. Инициация и прогрессирование ПБХ — многофакторный процесс с влиянием на генетический, эпигенетический, иммунологический статус пациента различных факторов окружающей среды. Ранняя диагностика ПБХ значительно улучшилась благодаря выявлению классических серологических маркеров — антимитохондриальных антител. В 1980-х годах ПБХ был ведущим показанием для трансплантации печени.
Урсодезоксихолевая кислота (УДХК) в настоящее время является препаратом первой линии, большинство пациентов с ПБХ на фоне терапии имеют нормальную продолжительность жизни. Однако 1 из 3 пациентов не отвечает на лечение УДХК, поэтому клинически важна оценка биохимического ответа через год от начала терапии.
Заключение. Ранняя диагностика и стратификация пациентов с ПБХ низкого и высокого риска резистентности к терапии УДХК имеют большое клиническое значение для индивидуального подхода к лечению и определения необходимости дополнительной медикаментозной терапии.
Авторы заявляют об отсутствии возможных конфликтов интересов.
Абсандзе Кетован Гелаевна — аспирант научно-исследовательского отдела гепатологии ГБУЗ «МКНЦ им. А.С. Логинова ДЗМ». 111123, г. Москва, шоссе Энтузиастов, д. 86. E-mail: e.vinnitskaya@mknc.ru
Архипова Елена Владимировна — клинический ординатор ГБУЗ «МКНЦ им. А.С. Логинова ДЗМ». 111123, г. Москва, шоссе Энтузиастов, д. 86. E-mail: e.vinnitskaya@mknc.ru
Винницкая Елена Владимировна — д. м. н., руководитель научно-исследовательского отдела гепатологии ГБУЗ «МКНЦ им. А.С. Логинова ДЗМ». 111123, г. Москва, шоссе Энтузиастов, д. 86. E-mail: e.vinnitskaya@mknc.ru
Иванов Антон Николаевич — студент лечебного факультета 5-го курса ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Минздрава России. 119991, г. Москва, ул. Трубецкая, д. 8, стр. 2. E-mail: anton-ivanov96@yandex.ru
Сандлер Юлия Григорьевна — к. м. н., старший научный сотрудник научно-исследовательского отдела гепатологии ГБУЗ «МКНЦ им. А.С. Логинова ДЗМ». 111123, г. Москва, шоссе Энтузиастов, д. 86. eLIBRARY.RU SPIN: 2508-8056. E-mail: y.sandler@mknc.ru
Сбикина Евгения Сергеевна — младший научный сотрудник научно-исследовательского отдела гепатологии ГБУЗ «МКНЦ им. А.С. Логинова ДЗМ». 111123, г. Москва, шоссе Энтузиастов, д. 86. E-mail: esbikina@gmail.com
Первичный билиарный холангит (ПБХ) — хроническое, медленно прогрессирующее холестатическое заболевание печени аутоиммунной природы, характеризующееся негнойным деструктивным холангитом с поражением в первую очередь внутридольковых и септальных желчных протоков, приводящее при естественном течении к билиарному циррозу печени.
Одним из самых ранних упоминаний о билиарном циррозе принято считать наблюдение итальянского врача и патологоанатома Джованни Морганьи в 1761 г., описавшего плотную зеленую печень при длительно протекавшей многолетней желтухе. В 1851 г. английские врачи T. Аддисон and В. Галл впервые описали 5 случаев болезни, клинически проявлявшейся ксантомами и ксантелазмами, и сделали выводы о причастности печени к развитию заболевания, обозначив синдром как необструктивный билиарный цирроз, позднее он получил название синдрома Аддисона — Галла [1].
В дальнейшем предлагались различные номенклатурные названия, такие как гипертрофический цирроз печени с хронической желтухой [2], подострый холангит [3], интерстициальный хронический гепатит с гипертрофией печени, холангиолитический гепатит и цирроз, ксантоматозный билиарный цирроз [4], перихолангиолитический билиарный цирроз, хронический негнойный деструктивный холангит [5].
Спустя столетие, в 1950 г., был принят к широкому применению термин «первичный билиарный цирроз», предложенный Е.Х. Ареном и соавт. [6].
Уже в 1959 г. Шейла Шерлок выступала против этого термина, поскольку у многих пациентов не было цирроза [7].
К середине 1960-х гг. сформировались теории об участии иммунной системы в развитии заболевания. В дальнейшем серия работ Д. Дониак, Ш. Шерлок и соавт. позволила утвердить идею аутоиммунных реакций как важных звеньев патогенеза; начался поиск специфических антител [8, 9].
В 1967 г. была доказана роль антимитохондриальных антител (АМА) [10], позднее, в 1988 г., выявлены АМА М2, а в 1989 г. — субтипы Е2 [11].
Прогноз выживаемости пациентов значительно улучшился после того, как в 80-х годах прошлого столетия начали применять урсодезоксихолевую кислоту (УДХК). Термин «первичный билиарный цирроз» постоянно подвергался критике в связи с неточностью и неправильным отражением сути, предпринимались попытки его переосмысления [5].
Предложение о смене названия первичного билиарного цирроза на первичный билиарный холангит было одобрено Советом управляющих Европейской ассоциацией по изучению болезней печени в ноябре 2014 г., Советом управляющих Американской ассоциацией по изучению печени в апреле 2015 г. и Советом управляющих Американской гастроэнтерологической ассоциации в июле 2015 г.
РАСПРОСТРАНЕННОСТЬ И ЗАБОЛЕВАЕМОСТЬ
В последние годы отмечается тенденция к увеличению заболеваемости и распространенности ПБХ 13. Вероятно, этот рост вызван повышением точности диагностики, появлением новых методов лабораторного скрининга, формированием больших баз данных благодаря развитости системы здравоохранения некоторых стран и доступности медицинского обслуживания в отдельных регионах.
По данным многочисленных исследований, ПБХ встречается преимущественно среди женщин. Результаты исследований показывают, что по всему миру примерно 1 из 1000 женщин старше 40 лет имеет ПБХ [12]. Соотношение женщин и мужчин варьируется, в среднем оно составляет 10 : 1. Распространенность и заболеваемость ПБХ имеют неравномерное распределение по всему миру. Заболеваемость ПБХ колеблется от 0,33 до 5,8 на 100 000 жителей в год, а коэффициент распространенности варьирует от 1,91 до 40,2 на 100 000 жителей [13]. Среди населения стран Европы средняя заболеваемость ПБХ составляет 1-2 на 100 000 человек в год, в странах Азии более низкие показатели заболеваемости и распространенности, чем в западных странах 17.
Данные по распространенности и заболеваемости ПБХ в Российской Федерации в настоящий момент отсутствуют.
Следует отметить, что эпидемиологические исследования могут представлять собой только верхушку айсберга, поскольку имеются сведения, что АМА-позитивные люди без заболевания печени встречаются в два раза чаще, чем АМА-позитивные с заболеванием печени [16].
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
ПБХ считается многофакторным заболеванием. В последнее время ведущую роль в возникновении ПБХ отводят взаимодействию генетических и эпигенетических факторов риска с экологическими триггерами, приводящему к иммуноопосредованному повреждению желчных протоков с последующим развитием холестаза, дуктопении. Все это в итоге вызывает фиброз и цирроз печени.
В пользу аутоиммунного генеза ПБХ свидетельствует ряд фактов. Основной комплекс гистосовместимости человека HLA вовлечен в патогенетические механизмы ПБХ, как и при многих других аутоиммунных заболеваниях. Для классических генов HLA наиболее сильная связь выявлена с DRB*08 [17]. Широкомасштабные исследования генома (GWAS) ПБХ находят самую сильную связь с однонуклеотидными полиморфизмами (SNP) в области HLA [18].
ПБХ часто сочетается с другими аутоиммунными заболеваниями, включая синдром Шегрена и хронический тиреоидит [19, 20]; специфические AMA обнаруживаются в сыворотке более 90% пациентов с ПБХ и почти не выявляются у лиц без ПБХ [21, 22]. Кроме того, эпидемиологические данные указывают на увеличение распространенности ПБХ среди родственников первой линии, а также братьев и сестер. Индекс конкордантности у монозиготных близнецов составляет 63% — он один из самых высоких среди таковых у прочих аутоиммунных заболеваний [23]. Наконец, при гистологическом исследовании плотные инфильтраты, состоящие из Т- и В-лимфоцитов, обнаруживаются вблизи пораженных внутрипеченочных желчных протоков [24].
Однако последние исследования выявили специфические генетически опосредованные предпосылки развития ПБХ. Как выяснилось, взаимодействие между генетикой и факторами окружающей среды является более сложным, чем казалось раньше. Например, были найдены специфические экологические факторы, которые могут приводить к потере толерантности к пируватдегидрогеназному комплексу (ПДК-Е2). Они представляют собой ксенобиотики, которые могут либо имитировать, либо модифицировать липоевую кислоту. К ним относятся 2-октиновая кислота и 6,8-бис-ацетилтиооктановая кислота (метаболит ацетаминофена), часто используемые при производстве косметики. AMA-положительная сыворотка от пациентов с ПБХ выражено перекрестно реагирует с этими ксенобиотиками [25, 26].
Патогенетические механизмы ПБХ в настоящий момент остаются не полностью изученными. ПБХ является хроническим холестатическим аутоиммунным заболеванием, поражающим эпителиальные клетки внутрипеченочных желчных протоков. Его «визитная карточка» — выявляемые в крови специфичные АМА, а также характерная гистологическая картина поражения желчных протоков [27].
Морфологически ПБХ характеризуется как хронический деструктивный холангит с образованием гранулем в печени, а дегенерация и некроз холангиоцитов вызывают деструктивные изменения и приводят к исчезновению внутрипеченочных желчных протоков малого или среднего размера [28].
AMA представляют собой специфические для данной патологии аутоантитела, обнаруживающиеся среди всех трех классов иммуноглобулинов, синтезирующиеся плазмоцитами, которые могут проходить через эпителий желчных протоков и нарушать митохондриальную функцию холангиоцитов [29]. Это происходит путем повреждения молекул липоевой кислоты, присутствующей на 2-оксокислых дегидрогеназных комплексах, расположенных на внутренней мембране митохондрий [29]. Кроме потери гуморальной толерантности наблюдается повышение уровня аутореактивного кластера дифференцировки: CD4+, CD8+, ПДК-Е2-специфических Т-клеток в печени [29]. Под действием триггерных факторов происходит активация иммунных клеток (включая макрофаги), воздействующих на Т-лимфоциты, которые продуцируют ФНО-α, индуцирующий старение и апоптоз холангиоцитов, а также ИФН-γ, стимулирующий дальнейшее образование цитотоксических Т-лимфоцитов, и ИЛ-4, способствующий активации В-клеток и дальнейшей продукции антител, специфичных для ПДК-Е2.
Одним из возможных патофизиологических механизмов патогенеза ПБХ является гипотеза желчного бикарбонатного (HCO 3) зонтика, базирующаяся на данных экспериментальных, клинических и генетических исследований, в основе которой лежит положение о том, что холангиоциты (и гепатоциты) создают защитный апикальный щелочной барьер, стабилизирующий гликокаликс, путем секреции бикарбоната (HCO 3) в просвет желчного протока. Этот щелочной барьер сохраняет соли желчных кислот (ЖК) в их полярном, непроницаемом для мембраны состоянии [30, 31].
Желчная секреция при ПБХ нарушается в связи с возникающими дефектами в работе переносчиков и каналов, расположенных на апикальной и базолатеральной мембране холангиоцитов, задействованных в образовании HCO 3. Неисправный апикальный бикарбонатный (HCO 3)-секреторный аппарат ослабляет щелочной барьер, что приводит к частичному протонированию глицин-конъюгированных (pKa 4) вместо таурин-конъюгированных (pKa 1-2) желчных солей, в результате чего образующиеся глицин-конъюгированные ЖК становятся аполярными и приобретают способность пересекать мембрану холангиоцитов независимо от активности транспортеров солей желчи, тем самым индуцируя апоптоз в холангиоцитах [32].
Разрушающиеся клетки желчных протоков секретируют медиаторы, воздействующие на синусоидальные клетки, среди которых выделяют клетки Ито (звездчатые) — основные клетки, синтезирующие экстрацеллюлярный матрикс в поврежденной печени [33]. В здоровой ткани печени звездчатые клетки находятся в пространстве Диссе и являются основным депо витамина А, участвуют в регуляции фиброгенеза. В результате прогрессирующего хронического повреждения клетки Ито активируются, дифференцируются в миофибробластоподобные клетки, приобретая сократительные, провоспалительные и профибротические свойства [34]. В последующем это приводит к нарушению взаимодействия фибротических и антифибротических механизмов, избыточному синтезу экстрацеллюлярного матрикса и формированию фиброза печени.
ДИАГНОСТИКА ПЕРВИЧНОГО БИЛИАРНОГО ХОЛАНГИТА
Диагноз основан на сочетании клинических симптомов, биохимической картины холестаза, сохраняющейся более шести месяцев, и наличии в сыворотке АМА. Ряд антинуклеарных антител (ANA) связаны с ПБХ, из них специфичны для заболевания gp210, sp100, которые необходимо определять в случае отрицательных АМА. Всем пациентам с холестазом и отрицательными АМА следует проводить магнитно-резонансную холангиопанкреатографию. Биопсия печени должна выполняться, когда описанные выше диагностические мероприятия не выявили причину хронического внутрипеченочного холестаза. Биопсия адекватного качества должна содержать не менее 11 портальных полей [14, 34, 35]. Диагноз ПБХ может быть установлен, когда имеются два из следующих трех критериев:
биохимические данные холестаза, а именно повышение уровня щелочной фосфатазы (ЩФ);
наличие AMA- или ANA-специфических антител (sp100, gp210);
гистологические признаки невоспалительного деструктивного холангита и разрушения междольковых желчных протоков (уровень доказательства III, сила рекомендаций 1) [14, 34, 35].
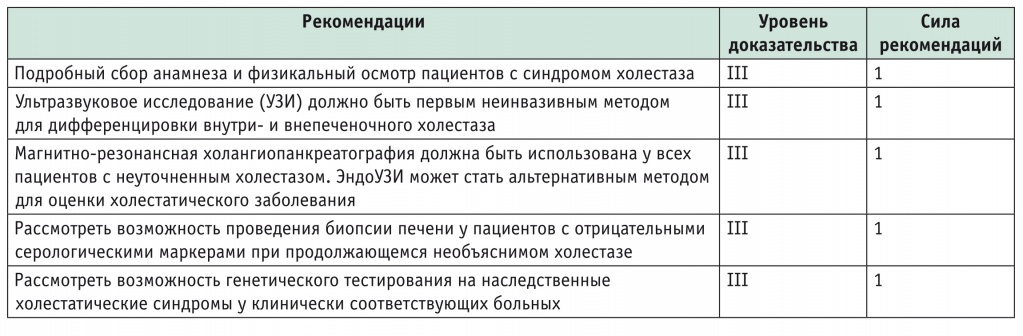
ПБХ следует подозревать у всех пациентов с персистирующим синдромом холестаза и такими симптомами, как кожный зуд и усталость ( табл. 1 ).
Рекомендации Европейской ассоциации по изучению болезней печени (2017) по диагностике первичного билиарного холангита [14]
И еще немаловажное положение: наличие изолированного повышения титра АМА недостаточно для диагностики ПБХ. Европейская ассоциация по изучению болезней печени рекомендует пациентам с нормальными биохимическими показателями цитолиза и холестаза и позитивными AMA ежегодное наблюдение с биохимической оценкой (уровень доказательства III, сила рекомендаций 1).
Более 60% больных при постановке диагноза не имеют клинических проявлений заболевания. Типичные проявления ПБХ: