Аутоиммунные антитела что это
Лабораторная диагностика аутоиммунных заболеваний
На сегодняшний день наличие огромного количества новейших тестов для диагностики патологических состояний требует от клиницистов знаний не только основ клинической биохимии, но и новых алгоритмов лабораторной диагностики.
В представленных работах мы попытались помочь клиницистам подобрать правильный подход в лабораторной диагностике ряда патологических состояний, не по протоколам, а основываясь на рекомендациях Всемирной организации здравоохранения, новейших достижениях науки и клинической практике, собственных научно практических исследований.
Представленные в наших работах комбинации различных тестов дадут возможность врачам охарактеризовать патологические процессы в организме, выйти на правильные диагностические критерии и проследить ход лечения.
При Вашем интересе к работам, мы можем продолжить публикации.
Лабораторная диагностика аутоиммунных заболеваний
Аутоиммунные заболевания (АИЗ) чаще развиваются у женщин, чем у мужчин, как правило, в молодом возрасте.
АИЗ развивается в тех случаях, когда в организме появляются антитела (АТ) или клоны реактивных Т-клеток, способные взаимодействовать с собственными антигенами и тем самым разрушать клетки и ткани несущие эти антигены. Возникший в результате АИЗ хронический процесс, приводит к долговременному повреждению тканей, структур, клеток, изменению регуляции биохимических процессов в клетках. Объясняется это тем, что аутоиммунная реакция постоянно поддерживается тканевыми антигенами. В качестве аутоантигенов могут быть различные соединения – белки, липиды, нуклеиновые кислоты, сахара, стероиды. Исследование и обнаружение в крови различных аутоантител имеет основное диагностическое значение для подтверждения АИЗ, контролю за лечением и прогнозированию.
Прежде чем перейти к диагностическим критериям АИЗ, кратко изложим основные механизмы развития АИЗ:
Исходя из особенностей изменений биохимических механизмов в клетках и строятся основные диагностические критерии АИЗ, для которых характерно «ЗОЛОТОЕ» правило. В связи с отсутствием данных об абсолютной диагностической значимости раздельного определения антител их всегда следует определять в комплексе. Следовательно, только достаточное количество тестов может иметь диагностическое значение.
Далее мы приведем примеры правильного подбора тестов, обладающих высокой информативностью при различных АИЗ:
Диагностика аутоиммунных эндокринных заболеваний
Для этих целей используются три теста: антитела к инсулину, антитела к островковым клеткам поджелудочной железы, антитела к декарбоксилазе глютаминовой кислоты (GAD). Во время асимптомотического развития диабета, антитела к трем указанным антигенам могут определяться у пациентов за 7 лет до клинического проявления болезни.
Для этих целей используются разновидности антиядерных антител, которые мы можем разделить на три группы:
Дополнительно можно ввести определение антител к центромере В и антитела к А-фодрину. Следовательно, если мы хотим диагностировать АИЗ соединительной ткани необходимо одновременно назначать следующие тесты:
Для диагностики, дифференциальной диагностики разработан высокоэффективный комплекс тестов – панель тестов, Gastro-5-Line, в которой одновременно определяются пять различных видов аутоантител, иммуноглобулины G и А антитела, а антигенами – мишенями являются внутренний фактор, париетальные клетки, глиадин, тканевая трансглутаминаза, маннан ( из бактерий)
В дополнении к указанным тестам необходимо использовать следующие определения ANCA (антинейтрофильные цитоплазматические антитела) антител: антитела к мембранному белку гранулоцитов и моноцитов (BPI) – хронические инфекционные болезни, болезнь Крона, язвенный колит, антитела к эластазе – элифизема, воспалительные ревматические болезни; антитела к катепсину G – воспалительные ревматические болезни, синдром Шегрена, синдром Фелти, СКВ; антитела к лизоциму – воспаление ЖКТ, язвенный колит; антитела к лактоферрину – первичный язвенный колит, склеротизирующий холангит.
АФС проявляется венозными и/или артериальными тромбозами, различными формами акушерской патологии (привычное невынашивание беременности, тромбоцитопенией, а также другими разнообразными неврологическими, кожными, сердечно-сосудистыми, гематологическими нарушениями. Существуют два способа диагноститки АФС – упрощенный и необходимый, в которых используется разное количество тестов.
Упрощенный вариант обеспечен следующими тестами:
Клинические параметры при назначении указанных тестов таковы: артериальный или венозный тромбоз различной локализации и/или привычное невынашивание беременности (спонтанные аборты, выкидыши, внутриутробная гибель плода).
Расширенный вариант, современными и эффективными в диагностике АФС являются следующие анализы:
Именно такая комбинация оптимальна в установлении диагноза АФС.
Возможны следующие комбинации различных биохимических маркеров:
Автор статьи: д.м.н., профессор Слюсарь Н. Н.
Аутоиммунные антитела что это
Получить результаты
Компания «Новые Медицинские Технологии»
Диагностика аутоиммунных заболеваний и синдромов
Показания к назначению анализа: диагностика и дифференциальная диагностика системных заболеваний соединительной ткани (особенно СКВ), аутоиммунного гепатита, вирусного гепатита с аутоиммунным компонентом (индуцированным вирусами или лечебными вмешательствами), первичного билиарного цирроза, рассеянного склероза; выявление аутоиммунного компонента при различных заболеваниях, в патогенезе которых может играть роль аутоагрессия. Материал для исследования: сыворотка крови.
Для определения антинуклеарных антител используется методика непрямой иммунофлюоресценции с использованием в качестве субстрата клеток культивируемой линии Нер-2.
Использование в качестве субстрата клеток злокачественной культивируемой линии благодаря их особенностям (высокое ядерно-цитоплазматическое соотношение, крупные размеры, наличие большого количества митозов) позволяет оценить различные типы свечения, характерные для присутствия в образце крови широкого спектра антител к различным антигенам, имеющих различные клинические ассоциации.
Следует иметь в виду, что часть из определяемых типов свечения является высокоспецифичной, четко ассоциирована с определенными заболеваниями и имеет вполне определенную диагностическую значимость, в особенности при выявлении в высоких титрах; однако некоторые антитела к различным антигенам могут давать сходные типы свечения, в таких случаях может требоваться дальнейшее обследование для уточнения конкретного антигена, к которому направлены аутоантитела. С другой стороны, определенный тип антител может встречаться при нескольких нозологических формах. Существуют также антитела (они встречаются редко), реагирующие исключительно с компонентами веретенного аппарата клеток; обычно они не связаны с аутоиммунными заболеваниями, и их обнаружение расценивается как ложнопозитивный, не имеющий клинических ассоциаций результат.
Все вышеперечисленные особенности обязательно отражаются в лабораторном заключении, где, помимо указания типа свечения и соответствующего ему наиболее вероятного типа антител, даются также рекомендации по трактовке результатов в смысле возможной ассоциации с конкретными нозоформами или синдромами, а также необходимые дополнительные лабораторные исследования.
ТРАКТОВКА РЕЗУЛЬТАТОВ.
У здоровых лиц моложе 60 лет следует ожидать отрицательных результатов на антитела к компонентам ядра и цитоплазмы; в низком титре (слабоположительный результат) эти антитела все же обнаруживаются у 2-3% (по некоторым данным, до 10%) практически здоровых людей, однако никогда нельзя предсказать, не разовьется ли у этих людей аутоиммунное заболевание в будущем (так, по данным некоторых авторов, антитела к ДНК начинают выявляться задолго до начала клинических проявлений СКВ, латентный период может продолжаться годами). После 60 лет частота слабоположительных результатов с возрастом постоянно растет. Клиническая значимость этих результатов остается неясной; как правило, они выявляются только в первичном (скрининговом) разведении 1:40. Исходя из этого, при выявлении положительного результата в скрининговом титре 1:40 всегда необходимо титрование, как минимум до диагностического титра 1:80. В любом случае представляется целесообразным последующее регулярное клинико-лабораторное наблюдение лиц, у которых выявлены ANA в низком титре.
ОГРАНИЧЕНИЯ МЕТОДА Положительный результат предполагает наличие определенных заболеваний (см. ниже), однако, как и результат любых лабораторных исследований, может нуждаться в подтверждении или уточнении с помощью других методов, а также в установлении клинико-лабораторных корреляций.
Надо иметь в виду, что различные лекарственные препараты могут вызывать образование аутоантител (гидралазин, прокаинамид, фенитоин, карбамазепин, изониазид, хлорпромазин, пеницилламин, леводофа, пенициллин, фенилбутазон, пероральные контрацептивы, хинидин). Наиболее частыми мишенями для этих ятрогенных аутоантител являются ядерные гистоны, что приводит к развитию гомогенного или гомогенного периферического типа свечения.
ЗАБОЛЕВАНИЯ, ПРИ КОТОРЫХ ЧАЩЕ ВСЕГО ВЫЯВЛЯЮТСЯ
АНА ИЛИ АНТИЦИТОПЛАЗМАТИЧЕСКИЕ АНТИТЕЛА
— системная красная волчанка (СКВ),
— ревматоидный артрит,
— синдром Шегрена,
— склеродермия,
— дерматомиозит,
— узелковый периартериит и др.;
Антинуклеарные антитела также могут выявляться при острых и хронических лейкозах, приобретенной гемолитической анемии, болезни Вальденстрема, малярии, хронической почечной недостаточности, тромбоцитопениях, лимфопролиферативных заболеваниях, миастении и тимомах.
Ковид и аутоиммунные заболевания
Коронавирус
Клиническая картины ковида
Во многих случаях у людей, инфицированных SARS-CoV-2, наблюдаются симптомы гриппа, такие как лихорадка, усталость и сухой кашель. Головная боль, миалгия, боль в горле, тошнота и диарея также наблюдаются у пациентов с COVID-19. В тяжелых случаях возникают одышка и гипоксемия. В критических случаях заболевание быстро прогрессирует, и у пациентов может развиться септический шок и полиорганная дисфункция. Таким образом, COVID-19 может быть системным заболеванием, поражающим несколько систем органов, включая кожу, почки, дыхательную систему, сердечно-сосудистую систему, пищеварительную систему, нервную систему и гематологическую систему. Нарушение регуляции иммунного ответа и повышение провоспалительных цитокинов, вызванных SARS-CoV-2, способствуют патогенезу заболевания и повреждению органов, что привлекло внимание к иммунорегулирующей терапии при лечении COVID-19.
Сходство ковида с аутоиммунными заболеваниями
COVID-19 имеет сходство с аутоиммунными заболеваниями по клиническим проявлениям, иммунным ответам и патогенетическим механизмам. Аутоантитела как признак аутоиммунных заболеваний также могут быть обнаружены у пациентов с COVID-19. Сообщалось, что у некоторых пациентов после заражения COVID-19 развились аутоиммунные заболевания, такие как синдром Гийена-Барре или системная красная волчанка. Предполагается, что SARS-CoV-2 может нарушать самотолерантность и вызывать аутоиммунные реакции за счет перекрестной реактивности с клетками-хозяевами.
Подобно некоторым аутоиммунным и иммуноопосредованным тромбовоспалительным заболеваниям, включая волчанку, антифосфолипидный синдром и ANCA-ассоциированный васкулит, активация нейтрофилов и образование внеклеточной ловушки нейтрофилов (НЕТоз), по-видимому, играют патогенную роль при COVID-19.
Риск заражения ковидом пациентов с аутоиммунными заболеваниями
Результаты поперечного исследования, проведенного на северо-востоке Италии, показали, что пациенты с аутоиммунными заболеваниями имели схожую частоту инфицирования SARS-CoV-2 по сравнению с населением в целом. Другое итальянское исследование, проведенное в Милане, также подтвердило, что аутоиммунное заболевание не является фактором риска заражения COVID-19. Интересно, что исследование из Милана показало, что пациенты с аутоиммунными заболеваниями не имеют худшего прогноза по сравнению с людьми, не страдающими аутоиммунными заболеваниями. Однако испанское исследование показало, что госпитализированные пациенты с аутоиммунными заболеваниями имеют более тяжелое течение COVID-19.
Напротив, результаты многоцентрового ретроспективного исследования, проведенного в провинции Хубэй, Китай, показали, что пациенты с аутоиммунными заболеваниями могут быть более восприимчивыми к инфекции SARS-CoV-2 по сравнению с контрольной группой. Кроме того, в этом исследовании были изучены члены семей пациентов, которые проживали в той же среде во время вспышки, что и контрольная группа.
В настоящее время, пока не появится больше данных, крайне важно подчеркнуть важность физического дистанцирования, ношения масок и частого мытья рук для всех, особенно для наших пациентов с аутоиммунными заболеваниями. Приверженность к лекарствам также очень важна для предотвращения вспышек аутоиммунных заболеваний, которые могут привести к повреждению органов.
Аутоантитела при ковиде
Аутоантитела, встречающиеся при ряде аутоиммунных заболеваний, были обнаружены у пациентов с COVID-19. Исследователи выявили наличие антинуклеарных антител (ANA), антицитоплазматических нейтрофильных антител (ANCA) и антиантифосфолипидных (APL) антител у пациентов с COVID-19. Результаты показали, что 45% пациентов были положительными по крайней мере на одно аутоантитело, а пациенты с положительными аутоантителами имели тенденцию иметь худший прогноз и значительно более высокую частоту дыхания при поступлении. Положительный показатель для ANA составил 33%, положительный показатель для антикардиолипиновых антител (IgG и / или IgM) составил 24%, а у трех пациентов были получены положительные результаты на антитела против β2-гликопротеина-I (IgG и / или IgM) (9%). Однако ANCA был отрицательным у всех пациентов.
У пациентов с COVID-19 с неврологическими симптомами наличие аутоантител к контактин-связанному белку 2 (анти-Caspr2), ганглиозиду GD1b (анти-GD1b) и гликопротеину олигодендроцитов миелина (анти-MOG) было показано в отчетах о случаях или ретроспективно. исследования. Однако клиническое значение этих антител остается неясным. Кроме того, имеются сообщения о случаях, демонстрирующих наличие холодовых агглютининов и аутоантител против антигенов эритроцитов у пациентов в критическом состоянии с COVID-19. а также наличие антител против Ro / SSA у пациентов с обострением пневмонии COVID-19. В исследовании, включающем 113 образцов, изучались антитела к эритроцитам с помощью прямого и непрямого антиглобулинового теста (DAT или IAT). Положительный DAT был обнаружен у 46% пациентов с COVID-19, что было значительно выше, чем у контрольных пациентов без COVID-19. Наличие связанных с мембраной эритроцитов иммуноглобулинов способствует развитию гемолитической анемии и связано с тяжестью анемии при COVID-19.
Клинический аутоиммунитет после ковида
Молекулярная мимикрия инфекционных патогенов
Производство аутоантител является ключевым признаком аутоиммунных заболеваний. Однако лежащие в основе механизмы сложны и до сих пор полностью не изучены. Молекулярная мимикрия инфекционных патогенов считается одним из механизмов. Вирусная инфекция может нарушить иммунологическую толерантность из-за воздействия антигенных эпитопов, которые вызывают перекрестно-реактивные антитела. Имеется большое количество сообщений, указывающих на антигенную мимикрию между вирусными и человеческими белками.
Лимфоциты при ковиде
Инфекция SARS-CoV-2 вызывает иммунные реакции, которые могут иметь важное значение при разработке стратегий вакцинации против этого вируса. Т-клеточный иммунитет играет центральную роль в контроле инфекции SARS-CoV-2. Антиген-специфические CD4 + и CD8 + Т-клетки и ответы нейтрализующих антител играют защитную роль против SARS-CoV-2, в то время как нарушение адаптивных иммунных ответов, таких как дефицит наивных Т-клеток, может привести к плохим исходам заболевания. В клинических лабораторных тестах, лимфопении (количество лимфоцитов ≤1.0 × 10 9 / л) связаны с тяжелой болезнью в COVID-19 больных и может быть прогностическим фактором тяжести заболевания и смертности.
Лечение ковида препаратами для терапии аутоиммунных заболеваний
Некоторые лекарства, используемые для лечения аутоиммунных ревматологических заболеваний, могут оказывать терапевтический эффект у пациентов с тяжелыми вариатами инфекции COVID-19, что обращает внимание на взаимосвязь между COVID-19 и аутоиммунными заболеваниями. Риск заражения и прогноз COVID-19 у пациентов с аутоиммунными заболеваниями остаются спорными, но строго рекомендуется соблюдение пациентом режима приема лекарств для предотвращения обострений аутоиммунных заболеваний.
В тяжелых и критических случаях применялись иммуномодулирующие препараты и биологические агенты, нацеленные на провоспалительные цитокины, для сдерживания устойчивого иммунного ответа при COVID-19. Кортикостероиды, ингибиторы JAK, блокаторы IL-1 и антагонисты рецепторов IL-6, которые знакомы ревматологам, используются для лечения пациентов с COVID-19.
Вакцинация против ковида и аутоиммунные заболевания
Анализы на гормоны и аутоантитела
Гормоны
Гормоны управляют следующими процессами:
Гормоны гипофиза
Гипофиз – своеобразный командный пункт гормональной системы организма. Здесь вырабатываются тропные гормоны. Их еще называют «гормонами гормонов». Эти вещества являются регуляторами выработки гормонов остальными железами внутренней секреции.
ТТГ – тиреоторопный гормон. Стимулирует работу щитовидной железы – основного регулятора обмена веществ в нашем организме.
ФСГ – фолликулостимулирующий гормон. У женщин это гормон стимулирует созревание фолликула в яичниках, а у мужчин играет очень важную роль в созревании спермы.
ЛГ – лютеинезирующий гормон. У женщин этот гормон вызывает разрыв фолликула (овуляцию) и образование желтого тела, а у мужчин стимулирует синтез тестостерона (основного мужского полового гормона).
Пролактин. Гормон, необходимый для нормального развития грудных желез, обеспечивающий выработку молока молочными железами. Избыток этого гормона вызывает у женщин – нарушение менструального цикла, у мужчин – импотенцию и потерю полового влечения (либидо).
СТГ – соматропный гормон. «Гормон роста». Самый необходимый гормон для нормального физического развития ребенка, у взрослых секреция СТГ в норме значительно ниже. Кроме того, он влияет на образование костной и хрящевой ткани, и выполняет еще ряд разнообразных функций, суть которых сводится к росту и развитию организма. Недостаточность продукции этого гормона у детей приводит к развитию карликовости. Симптомы недостаточности СТГ у взрослых пока недостаточно изучены. Избыток этого гормона у детей приводит к гигантизму, а у взрослых – к акромегалии.
Гормоны щитовидной железы
Щитовидная железа – основной регулятор обмена веществ в нашем организме.
Йодсодержащие тиреоидные гормоны, продуцируемые этой железой, являются главными стимуляторами метаболических процессов.
У детей тиреоидные гормоны способствуют процессу роста, а также значительно влияют на развитие головного мозга.
По соотношению этих гормонов можно судить о функциональном состоянии щитовидной железы.
Состояние, когда синтез тиреоидных гормонов снижен, называется гипотиреозом. У взрослых он характеризуется снижением скорости всех метаболических процессов, замедлением психической реакции, резким повышением утомляемости. У детей значительное снижение уровня этих гормонов в раннем возрасте приводит к сильной задержке физического и умственного развития – кретинизму.
Состояние избыточности синтеза тиреоидных гормонов называется гипертиреозом. У людей с такой патологией резко повышен основной обмен, скорость расщепления белков и жиров, сами больные выглядят очень возбужденными. У многих гипертиреоз может сопровождаться зобовидным утолщением шеи, развитием экзофтальма (пучеглазия).
Половые гормоны
Производятся в половых железах – яичниках (у женщин) и яичках (у мужчин).Незначительное количество синтезируется в надпочечниках. Основные функции – формирование и поддерживание половых функций мужского или женского организма.
Мужские гормоны
Тестостерон. Основной мужской половой гормон. Он ответственен за формирование вторичных половых признаков мужского организма. Кроме того, он обладает анаболическим эффектом. С его помощью достигается ускоренный рост мускулатуры, усиленное образование эритроцитов, более быстрая регенерация тканей. Улучшается общий обмен веществ, активизируется сжигание жира.
Повышение концентрации тестостерона может наблюдаться при наличии лишней мужской половой хромосомы (XYY), преждевременном созревании у мальчиков, различных опухолях яичек.
Снижение концентрации – при генетических заболеваниях (синдром Кляйнфельтера, гермафродизм), при длительной гиподинамии, травмах, атрофических явлениях в яичках, под воздействием ионизирующих излучений и токсических веществ.
Женские гормоны
Женские половые гормоны делятся на две группы – эстрогены и гестагены.
Эстрогены вырабатываются в первой фазе менструального цикла, гестагены – во второй. Именно бесперебойная выработка этих гормонов обеспечивает безотказную работу главных женских «часов».
Наиболее важный из эстрогенов – эстрадиол. У девочек он вызывает формирование вторичных половых признаков, а у взрослых женщин – существенно влияет на процессы оплодотворения. Кроме того, эстрадиол обладает анаболическим эффектом, правда, менее выразительным, чем тестостерон у мужчин. Еще один важный эффект эстрадиола – предотвращение потери кальция костями скелета.
К гестагенам относится, в частности, прогестерон. Он вызывает развитие слизистой матки, подготовки ее к беременности, является основным гормоном, ответственным за сохранение беременности. Прогестерон может служить точным маркером овуляции. Любое отклонение значений этих гормонов от нормальных показателей вызывает нарушение менструального цикла, может быть причиной бесплодия или невынашивания беременности.
ВНИМАНИЕ: Для получения точных результатов анализа на эстрадиол необходимо сдавать на 5-й – 7-й день менструального цикла. Анализ на прогестерон необходимо сдавать в середине второй фазы менструального цикла. Эти анализы сдают строго натощак.
β – ХГЧ является специфическим гормоном. Он начинает вырабатываться клетками плаценты к концу первой недели после оплодотворения. В первые недели беременности концентрация гормона удваивается каждые два дня. На 10-ый день после зачатия уровень β – ХГЧ возрастает в 40 раз, а к первому дню ожидаемой, но не наступившей менструации – в 100 раз.
Таким образом, возможно определять наличие беременности начиная с 7-19 дня после зачатия, еще до задержки с эффективностью не ниже 99 %.Ошибки в диагностике происходят крайне редко и, как правило, связаны с той или иной патологией (нарушение менструального цикла, склонность к невынашиванию беременности, киста желтого тела), предшествующей беременности или абортом. В этих случаях рекомендуется повторное обследование, проводимое через 3-4 дня.
Наряду с диагностикой беременности, данное исследование помогает обнаружить многие заболевания женской половой сферы.У мужчин повышение концентрации этого гормона может свидетельствовать о возможности развития опухолей различной локализации.
Аутоантитела
Стоимость анализов на гормоны и аутоантитела в нашем медцентре
Исследование в режиме CITO:
* Отделить от форменных элементов, ** Отделить от форменных элементов и заморозить
Старые друзья — ключ к аутоиммунным заболеваниям
Старые друзья — ключ к аутоиммунным заболеваниям
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Всю свою историю человечество страдало от различных инфекционных заболеваний и боролось с ними. Эпидемии чумы и холеры тысячелетиями наводили ужас на цивилизованный мир. Благодаря современным достижениям гигиены и медицины эти враги побеждены. Но не потеряли ли мы что-то важное на этом пути?
Конкурс «био/мол/текст»-2017

Работа участвовала в номинации «Биомедицина сегодня и завтра» конкурса «био/мол/текст»-2017.
Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Спонсором приза зрительских симпатий и партнером номинации «Биомедицина сегодня и завтра» выступила фирма «Инвитро».
Человеческий организм — штука несовершенная. Мы стареем, болеем и умираем. Если в каменном веке ведущей причиной смерти были травмы, голод и дикие животные, в Средние века — чума и холера, то сейчас, по данным Всемирной организации здравоохранения, это онкологические и сердечно-сосудистые заболевания. И если посмотреть на научные бюджеты и распределение грантов в биомедицине, мы увидим, что слово «рак» в заявке в разы повышает ваши шансы получить финансирование.
Однако есть заболевания, возможно, не столь смертельные, но куда сильнее бьющие по нам экономически. Это аутоиммунные заболевания, такие, как рассеянный склероз, системная красная волчанка или диабет 1-го типа. Если рак и инсульты чаще всего встречаются у пожилых людей, то аутоиммунные состояния обычно манифестируют (проявляются в виде симптомов) у молодых людей трудоспособного возраста и либо ложатся тяжким бременем на бюджет страны или больного (россияне, больные диабетом, если не получают инсулин от государства, тратят на поддержание собственной жизни от 1 до 5–6 тысяч рублей в месяц), либо, как в случае рассеянного склероза, просто ставят крест на карьере и жизни пациента.
Особенность аутоиммунных заболеваний состоит в том, что практически ни для одного из них мы за долгие годы исследований и экспериментов не научились достигать стойкой ремиссии. Текущие решения сводятся либо к поддерживающей терапии (как в случае с инсулинозависимым диабетом), либо к попыткам отсрочить терминальную стадию заболевания, на что нацелены препараты от рассеянного склероза. До недавнего времени ситуация выглядела довольно плачевно. Дополнительно усугубляет ее тот факт, что количество людей с аутоиммунными заболеваниями растет каждый год, и мы находимся на пороге настоящей эпидемии.
Однако там, где фармацевтическая отрасль терпит одну неудачу за другой, внезапно сама природа показала, куда смотреть исследователям и откуда брать по-настоящему работающее лекарство.
История вопроса
Чтобы понять, откуда возникла проблема с аутоиммунными заболеваниями, придется заглянуть далеко в прошлое.
Весь прогресс человечества с определенной долей приближения можно считать гонкой со смертью. Палеолитические охотники страдали от болезней или голода и погибали в лапах хищников. Ответом стало приручение огня, разработка более эффективных орудий и переход от непредсказуемых и опасных охоты и собирательства к оседлости и сельскому хозяйству. В эпидемиологии этот процесс принято называть «первым эпидемиологическим переходом» (англ. First epidimiologic transition, FET).
Цель перехода в целом была достигнута. Жизнь в деревянных, а затем в каменных домах позволила более не бояться хищников. Сельское хозяйство, пусть и не со стопроцентной вероятностью, но защищало от голодной смерти. Качество и продолжительность жизни ощутимо выросли. Но на смену старым убийцам пришли новые. Дело в том, что одним из наиболее значительных следствий «перехода» стали эпидемии, которых человечество раньше не знало.
Дело в изменившемся в ходе FET образе жизни человека. До этого мы жили небольшими группами, состоявшими не более чем из 50 особей, занимавшими довольно обширные пространства. К тому же мы постоянно меняли место жительства, нигде не оставались надолго. Культура гигиены была довольно низкой — зачем следить за чистотой убежища, если ты уже съел всех мамонтов вокруг и завтра надо искать новое место?
В ходе FET люди начали надолго оставаться на одном месте, формировать более крупные группы для защиты от набегов соплеменников. Скученность и загрязнение места обитания создали оптимальные условия для развития у нас инфекций. Начались эпидемии, которые были тем свирепее, чем больше был город и чем плотнее жили в нем люди.
Рисунок 1. Васнецов В.М. «Воины Апокалипсиса», 1887.
Довольно долгое время, около 5000 лет, понадобилось человечеству, чтобы научиться справляться с инфекциями. Где-то раньше, где-то позже люди осознали важность гигиены для жизни и здоровья. Были эмпирически найдены лекарства от многих болезней. Можно сказать, весь прогресс медицины и человечества в целом происходил под постоянно довлеющим страхом новых эпидемий.
Все это не могло не отразиться на нашей культуре. Во многие мировые религии с самого начала исторического периода включались гигиенические требования. Чего стоят одни только египетские жрецы, ежедневно брившие все тело и постоянно очищавшие его от любой грязи. Слово «нечистый» во многих культурах синонимично слову «плохой», «тот, кого надо избегать». Неотделимость смерти от мора научила нас панически бояться любой нечистоты, любых признаков болезни и бежать со всех ног (рис. 2).
Рисунок 2. Обложка Le petit journal от 1 сентября 1912 года, посвященного эпидемии холеры в Индии и на Ближнем Востоке в начале 20-го века.
В настоящее время мы настолько чисты, насколько не были никогда в истории. Особенно хорошо это видно в развитых странах. Мы привыкли к тому, что во все дома подведена вода и всегда есть возможность принять ванную или душ. Мы пользуемся мылом, влажными салфетками, асептическими гелями. Мы даже моем наши дороги шампунем!
Казалось бы, ну чистые и чистые, что тут такого? При чем тут аутоиммунные заболевания? Оказывается, связь самая прямая.
Гигиеническая гипотеза
Первые наметки того, что ученые сегодня называют «гигиенической гипотезой» или «гипотезой старых друзей» появились в научной литературе еще в конце 19-го века. Этот период в истории иммунологии называют «вторым эпидемиологическим переходом» (англ. Second epidimiologic transition, SET). Он характеризуется сильным снижением заболеваемости различными инфекционными заболеваниями (бактериальными и гельминтными), а также намного более редким переходом этих заболеваний в эпидемии. Возьмем, например, чуму. Все мы из школы знаем, как сильно она влияла на судьбы Европы Средних веков. Но многие ли знают, что она отнюдь не побеждена полностью? По данным ВОЗ, в 2015 году чумой по всему миру заболели 320 человек, 77 из которых умерли. Заметьте, никакой эпидемии. Очаги оперативно локализуются, заболевшие получают адекватное лечение, почти все выздоравливают. «Черная смерть» никого больше не пугает.
Этот переход стал возможен благодаря появлению антибиотиков и других высокоэффективных противопаразитических лекарств. В развитых странах он завершился к концу 20-го века. Если в середине века в Европе каждый третий житель был поражен гельминтами [1], то в настоящий момент обнаружение носителя этих паразитов скорее редкость. Россия в этом отношении практически не отстает от развитого мира благодаря нашим сильным гигиеническим традициям. Дополнительный вклад вносит городской образ жизни, централизованное снабжение очищенной водой, контроль качества пищи и так далее.
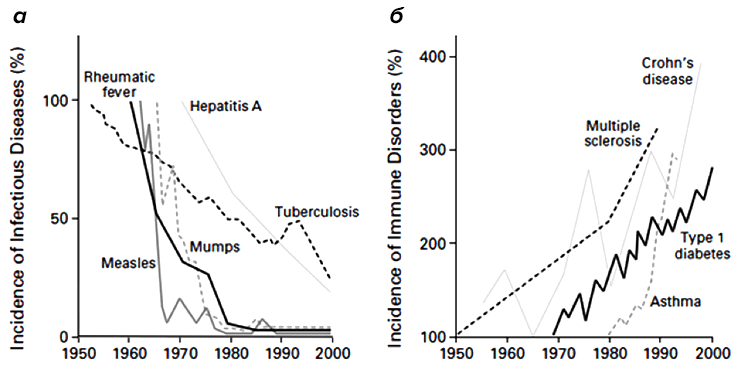
Однако еще с 19-го века начали появляться данные, что современный городской образ жизни и общее благополучие (как правило, сопровождающееся повышенной «чистотой» жизни) приводят к определенным заболеваниям (рис. 3). Типовой аристократ викторианской эпохи обязательно имел несколько «светских» заболеваний, таких, как «сенная лихорадка» или, как мы зовем ее сейчас, аллергия на пыльцу. Более серьезным «заболеванием богатых» стал диабет первого типа [2], который был бичом «благополучного общества» до открытия целебных свойств инсулина.
Рисунок 3. Обратное отношение между частотой инфекционных заболеваний и частотой иммунных расстройств с 1950 по 2000 годы. а — Изменение относительного количества заболевших различными инфекционными заболеваниями. б — Относительный рост заболеваемости аутоиммунными заболеваниями за тот же период.
Заболевания эти возникли в истории человечества внезапно и довольно-таки недавно — 200 лет назад они либо отсутствовали, либо были столь редки, что не оставили следа в медицинской литературе. Наличие связи между возникновением этих заболеваний и условиями жизни больных впервые свел воедино Дэвид Стракан в 1989 году в короткой заметке, где он постулировал «гигиеническую гипотезу» [3]. Он отметил, что сенной лихорадке больше подвержены те люди, у которых было меньше братьев и сестер в детстве. Стракан предположил, что устойчивость к сенной лихорадке передается с детскими инфекциями от сиблинга к сиблингу и является следствием сниженной гигиены.
Впоследствии многие исследователи показали то же самое на примере других аллергий и аутоиммунных реакций. К примеру, если детям из неблагополучных по гигиене регионов вроде Чили или Тайланда провести европейскую программу дегельминтизации, у них букетом высыпают аллергии [4].
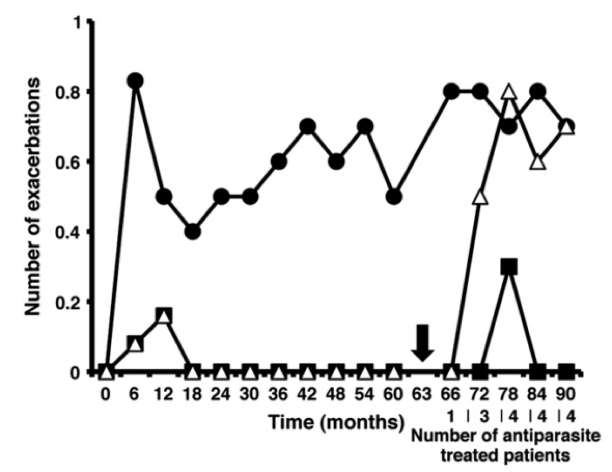
Наверное, самым интересным примером тут является история с рассеянным склерозом [5–8]. Ученые решили посмотреть, что происходит, когда больной этим страшным заболеванием заражается гельминтами, и начали искать инфицированных червями пациентов с РС. Результаты были ошеломляющи. У пациентов, которые заражались определенными гельминтами (например, власоглавом Trichuris trichiura) течение заболевания практически останавливалось [6]. Во время инфекции у них на 95% снижалось количество новых бляшек в мозге (рис. 4). Результат, недостижимый ни одним современным методом терапии! Если же по каким-то причинам гельминтов требовалось удалить (например, развивалось острое воспалительное поражение кишечника), болезнь возобновлялась с той стадии, на которой остановилась при инфекции.
Рисунок 4. График появления новых бляшек в мозге (когортное исследование 2011 года). Круги — неинфицированные гельминтами пациенты, квадраты — инфицированные, треугольники — инфицированные, но вылеченные от гельминта (момент излечения показан черной стрелкой).
Можно сказать, власоглав поддерживал здоровье этих людей, позволяя им вести нормальный образ жизни, пока они позволяют ему жить внутри себя. Так что же происходит? Как черви справляются с задачей, с которой не способна справиться современная медицина? Для ответа на этот вопрос нам придется разобраться, как же работает наш иммунитет.
Иммунный ответ
Иммунная система призвана защищать организм от внутренних и внешних врагов. Внешними врагами являются вирусы, бактерии, простейшие и черви, которые постоянно попадают в наш организм и уничтожаются на дальних рубежах. Внутренними врагами являются раковые клетки, а также клетки, зараженные вирусами или внутриклеточными бактериями.
Ключевые для иммунитета понятия — «антиген» и «воспаление». Антиген — это какая-либо молекула, которую способна узнать и атаковать иммунная система. Практически что угодно может быть антигеном. Воспаление же — это реакция ткани на повреждение или опасность такого повреждения. Молекулы, запускающие воспаление, называются провоспалительными, а блокирующие его — противовоспалительными.
Когда паразит попадает в организм, первым делом его встречает врожденный иммунитет, клетки которого (макрофаги) есть во всех тканях. Антигеном в данном случае служат нехарактерные для нашего организма молекулы — клеточная стенка бактерий, двухцепочечная РНК некоторых вирусов, свободно плавающая в межклеточном пространстве наша ДНК и так далее. При обнаружении пришельцев, клетки врожденного иммунитета пытаются их уничтожить, параллельно выделяя провоспалительные молекулы (рис. 5). Воспаленная ткань блокирует выход паразита из места проникновения в остальной организм и привлекает новые клетки иммунитета к месту повреждения.
Рисунок 5. Фагоцит пожирает бактерии.
Если врожденному иммунитету не удается уничтожить захватчиков, в дело вступает адаптивный иммунитет. Происходит это отнюдь не сразу: активации адаптивного ответа предшествуют 3–4 дня подготовки в лимфоузлах (при этом лимфоузлы увеличиваются в размерах, что является признаком инфекционного заболевания). Начинается все с того, что некоторые из клеток врожденного иммунитета прибывают в лимфоузел, неся на себе антигены из места поражения. Антигенами в данном случае выступают короткие (от 8 до 20 аминокислот) пептиды из белков инфекционного агента и окружающих тканей. По сути, макрофаг (или специализированный активатор адаптивного иммунитета — дендритная клетка) просто захватывает из места воспаления образцы растворенных белков, ошмётков паразита и погибших клеток и приносит в лимфоузел.
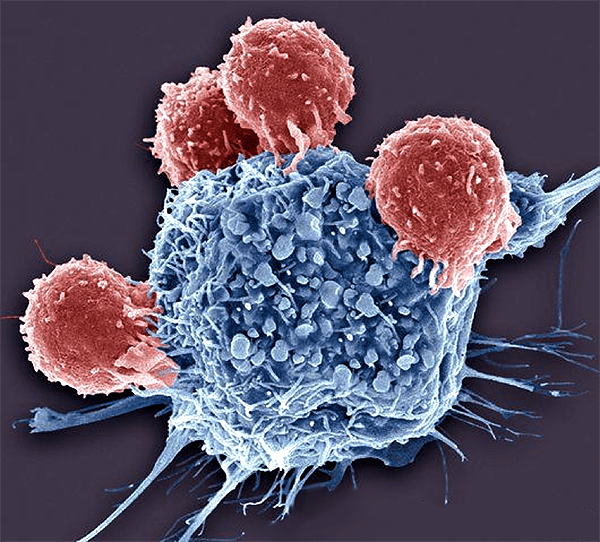
В лимфоузле его встречают наивные (неактивированные) клетки адаптивного иммунитета — Т-лимфоциты. Каждый лимфоцит, выйдя из места своего формирования, несет на себе уникальный рецептор, который формируется путем направленного внесения мутаций в геном. Заранее неизвестно, может ли этот рецептор распознать какой-либо антиген, но его вариантов так много (по некоторым оценкам, у нас может быть до 10 48 разных типов этого рецептора, но большая часть их будет нефункциональна), что в течение нескольких часов в лимфоузле обнаруживается как минимум несколько клеток, способных распознать антигены паразита. Затем эти клетки делятся, активируются и отправляются в поврежденную ткань, где отыскивают свои антигены и уничтожают как самих захватчиков, так и зараженные клетки, если мы говорим о вирусе или внутриклеточной бактерии (рис. 6).
Рисунок 6. Т-лимфоциты (красные) убивают раковую клетку (синяя) своего же организма. После получения сигнала раковая клетка начинает распадаться на небольшие пузырьки, которые затем съедят клетки врожденного иммунитета.
Иммунологическая толерантность
Иммунная система — единственная из систем организма, в чью задачу входит уничтожение других живых существ — отдельных клеток или многоклеточных организмов. Причем наши собственные клетки тоже часто должны уничтожаться, если они заражены вирусом, бактерией или превратились в раковые. При этом необходимо избегать иммунного ответа на нормальные клетки. Если такой ответ развивается — возникает аутоиммунное заболевание.
Чтобы этого избежать, в нашем организме есть система создания иммунологической толерантности — защиты «своего» от иммунитета. Центральная толерантность заключается в уничтожении в процессе развития тех Т-лимфоцитов, которые мутировали свои рецепторы так, что они могут узнать и атаковать свои антигены. Часть таких лимфоцитов из убийц превращается в защитников (так называемые регуляторные Т-лимфоциты) — они узнают заведомо «свой» антиген и подавляют любой иммунный ответ против него.
Периферическая толерантность возникает, когда Т-лимфоцит распознает антиген в лимфоузлах, но никакого воспаления в месте, откуда этот антиген попал в лимфоузел, нет. Напротив, высока концентрация противовоспалительных молекул. Такой лимфоцит опять-таки или уничтожается, или превращается в регуляторный.
Паразиты и симбионты
Миллиарды лет эволюции крупные многоклеточные организмы были домом и едой для более мелких одноклеточных и многоклеточных. Человек тут не исключение — ведь мы являемся как хорошим источником пищи, так и отличным защитником для всего, что сумеет поселиться внутри нас или на нас.
Эволюция поделила этих сожителей на 2 большие группы — паразиты и симбионты. Паразиты делают ставку на быстрое размножение. У них есть возможность подавления врожденного иммунитета, а пока адаптивный активируется, они уже успевают размножиться за счет наших ресурсов и передать инфекцию дальше. Так действует, например, вирус гриппа или бактериальная пневмония.
Симбионты же научились подавлять как врожденный, так и адаптивный иммунитеты. Для этого им пришлось умерить свои аппетиты — если клетки организма постоянно повреждаются, то никакие уловки не смогут предотвратить активацию иммунитета. Потому они поселились на поверхностях нашего тела, прежде всего на поверхности ЖКТ, где они получают лишь часть нашей пищи, но не покушаются на сам организм.
Помимо этого, они научились подавлять воспаление, выделяя вещества, которые похожи на наши противовоспалительные молекулы. Макрофаги врожденного иммунитета, столкнувшись с такими бактериями, могут почувствовать антигены клеточной стенки, но не активируются, так как подавлены противовоспалительным фоном вокруг.
Третьим механизмом защиты стала антигенная мимикрия. Для адаптивного иммунитета основным антигеном являются пептиды из белков. И многие наши симбионты в ходе эволюции поменяли свой белковый состав так, чтобы в нем был максимум пептидов, похожих на наши. Таким образом они встают под защиту регуляторных лимфоцитов. Этот механизм характерен для всех видов наших сожителей — бактерий, червей (рис. 7), вирусов и так далее.
Рисунок 7. Власоглав — один из гельминтов, активно изучаемых в рамках гигиенической гипотезы.
В течение миллионов лет каждая особь нашего вида, рождаясь, сразу же вступала в контакт с симбионтами, населявшими кожу, слизистые и кишечники своих собратьев. Со временем организм научился извлекать выгоду из такого постоянного неустранимого сосуществования. В частности, способность бактерий и червей создавать сильный противовоспалительный фон в месте своего обитания стала за это время ключевым фактором создания периферической толерантности. Она распространилась как на антигены самих сожителей, так и на сопутствующие им — антигены пищи (в кишечнике), пыли и пыльцы (в легких) и собственного организма (те самые антигены, которые сожители развили в ходе антигенной мимикрии).
И снова гигиеническая гипотеза
Внимательный читатель уже смог уловить, где тут связь. Особенность второго эпидемиологического перехода состоит в том, что мы с вами чисты, как никогда прежде, лишены практически всех червей и многих патогенов. Ребенок видит свою первую грязь или лужу отнюдь не в первые дни жизни, как раньше. Антибиотики и правила гигиены, центральное водоснабжение и мытье асфальта шампунем несомненно сделали нашу жизнь лучше. Но незаметно для себя вместе с «грязью» мы также начали устранять из своей жизни и часть тех самых симбионтов, червей и бактерий (а по мнению некоторых ученых — и некоторых вирусов), которые помогали нам создавать толерантность к собственному организму и аллергенам окружающей среды.
Уже сейчас мы имеем доказательства того, что заражение некоторыми видами симбиотической флоры ведет к снижению частоты многих аутоиммунных заболеваний [9], [10]. Это как раз та самая флора, которая широко представлена в странах третьего мира и почти не представлена в развитых странах. Пример с «остановкой» рассеянного склероза лишь самый яркий, но таких примеров намного больше. Показано, что у пациентов, зараженных таким ныне изгнанным «паразитом», повышается количество регуляторных Т-клеток, возрастает концентрация противовоспалительных молекул [9]. Изгнание симбионта возвращает все вспять. У некоторых симбионтов выявлена сильная связь с диабетом, у других — с рассеянным склерозом и так далее.
Особенно сильно на риск развития таких заболеваний влияет первый год жизни. Если в этот период ребенок оказывается в деревне, проводит некоторое время в больших группах сверстников (в больнице или в детском саду) и вообще чаще встречается с инфекциями — риск развития аутоиммунных заболеваний серьезно снижается [11], [12].
Разумеется, не только микробиом (совокупность всех симбиотических микроорганизмов конкретного человека) [13] и гельминты влияют на риск развития аутоиммунных и аллергических реакций. Есть и генетическая предрасположенность, и условия, в которых человек впервые встречается с тем или иным внешним антигеном. Есть некоторые микроорганизмы, которые не защищают, а, напротив, провоцируют аутоиммунные заболевания. Например, стрептококк способен вызывать ревматизм, а некоторые стафилококки производят суперантиген, который неспецифически запускает все клоны Т-лимфоцитов с любым рецептором — это тоже может привести к аутоиммунным заболеваниям.
Но исключения лишь подтверждают правило. Способность симбионтов и паразитов влиять, позитивно или негативно, на развитие аутоиммунных заболеваний — уже доказанный факт. Что делать с этой информацией, врачи и ученые пока не знают. Мы пробовали получать гомогенаты червей и использовать их в качестве лекарства [14]. Это не сработало. Иммунологи выясняют механизмы, с помощью которых черви достигают того, что недоступно всем врачам мира, а врачи и фармацевтические компании разрабатывают инновационные методы терапии. По состоянию на 2015 год во всем мире проводилось свыше 20 клинических испытаний «гельминтной терапии», в ходе которой пациенты принимают дозированную, полученную в стерильных условиях лучших фармпроизводств суспензию живых яиц глистов (табл.) [15]. Несмотря на неплохие результаты [16], проблемы все же остаются [4]. Например, часто гельминтов приходится удалять из-за развивающегося воспалительного заболевания кишечника. Но лучшего варианта у нас пока нет.
| Заболевание | Количество исследований | Общее количество пациентов | Результаты |
|---|---|---|---|
| Болезнь Крона | 6 | 543 | Показана безопасность и статистически значимые улучшения у большинства пациентов. |
| Неспецифический язвенный колит | 3 | 192 | Показана безопасность и статистически значимые улучшения у большинства пациентов. |
| Рассеянный склероз | 6 | 156 | Показана безопасность, статистически значимые улучшения у части пациентов. |
| Непереносимость глютена (целиакия) | 2 | 35 | Исследования только начались |
| Расстройства аутического спектра | 3 | 90 | Пилотное исследование показало эффективность, подтверждающие только начаты |
| Псориаз | 3 | 55 | Исследования только начались |
| Аллергия на арахис | 1 | 18 | Исследования только начались |
| Бронхиальная астма | 1 | 32 | Зафиксированы статистически недостоверные улучшения |
| Аллергический риноконъюнктивит | 2 | 130 | Эффективность не показана |
| Ревматоидный артрит | 1 | 50 | Исследование только началось |
О ревматоидном артрите рассказано в статье «Ревматоидный артрит: изменить состав суставов» [17], а псориазу на «Биомолекуле» посвящен целый спецпроект — «Псориаз». — Ред.
Что же делать нам, простым смертным, пока ученые по кусочкам разбирают эту тайну и ищут решение? Начать стóит со снижения маниакального стремления к чистоте во всем. Я не предлагаю не мыть руки перед едой. Но довольно часто в последнее время мы перегибаем палку. Антибиотики при каждом чихе, асептические спиртосодержащие гели каждые 10 минут, антибактериальное мыло вместо обычного в ванной. Все эти меры способны спасти вас от эпидемии. Но каждодневное их применение, особенно детьми, способно нанести куда больший урон, чем грипп или пищевое отравление.