Ацеклофенак и диклофенак в чем отличие мазей
Нестероидные противовоспалительные препараты
Поделиться:
Нестероидные противовоспалительные препараты, или НПВП, — анальгетики, проявляющие сразу три эффекта: обезболивающий, жаропонижающий и противовоспалительный. При этом дурная слава о плохом влиянии этих лекарств на желудок буквально преследует их.
Разбираться в особенностях принципа действия, показаниях и, конечно же, безопасности НПВП мы будем во второй статье из цикла о препаратах анальгетиках.
Ацетилсалициловая кислота: анальгетик с опытом
Мало кто знает, что самый первый НПВП, ацетилсалициловая кислота, имеет растительное происхождение — ее предшественник был получен из лабазника, или таволги вязолистной. Препарат создали фармацевты Байера в конце XIX века и назвали его в честь латинского наименования лабазника Spiraea ulmariа аспирином.
Принцип действия аспирина, как и всех других НПВП, состоит в блокировании фермента циклооксигеназы (ЦОГ). В организме существуют два типа ЦОГ. Первый, ЦОГ-1, — это нужный, «добрый» фермент: он выполняет множество важных функций, в том числе и защищает слизистую желудка. Второй, ЦОГ-2, отвечает за выработку простагландинов, запуская механизм боли и воспаления.
Ацетилсалициловая кислота блокирует оба вида ЦОГ, причем первый тип фермента в большей степени, чем второй. Поэтому список ее побочных эффектов немал, и лидером в нем является повреждение слизистой желудка, чреватое развитием гастрита и даже язвенной болезни. Аспирин категорически противопоказан детям младше 15 лет из-за опасности развития синдрома Рейе — тяжелого поражения мозга и печени.
Взрослые могут принимать препарат как жаропонижающее и легкое обезболивающее. Однако в последние годы ацетилсалициловая кислота на этом поприще уступила место более безопасным НПВП и перешла в разряд кардиологических препаратов благодаря свойству препятствовать агрегации тромбоцитов и «разжижать» таким образом кровь.
Сомнительный анальгин?
Метамизол натрия, или анальгин, — достаточно активный обезболивающий и очень слабый противовоспалительный препарат. К желудку он относится лояльно, направляя все свое негативное влияние на кровь. Серьезный побочный эффект анальгина — способность изменять картину крови и приводить к развитию апластической анемии, агранулоцитоза и других гематологических неприятностей.
Во многих странах мира, в том числе США, анальгин запрещен к продаже. А вот в Германии, к примеру, он широко применяется и даже считается препаратом выбора для лечения послеоперационной боли. В России анальгин знают, любят и пьют, и, признаться, в этом нет ничего страшного — главное не потреблять его регулярно (т. е. изо дня в день) и не превышать рекомендуемые дозы.
Диклофенак сотоварищи
Группа производных кислот поражает выбором даже специалистов, но каждый препарат, входящий в нее, все-таки имеет свое «лицо». Производные органических кислот отличаются выраженными противовоспалительными свойствами, нередко затмевающими обезболивающий и жаропонижающий эффект. Исключение составляет ибупрофен, который все-таки чаще всего применяется для борьбы с болью и лихорадкой, а не воспалением.
Одними из самых мощных противовоспалительных препаратов этой подгруппы считаются индометацин и диклофенак. Первый оказывает неблагоприятное действие на желудок и кровь, и применяется сегодня редко. Диклофенак гораздо более безопасен, что вкупе с высокой активностью и экономичностью обеспечивает крайне высокую популярность при ревматических заболеваниях.
Однако по анальгетическому эффекту диклофенак значительно уступает многим препаратам, в частности напроксену, который успешно применяют для борьбы с различными видами интенсивной боли, в том числе зубной, головной, периодической и т. д. Напроксен продается без рецепта врача и пользуется спросом как довольно безопасный, доступный и при этом мощный анальгетик.
Еще один НПВП, который используют для обезболивания, — кеторолак, известный под торговым названием Кетанов. Он отличается быстротой, силой и длительностью анальгетического действия в комплексе с традиционными для НПВП желудочно-кишечными побочными эффектами. Поэтому кеторолак применяют только по рецепту врача для купирования послеоперационной боли, боли при онкологических заболеваниях и в других непростых случаях.
Мефенаминовая кислота гораздо «невинней» кеторолака, однако и не столь результативна. Ее слава эффективного жаропонижающего средства несколько преувеличена: препарат чуть более активен, чем ацетилсалициловая кислота.
И еще один представитель НПВС, который нельзя обойти вниманием, — мелоксикам, совмещающий довольно щадящее действие на желудок с мощным противовоспалительным эффектом, благодаря чему он часто применяется в ревматологии.
Коксибы: последнее слово фармакологии
Коксибы — самая молодая группа НПВП, первый представитель которой, целекоксиб, появился в продаже в конце 1990-х годов. Коксибы почти не влияют на ЦОГ-1, а, значит, практически не оказывают традиционных для этой группы желудочно-кишечных побочных эффектов. Они достойно борются с болью и воспалением при артритах и других ревматоидных заболеваниях, однако первоначальных ожиданий, которыми были полны специалисты при появлении первого коксиба, не оправдали.
Препараты этой группы все-таки не лишены побочных эффектов (в частности, специалисты до сих пор обсуждают возможное влияние коксибов на повышение риска инфаркта и инсульта) и к тому же отличаются немаленькой ценой, способной вышибать почву из-под и без того нездоровых ног. Решение об их назначении должен принимать только врач, и самолечением коксибами, как, впрочем, и большинством других НПВП, заниматься не стоит.
Читателям, которых все-таки терзают муки выбора, хотелось бы сказать: не терзайтесь. Избавьтесь от этого камня на своей душе, водрузив его на плечи лечащего врача. Доверьте ему вашу боль и воспаление и не испытывайте желудок на прочность в попытках попасть пальцем в небо и отыскать из десятков лекарств самый «лучший» НПВП.
Товары по теме: [product](ацетилсалициловая кислота), [product](анальгин), [product](ибупрофен), [product](напроксен), [product](кетопрофен), [product](индометацин), [product](кеторолак), [product](ацеклофенак), [product](диклофенак), [product](пироксикам), [product](мелоксикам), [product](аркоксиа), [product](целекоксиб), [product](эторикоксиб), [product](акьюлар), [product](кетанов), [product](кеторол), [product](кетокам), [product](кетофрил), [product](долак), [product](аленталь), [product](аэртал), [product](наклофен), [product](мовалис), [product](либерум), [product](артрозан), [product](мирлокс), [product](амелотекс), [product](брутан), [product](ибуклин), [product](некст), [product](нурофен), [product](налгезин), [product](кетонал), [product](метиндол ретард), [product](коплавикс), [product](агренокс), [product](экседрин), [product](кардиомагнил), [product](кардиаск), [product](аспирин), [product](цитрамон), [product](тромбо АСС), [product](ацекардол), [product](аскофен-П), [product](аспикор), [product](тромбопол)
Большое проспективное открытое многоцентровое исследование по сравнению безопасности применения ацеклофенака и диклофенака у пациентов с ревматическими заболеваниями
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Нестероидные противовоспалительные препараты (НПВП) широко используются при ряде заболеваний опорно–двигательного аппарата, и их эффективность уже достаточно хорошо изучена. Однако развитие побочных реакций, в частности, со стороны верхних отделов желудочно–кишечного тракта, часто приводят к отмене терапии. У пациентов с повышенным риском (пожилые люди и пациенты с желудочно–кишечными заболеваниями в анамнезе) могут развиваться более серьезные побочные явления, такие как пептические язвы и их осложнения [1]. Иногда встречаются и побочные реакции со стороны печени и почек [2]. Очевидно, что существует потребность в препаратах с лучшим профилем побочных реакций.
Нестероидные противовоспалительные препараты (НПВП) широко используются при ряде заболеваний опорно–двигательного аппарата, и их эффективность уже достаточно хорошо изучена. Однако развитие побочных реакций, в частности, со стороны верхних отделов желудочно–кишечного тракта, часто приводят к отмене терапии. У пациентов с повышенным риском (пожилые люди и пациенты с желудочно–кишечными заболеваниями в анамнезе) могут развиваться более серьезные побочные явления, такие как пептические язвы и их осложнения [1]. Иногда встречаются и побочные реакции со стороны печени и почек [2]. Очевидно, что существует потребность в препаратах с лучшим профилем побочных реакций.
После перорального приема ацеклофенак, новое производное фенилуксусной кислоты ([2–(2’,6’–дихлорофениламино) фенил] ацетооксиуксусная кислота), быстро и хорошо абсорбируется. Время полужизни препарата составляет 4 часа [3]. Его эффективность, как действенного НПВП в терапии остеоартритов, ревматоидных артритов и анкилозирующих спондилитов, была доказана многими клиническими испытаниями, проводившими сравнение с кетопрофеном [4], индометацином [5,6], диклофенаком [7–10], напроксеном [11,12], пироксикамом [13] и теноксикамом [14]. Доклинические исследования на животных позволили предположить, что ацеклофенак в меньшей степени способен вызывать повреждения желудочного–кишечного тракта, чем диклофенак или другие НПВП [15–17]. У грызунов ульцерогенная активность ацеклофенака оказалась менее выраженной, чем у напроксена, диклофенака или индометацина [16].
Рандомизированные двойные слепые исследования у пациентов с остеоартритом предположили, что ацеклофенак реже вызывает побочные эффекты со стороны желудка и кишечника, а также отмену терапии, чем сравнивавшиеся НПВП [8,18]. Мета–анализ 13 испытаний III фазы [19], включивший 3574 пациентов, сравнивал ацеклофенак с другими НПВП. Частота развития побочных эффектов, желудочно–кишечных осложнений и отмены терапии на фоне приема ацеклофенака была значимо ниже (p Пациенты и методы
Для сравнения безопасности ацеклофенака и диклофенака было проведено открытое, неслепое обсервационное исследование в соответствии со стандартами SAMM, предложенными рабочей группой специалистов. В эту группу входят представители Агентства по контролю за лекарственными средствами (Medicines Control Agency (MCA)), Комитета по безопасности лекарственных средств (Committee on the Safety of Medicines), Британской медицинской ассоциации (British Medical Association), Ассоциации Британской фармакологической промышленности (Association of the British Pharmaceutical Industry) и Королевского Колледжа врачей общей практики (Royal College of General Practitioners).
Пациенты из Великобритании включались в исследование своими лечащими врачами на протяжении двух лет. Соответствующими критериям включения считались мужчины и женщины старше 18 лет, имеющие клинически признаки ревматоидного артрита, остеоартрита или анкилозирующего спондилита. Критериями исключения были следующие: пептическая язва в стадии обострения, желудочно–кишечное кровотечение, умеренное и тяжелое нарушение функции почек (уровень сывороточного креатинина > 300 мкмоль/л), беременность или планируемая беременность, побочные явления в анамнезе (например, приступы бронхиальной астмы, острый ринит или крапивница) или гиперчувствительность к НПВП или ацетилсалициловой кислоте, а также предшествующая терапия (за исключением ибупрофена) в течение 30 дней до первого визита.
Исследуемые препараты, стратификация и методы оценки
До включения в исследование по выбору лечащего врача пациентам назначался ацеклофенак 100 мг дважды в день или диклофенак 75 мг дважды в день. Протокол исследования рекомендовал придерживаться соотношения пациентов, получающих ацеклофенак или диклофенак, равным 3:1 соответственно, для того чтобы с большей точностью выявить необычные побочные эффекты от приема ацеклофенака. Период лечения продолжался 12 месяцев, и в это время был разрешен прием сопутствующих медикаментов.
По каждому пациенту была получена и зафиксирована исходная информация (анамнез заболевания, состояние почек, курение и употребление алкоголя). Побочные эффекты регистрировались в специальных формах во время плановых визитов к лечащему врачу на 1, 6 и 12–м месяцах исследования. Наблюдение за развитием побочных реакций продолжалось еще на протяжении 30 дней после приема последней в исследовании дозы препарата.
Первичным исходом исследования была безопасность лечения, оценивавшаяся по частоте развития побочных реакций, отмены терапии вследствие развития побочных реакций, частоте наступления тяжелых побочных эффектов или смерти. В подгруппах безопасность препаратов также оценивалась в зависимости от пола, возраста, расовой принадлежности и других клинически значимых характеристик пациентов (например, характер и тяжесть заболевания, употребления табака и алкоголя).
Данные по всем пациентам, получавшим исследуемые препараты, были включены в анализ безопасности терапии. Побочные эффекты регистрировались по системам организма в соответствии с кодовыми знаками для Толкового словаря терминов побочных реакций (COSTART).
Побочные реакции оценивались пациентами, как легкие, умеренные или тяжелые, а лечащим врачом – как несвязанные с препаратом, возможно связанные с приемом препарата или связанные с препаратом.
Тяжелыми побочные реакции считались при наличии следующего: летальный исход, госпитализация или продление госпитализации, другие угрожающие жизни состояния, постоянная инвалидизация, передозировка, рак или врожденные нарушения.
Отмена препарата проводилась при следующих условиях: побочные реакции, недостаточный терапевтический эффект, отклонение от протокола исследования, некомплаентность, невозможность наблюдения за пациентом или другие причины, в том числе и недоступность информации.
Статистические методы анализа были применены для сравнения демографических показателей, продолжительности приема исследуемых препаратов, частоты возникновения всех побочных эффектов, тяжелых побочных реакций и смерти в обеих группах.
Категориальные (непараметрические) характеристики, такие как пол и раса, сравнивались с использованием c 2 – теста. Непрерывные параметры обеих групп сравнивались при помощи вариантного анализа (ANOVA).
Сравнение частоты развития побочных эффектов, связанных с препаратами, и тяжелых побочных реакций в каждой группе проводилось с использованием точного теста Фишера. Сравнение числа пациентов, выбывших из исследования досрочно, проводилось при помощи c 2 – теста.
В исследование 1078 врачами было включено 10142 пациента. Среди них ацеклофенак получали 7890 пациентов, диклофенак – 2252 пациента, что соответствует соотношению 3,5:1. Кроме того, 159 пациентов получали неспецифическую терапию.
Большинство пациентов были в возрасте і 50 лет (73,9%), европеоидной расы (88,1%) и страдали остеоартритом (91,4%). Большинство пациентов были женщины (59,9%), кроме пациентов с анкилозирующим спондилитом, где доминировали мужчины (76,6%). Большая часть пациентов страдала артритом более 1 года (76,1%), а 28,1% пациентов имели длительность заболевания более 5 лет.
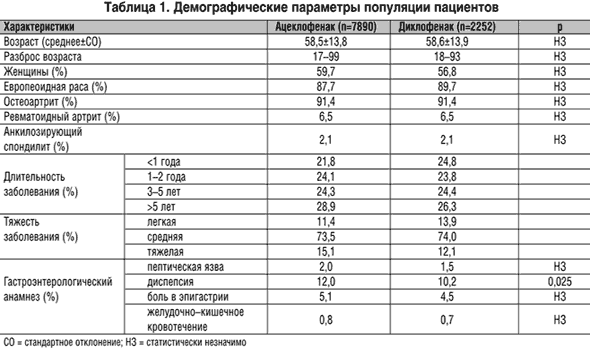
В целом между двумя группами не было различий по демографическим характеристикам, которые включали в себя пол, возраст, расу и вид заболевания (табл. 1). Тем не менее у пациентов, получавших ацеклофенак, длительность заболевания была значимо больше (p=0,019). Более того, значительно большее число пациентов, получавших ацеклофенак, имели тяжелые клинические проявления артрита (15,1%) по сравнению с получавшими диклофенак (12,1%).
Около 20% всей популяции пациентов страдали или имели в анамнезе желудочно–кишечные заболевания. По этому показателю значимых различий между группами установлено не было, хотя диспепсия в анамнезе чаще встречалась в группе ацеклофенака (p=0,025; табл. 1).
12–месячный период терапии закончили 27,9% пациентов, получавших ацеклофенак, и 27,0% получавших диклофенак. Средняя продолжительность приема лекарств в обеих группах была примерно одинакова: 168,1 дней для ацеклофенака и 170,0 дней для диклофенака.
Оба препарата переносились хорошо, и большинство побочных реакций носили легкий или умеренный характер. Пациенты, получавшие ацеклофенак, сообщили о меньшем числе побочных реакций (22,4%) по сравнению с диклофенаком (27,1%) (p Обсуждение результатов
В данной статье представлены результаты самого большого длительного проспективного обсервационного исследования по оценке в повседневной клинической практике побочных реакций, возникающих на фоне приема НПВП. Дизайн исследования четко согласовался с рекомендациями SAMM и был одобрен MCA. Выборка пациентов была репрезентативной и соответствовала популяции пациентов в обычной клинической практике.
Самым важным результатом этой работы стало то, что применение ацеклофенака сопровождалось лучшим профилем желудочно–кишечных побочных явлений и лучшей переносимостью, даже несмотря на то, что пациенты, принимавшие ацеклофенак, имели в анамнезе большую частоту заболеваний желудочно–кишечного тракта, чем пациенты из группы диклофенака. Различия между группами были большими и статистически значимыми. Например, частота возникновения абдоминальной боли, диареи и тошноты, которые вели к отмене терапии, у пациентов, получавших диклофенак, была в два раза больше, чем на фоне приема ацеклофенака. Это может обусловливать лучшую приемлемость терапии ацеклофенаком.
Механизм, лежащий в основе улучшенного профиля побочных эффектов ацеклофенака, остается неизвестным. Соответствующие механизмы сложны и вряд ли обусловлены каким–либо одним биологическим эффектом, например, таким как дифференциальная суппрессия циклооксигеназы–1 или циклооксигеназы–2. Тем не менее недавно проведенное гастроскопическое исследование показало, что диклофенак в значительной степени нарушает содержание гексозамина и локальный кровоток в слизистой оболочке желудка [22]. При терапии ацеклофенаком, напротив, содержание гексозамина в слизистой оболочке желудка значительно повышено, а локальный кровоток остается неизмененным [22]. Хотя точные механизмы повышения содержания гексозамина неизвестны, небольшая структурная модификация ацеклофенака может оказать превентивный эффект в отношении повреждения слизистой оболочки желудка в результате недостаточной секреции слизи.
Улучшенная переносимость ацеклофенака по сравнению с диклофенаком, о которой сообщалось в этом большом когортном SAMM–исследовании, подтверждает результаты нескольких клинических испытаний и мета–анализов, проводивших сравнение ацеклофенака с другими препаратами группы НПВП. Поскольку исследования типа SAMM дают ценную информацию по препарату, касающуюся его безопасности у большого числа пациентов, отражающих обычный контингент клинической практики, мы можем предположить, что описанный нами улучшенный профиль безопасности ацеклофенака приведет к меньшему количеству серьезных осложнений в обычных клинических ситуациях.
Камчатнов П.Р., Радыш Б.Б., Михайлова Н.А., Кутенев А.В.
Лечение
Желательны полное и раннее устранение боли с целью активного вовлечения пациента в процесс лечения и реабилитации, разъяснение больному доброкачественного характера заболевания, обучение его методам профилактики обострения. Важным является обеспечение оптимального уровня повседневной физической активности. Избыточая иммобилизация нежелательна не только у больных с изолированной БНС, но и у большинства пациентов радикулопатией. Ранняя активизация больного имеет исключительное значение в отношении предупреждения развития депрессивных расстройств и формирования болевого поведения [38].
В соответствии с Европейскими рекомендациями по лечению пациентов с острой БНС препаратом первого ряда для ее купирования является парацетамол. По обезболивающему эффекту он эквивалентен ацетилсалициловой кислоте и сопоставим с большинством нестероидных противовоспалительных препаратов (НПВП) или незначительно уступает им. Противоболевой эффект реализуется вследствие угнетения активности циклооксигеназ в периферических тканях и центрального противовоспалительного действия.
Экспериментальное изучение ацеклофенака
Сам по себе ацеклофенак обладает умеренным ингибирующим действием на ЦОГ 1 и 2 типов, однако в условиях местного воспаления полиморфноядерными лейкоцитами и моноцитами ацеклофенак частично метаболизируется в диклофенак и 4-гидроксидиклофенак, благодаря которым и угнетается активность ЦОГ [43].
Ацеклофенак способен препятствовать дегенерации хрящевой ткани. В эксперименте он продемонстрировал хондропротективные свойства, обеспечивая опосредованную интерлейкином-1 супрессию продукции металлопротеиназ, что стимулировало синтез протеогликанов хондроцитами [4]. В культуре клеток хрящевой ткани больных с остеоартрозом применение ацеклофенака сопровождалось повышением синтеза протеогликанов и гиалуроновой кислоты [6]. Ацеклофенак, обеспечивая сохранность хрящевой ткани, существенно не влияет на пролиферацию клеток сухожилий, не вызывая, соответственно, их гиперплазии.
Клиническая эффективность ацеклофенака
Считается, что обезболивающая активность 100 мг ацеклофенака по продолжительности своего действия превышает таковую после приема 650 мг парацетамола [8].
В рамках 6-месячного мультицентрового двойного слепого исследования 170 больных получали ацеклофенак (100 мг 2 раза/сут.) и диклофенак (50 мг 3 раза/сут.) [29]. Уменьшение болей и облегчение движений имели место в обеих группах, однако двигательные нарушения в большей степени купировались у больных, получавших ацеклофенак (17 и 22% соответственно).
Данные клинических исследований (выраженный обезболивающий эффект, хорошая переносимость), а также своеобразие влияния препарата на медиаторы воспаления говорит в пользу того, чтобы рассматривать ацеклофенак в качестве препарата выбора для длительной терапии больных с остеоартрозами, ревматоидным артритом, анкилозирующим спондилитом, некоторыми другими хроническими дегенеративными поражениями суставов [33].
Выраженные противовоспалительный и обезболивающий эффекты ацеклофенака обусловили изучение его эффективности у пациентов с БНС. Одно из первых таких исследований было посвящено сравнению эффективности ацеклофенака (135 больных 100 мг 2 раза/сут.) и теноксикама (138 больных 20 мг однократно в сутки) у больных с анкилозирующим спондилитом [39]. Исследование носило характер мультицентрового двойного слепого и продолжалось 12 недель. Оба препарата продемонстрировали высокую эффективность и сопоставимую переносимость.
Мультицентровое рандомизированное двойное слепое исследование было посвящено сравнению эффективности ацеклофенака (100 мг 2 раза/сут.) и диклофенака резината (75 мг 2 раза/сут.) у больных с острой неспецифической БНС [36]. В исследование были включены 227 больных, курс лечения составил 10 суток. Сроки и качество купирования болевого синдрома оказались сопоставимы в обеих группах, однако применение ацеклофенака характеризовалось значительно меньшим числом побочных эффектов.
Переносимость
Широкое, в особенности долгосрочное, применение неселективных ингибиторов ЦОГ сопряжено с высоким риском желудочных кровотечений. В связи с относительно низким риском гастроинтестинальных осложнений большой интерес вызывает возможность применения селективных ингибиторов ЦОГ-2. В ряде крупных рандомизированных клинических исследований, выполненных двойным слепым методом, было убедительно доказано, что селективные ингибиторы ЦОГ-2 обладают достоверно меньшим риском поражения желудочно-кишечного тракта по сравнению с препаратами неселективного действия. Убедительные результаты были получены в ходе исследований CLASS, VIGOR [7,37]. Ацеклофенак в большей степени ингибирует образование ЦОГ-2, вследствие чего частота серьезных гастроинтестинальных осложнений при его применении значительно ниже, чем у других НПВП (пироксикам, индометацин, теноксикам и кетопрофен) [19].
В предпринятое несколько позже Паневропейское исследование было включено 23407 пациентов с воспалительными и дегенеративными заболеваниями суставов [25]. Значительное улучшение, по мнению как больных, так и лечащих врачей, наступило у 84% больных, получающих ацеклофенак, при этом 90% из них сохранили приверженность к лечению. Результаты исследования позволили рекомендовать ацеклофенак для купирования как острых, так и хронических болевых синдромов.
Применение селективных ингибиторов ЦОГ-2 сопряжено с повышением риска сердечно-сосудистых осложнений, в первую очередь острого инфаркта миокарда и нарастания системного артериального давления [28,44]. Однако указанное свойство препаратов подтверждено не во всех исследованиях. Так, наблюдение более чем за 30 тыс. больными с остеоартритом и ревматоидным артритом, получавшими диклофенак (150 мг/сут.) или эотрикоксиб (60-90 мг/сут.), установило практически идентичный риск тромботических осложнений при их приеме [9]. В ходе цитированного выше исследования [34] зарегистрирована достоверно меньшая частота тромботических осложнений и случаев повышения артериального давления по сравнению с мелоксикамом и рофекоксибом.
Фармакокинетика ацеклофенака
При пероральном применении ацеклофенак быстро и полностью адсорбируется в кишечнике и спустя 1,5-2 ч достигает максимальной концентрации в крови. Препарат не обладает кумулятивной активностью, а его фармакокинетика не зависит от возраста пациентов. Назначается внутрь по 100 мг 2 раза/сут.
При одновременном применении других препаратов с ацеклофенаком возможно повышение концентраций в плазме крови дигоксина, фенитоина, лития и уменьшение эффективности диуретиков и антигипертензивных средств. При приеме ацеклофенака и кортикостероидов или других НПВП повышается риск развития побочных эффектов со стороны желудочно-кишечного тракта. При применении с ацетилсалициловой кислотой возможно снижение концентрации ацеклофенака в плазме крови. При одновременном применении непрямых антикоагулянтов повышается риск развития кровотечений.
Приведенные сведения об эффективности и переносимости ацеклофенака (Аэртал) позволяют рассматривать его в качестве препарата выбора у пациентов с острой болью в спине.
Литература
ИСТОЧНИК РМЖ 26 ЯНВАРЯ 2010 Г, ТОМ 18, № СПЕЦ