Аэртал крем или мазь что лучше
Инструкция
| Регистрационный номер: | ЛП-001289 |
| Торговое наименование препарата: | Аэртал® |
| Международное непатентованное наименование: | Ацеклофенак |
| Лекарственная форма: | Крем для наружного применения |
Состав на 1 г крема
Действующее вещество: ацеклофенак 100% микронизированный 0,015 г.
Вспомогательные вещества: воск эмульсионный, парафин жидкий, метилпарагидроксибензоат, пропилпарагидроксибензоат, вода.
Описание
Препараты для местного применения при суставной и мышечной боли; нестероидные противовоспалительные препараты для местного применения: ацеклофенак.
Механизм действия
Ацеклофенак представляет собой нестероидный противовоспалительный препарат, обладающий также жаропонижающим и анальгезирующим действием. Препарат подавляет развитие отека и эритемы независимо от этиологии воспаления. Ацеклофенак подавляет образование простагландинов и лейкотриенов за счет обратимого ингибирования циклооксигеназы.
Клиническая эффективность и безопасность
Установленная клиническая эффективность препарата дополняется хорошей переносимостью.
Применение крема Аэртал® целесообразно у пациентов с травматическими повреждениями или воспалительными заболеваниями опорно-двигательного аппарата. Было доказано, что крем Аэртал® обладает противовоспалительным и обезболивающим действием при местном применении при лечении травм опорно-двигательной системы.
Всасывание
После нанесения ацеклофенак всасывается из зоны нанесения, быстро достигая насыщения. Он накапливается в зоне всасывания, что способствует увеличению противовоспалительной активности, и постепенно поступает в системный кровоток в небольших концентрациях, поэтому риск побочного действия, в том числе на желудочно- кишечный тракт, минимизируется.
Распределение
Ацеклофенак распределяется по всему организму.
Выведение
Ацеклофенак метаболизируется в печени и выводится медленно почками и через кишечник, частично в неизмененном виде.
Показания к применению
Лечение местной боли вследствие травматических повреждений и воспалительных заболеваний опорно-двигательного аппарата, в том числе спортивных травм. Препарат может использоваться для уменьшения воспаления сухожилий, связок, мышц и суставов в случаях растяжения, перенапряжения или ушибов, а также для лечения люмбаго, кривошеи и периартрита.
Противопоказания
С осторожностью
Печеночная порфирия (обострение), эрозивно-язвенные поражения ЖКТ (в фазе обострения), тяжелые нарушения функции печени и почек, ХСН; бронхиальная астма, крапивница или острый ринит, спровоцированные приемом АСК или других НПВП; нарушения свертываемости крови (в т.ч. гемофилия, удлинение времени кровотечения, склонность к кровотечениям); пожилой возраст; период лактации.
Применение при беременности и в период грудного вскармливания
Беременность
Крем Аэртал® противопоказан при беременности. Информация о применении крема Аэртал® при беременности отсутствует.
Период грудного вскармливания.
Неизвестно, проникает ли ацеклофенак в грудное молоко. Крем Аэртал® не следует применять во время кормления грудью.
Способ применения и дозы
Способ применения
Крем Аэртал® предназначен только для наружного применения и не должен наноситься под окклюзионные повязки. После нанесения крема необходимо вымыть руки, за исключением тех случаев, когда руки являются местом нанесения препарата. Препарат не должен попадать в глаза или полость рта. Аэртал ® можно наносить только на неповрежденную кожу.
Применение у детей
Опыт применения крема Аэртал® у детей отсутствует, поэтому крем Аэртал® противопоказан к применению у детей.
Пожилые пациенты
Коррекция режима дозирования у лиц пожилого возраста не требуется.
Побочное действие
Аэртал® крем продемонстрировал хорошую переносимость. В ряде случаев описано легкое или умеренное местное раздражение, сопровождающееся гиперемией кожи и зудом, которые исчезают при прекращении лечения. В редких случаях вирус Варицелла-Зостер в сочетании с лечением НПВП может вызывать серьезные осложнения в форме инфекции кожи и мягких тканей. Кроме того, имеются отдельные сообщения о реакциях фоточувствительности (от >1/1000 до 1/10), часто (от >1/100 до 1/1000 до 1/10000 до
Крем Аэртал®
Клиническая эффективность препарата дополняется хорошей переносимостью. Применение крема Аэртал® целесообразно в случаях:
Состав на 1 г. крема:
Действующие вещество: ацеклофенак 100% микронизированный 0, 015 г.
Описание:
Белый однородный крем.
Показания к применению:
Лечение местной боли вследствие травматических повреждений и воспалительных заболеваний опорно-двигательного аппарата, в том числе спортивных травм.
Препарат может использоваться для уменьшения воспаления сухожилий, связок, мышц и суставов в случаях растяжения, перенапряжения и ушибов, а также для лечения люмбаго, кривошеи и периартрита.
Способ применения:
Крем Аэртал® предназначен только для наружного применения и не должен наноситься под окклюзионные повязки. Аэртал® следует наносить легкими массирующими движениями на пораженный участок три раза в день. Применяемая доза зависит от размера пораженного участка: 1,5-2 г крема Аэртал® (приблизительно соответствует полоске крема длиной 5-7 см).
Крем Аэртал®
Крем Аэртал® – нестероидный препарат, обладающий противовоспалительным и обезболивающим действием.
Действие крема Аэртал®:
— предотвращает развитие отека и эритемы.
Крем Аэртал® применяется для лечения местной боли вследствие:
— воспалительных заболеваний опорно-двигательного аппарата, в том числе артритов и миозитов;
— травматических повреждений опорно-двигательного аппарата, в том числе спортивных травм.
Препарат может использоваться для уменьшения воспаления сухожилий, связок, мышц и суставов в случаях растяжения, перенапряжения или ушибов, а также для лечения люмбаго, кривошеи и периартрита.
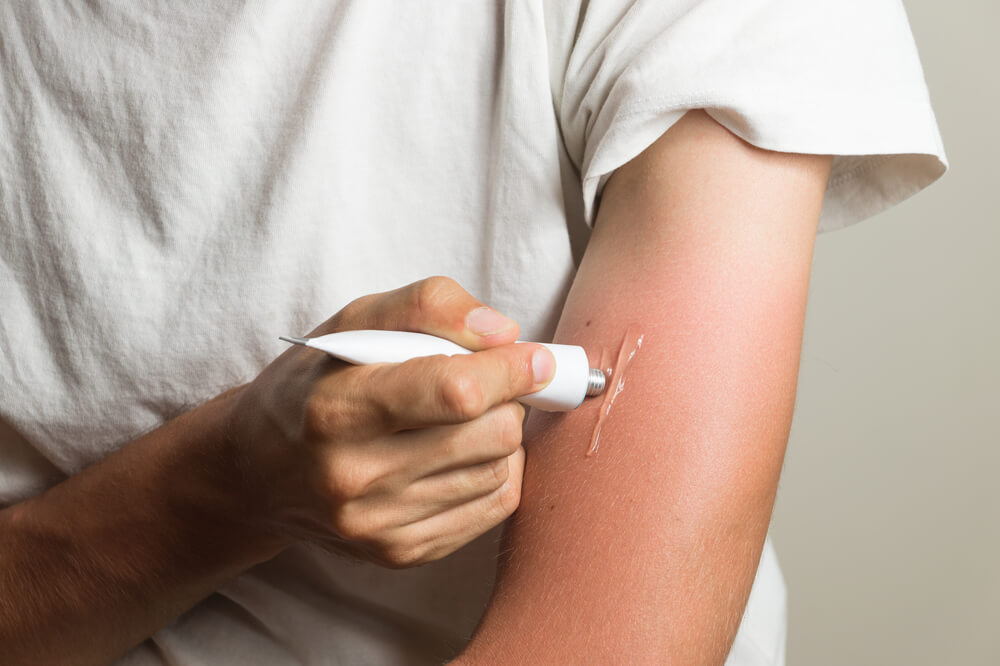
Крем Аэртал® предназначен исключительно для наружного применения. Его нельзя наносить под окклюзионные повязки и при нарушенной целостности кожных покровов в предполагаемом месте нанесения. Крем наносится массирующими движениями на место поражения 3 раза в день.
Преимущества крема Аэртал®
— клиническая эффективность при хорошей переносимости;
— единственный ацеклофенак в форме крема.
Состав крема Аэртал®:
В основе крема Аэртал® – сочетание вспомогательных веществ: эмульсионной воск и жидкий парафин, благодаря чему действующее вещество длительное время удерживается в зоне поражения. 5
Чем отличаются нестероидные противовоспалительные мази, кремы, гели
Крем Аэртал ® — это нестероидный противовоспалительный препарат на основе ацеклофенака, обладающий противовоспалительным и анальгезирующим действием. Концентрация действующего вещества в нем составляет 1,5%, при этом оно находится в креме в микронизированной форме. В состав основы крема Аэртал ® входят эмульсионный воск и жидкий парафин, а также некоторые другие вспомогательные вещества.
Аэртал ® крем следует наносить на болезненный участок трижды в день, мягкими массажными движениями. Доза нанесения определяется размером пораженного участка, при этом нужно учитывать, что 1,5–2 г крема соответствуют полоске 5–7 см.
1 Кукес В.Г. Клиническая фармакология. 2006. Сс. 534–543.
3 Краснюк И.И.. Фармацевтическая технология: Технология лекарственных форм: Учебник для студ. сред. проф. учеб, заведений. — М.: «Академия», 2004.
4 Дерматовенерология : учебник для медицинских вузов / А. В. Самцов, В. В. Барбинов.-СПб. : СпецЛит, 2008.
5 Кундер Е. В. Анальгетическая терапия воспалительных и дегенеративных заболеваний суставов // Международные обзоры: клиническая практика и здоровье. 2015. №1 (13). Сс. 56–63.
6 АЭРТАЛ® (AIRTAL®) инструкция по применению.
Ацеклофенак в терапии остеоартроза
Проведена оценка эффективности, переносимости, безопасности терапии ацеклофенаком по сравнению с диклофенаком больных гонартрозм. Показано, что оба препарата одинаково эффективны по влиянию на боль и функциональное состояние суставов, но лечение ацеклофен
Is carried out the estimation of effectiveness, transference, safety of aceclofenac therapy in comparison to diclofenac treatment of gonartrosis patients. It is shown that both preparations are equally effective on the influence on the pain and functional state of joints, but aceclofenac treatment is safer.
Остеоартроз (ОА) — заболевание, которое развивается в результате взаимодействия различных механических и биологических факторов, нарушающих существующее в норме равновесие между процессами деградации и синтеза всех компонентов матрикса и прежде всего суставного хряща [1]. В настоящее время ОА рассматривают как органное заболевание, поскольку в патологический процесс вовлекается не только хрящ, но и субхондральная кость, синовиальная оболочка, мениски, связки и периартикулярные мышцы.
Распространенность этого заболевания в популяции коррелирует с возрастом, достигая максимальных значений в возрасте старше 65 лет. Женщины болеют почти в 2 раза чаще мужчин. Развитие заболевания приводит к ухудшению качества жизни пациентов, ограничивает их физические возможности, а зачастую и социальные функции, является причиной инвалидности. По последним данным эпидемиологического исследования в России ОА с преимущественным поражением коленных и/или тазобедренных суставов страдает 13,0% населения [2].
Ведущим клиническим симптомом при ОА является боль, которая служит непосредственной причиной обращения больного к врачу. Ревматические заболевания (РЗ) отличаются по патогенезу и клинической картине, но имеют одно общее проявление — болевой синдром. С учетом патофизиологических механизмов предложено различать три основные группы болей: ноцицептивные, нейропатические и психогенные. Для ОА наиболее характерна ноцицептивная боль, которая возникает при раздражении периферических болевых рецепторов — «ноцицепторов», локализованных практически во всех органах и системах. Нейропатическая боль возникает вследствие повреждения различных отделов (периферической и центральной) соматосенсорной нервной системы и также может наблюдаться при ОА. Ноцицептивные болевые синдромы чаще всего являются острыми (ожог, порез, ушиб, ссадина, перелом, растяжение), однако при ОА они носят хронический характер. Ноцицепторами обильно снабжены ткани суставов: синовиальная мембрана, капсула сустава, связочный аппарат, периартикулярные мышцы, субхондральная кость, которые становятся источниками хронической боли при ОА. Одной из особенностей хронических болевых синдромов является рефлекторное вовлечение мышц, сначала на сегментарном поражению уровне, затем более диффузно, формирующем мышечно-тонический синдром, возникающий вследствие ноцицептивной импульсации, идущей от пораженных тканей. При длительной ноцицептивной импульсации тонически напряженная мышца сама становится источником боли и потенциально готова к формированию миофасциального болевого синдрома. Помимо возбуждения афферентными стимулами, мышечные ноцицепторы активируются эндогенными веществами, формирующимися при ее длительном напряжении и вызывающими ощущение боли, типа брадикинина, серотонина и высоких концентраций ионов калия. Брадикинин и серотонин тоже оказывают влияние на кровеносные сосуды и вызывают изменение локального состояния васкуляризации. Длительное напряжение мышц через механизмы нейрогенного воспаления способствует появлению локусов болезненных мышечных уплотнений, что еще более усиливает афферентный поток ноцицептивных импульсов в структуры ЦНС и как следствие этого, сенситизируется большее количество центральных ноцицептивных нейронов. Этот порочный круг играет важную роль в хронизации боли [29]. Интенсивность ее при ОА может зависеть от многих факторов, и, как показали последние исследования, одним из них является нарастание минеральной плотности субхондральной большеберцовой кости [3, 4].
Ведущее место в лечении ОА занимают нестероидные противовоспалительные препараты (НПВП), относящиеся к классу симптом-модифицирующих препаратов. В ревматологии НПВП рассматриваются как необходимый компонент комплексного лечения, что патогенетически обосновано, так как постоянно присутствующий воспалительный процесс является причиной болевого синдрома и прогрессирования заболевания. Обладая противовоспалительными, анальгетическими и жаропонижающими свойствами, они широко используются для уменьшения боли, воспаления, скованности и улучшения функции суставов, не влияя на исход заболевания, но значительно улучшая качество жизни больных. Как показали данные большого числа клинических исследований, при ревматических заболеваниях (РЗ) НПВП значительно эффективнее, чем высокие дозы парацетамола (4 г/сут), и не уступают опиоидным анальгетикам (таким как трамадол) [5, 6]. Однако даже кратковременный прием НПВП у определенной группы больных может приводить к развитию серьезных нежелательных явлений.
Разнонаправленность биологического действия НПВП объясняет не только их противовоспалительное действие, но и определенный спектр класс-специфических осложнений, возникающих на фоне их приема. Наиболее частые побочные эффекты НПВП — поражение желудочно-кишечного тракта (ЖКТ), негативное влияние на систему кровообращения, снижение агрегации тромбоцитов. Потенциально важными осложнениями являются также нефро- и гепатотоксичность.
Развитие НПВП-индуцированных гастропатий определяется в первую очередь системным воздействием НПВП, связанным с подавлением активности циклооксигеназы-1 (ЦОГ-1), определяющей синтез «цитопротективных» простагландинов (ПГ), что приводит к существенному снижению ее защитного потенциала и способствует повреждению слизистой. Снижение агрегации тромбоцитов, ухудшение капиллярного кровотока в слизистой, блокада NO-синтетазы и ферментных систем митохондрий эпителиоцитов, усиление клеточного апоптоза, влияние на желудочную секрецию и нарушение процессов репарации связаны с блокадой ЦОГ-2 и являются дополнительными факторами, связанными с системным воздействием НПВП [8]. НПВП-гастропатии возникают в хронологической связи с приемом НПВП и проявляются эрозиями и язвами верхних отделов ЖКТ, на фоне которых возможны такие осложнения, как желудочно-кишечное кровотечение и перфорация. Негативное влияние этих препаратов может отмечаться во всех отделах ЖКТ, от полости рта до прямой кишки. Поражения печени, ассоциированные с регулярным приемом НПВП, проявляются бессимптомным повышением трансаминаз у 1–5% больных. Клинически выраженные гепатотоксические реакции встречаются существенно реже — около 1 случая на 10 000 больных. Больным, регулярно принимающим НПВП и имеющим возможные факторы риска поражения печени, требуется регулярный контроль биохимического анализа крови.
Кардиоваскулярные побочные эффекты НПВП особенно выражены у лиц пожилого возраста и у больных, страдающих сопутствующими заболеваниями (ишемическая болезнь сердца, сахарный диабет), а также ревматическими воспалительными заболеваниями (в первую очередь ревматоидный артрит (РА)). НПВП являются независимым фактором риска развития артериальной гипертензии (АГ). Результаты рандомизированных клинических исследований и метаанализов свидетельствуют, что прием неселективных (нНПВП) и селективных НПВП (сНПВП) приводит к повышению АД и имеет существенное значение у больных, исходно имеющих АГ [9]. Особое внимание привлечено к потенциальным кардиоваскулярным осложнениям на фоне приема сНПВП, что связано с возможностью этих препаратов снижать ЦОГ-2-зависимый синтез простациклина (РGl2) клетками сосудистого эндотелия и отсутствием влияния на ЦОГ-1-зависимый синтез тромбоксана (ТхА2) тромбоцитами, что потенциально может приводить к нарушению баланса РGl2/ТхА2 и, следовательно, к активации агрегации и адгезии тромбоцитов и увеличению риска тромбообразования. Необходимо отметить, что НПВП, как класс, способны повышать риск развития кардиоваскулярных осложнений, однако этот фактор существенно уступает по значению другим, таким как курение, дислипидемия, ожирение [8, 27].
Тем не менее, при грамотном назначении НПВП можно снизить риск развития нежелательных явлений. При индивидуальном подборе НПВП необходимо учитывать анальгетический эффект препарата, индивидуальный риск развития нежелательных явлений со стороны ЖКТ и сердечно-сосудистой системы. Опасность ЖКТ-осложнений снижается при назначении ингибиторов протонной помпы (ИПП), а кардиоваскулярный риск — при использовании низких доз ацетилсалициловой кислоты [10]. Необходимо помнить, что основными факторами риска являются пожилой возраст (старше 65 лет), наличие в анамнезе язвенной болезни, длительный прием высоких доз НПВП и одновременное применение двух и более различных НПВП, а также сочетанный прием НПВП и гормональных препаратов. В последних международных рекомендациях по лечению больных ОА говорится о том, что терапию НПВП необходимо проводить в минимальных эффективных дозах и, по возможности, не назначать их длительно [7].
В России имеется широкий спектр НПВП и закономерно возникает вопрос о рациональном выборе препарата. Несомненно, он должен основываться на объективном сравнении достоинств и недостатков различных представителей этой группы препаратов. Доказано, что в эквивалентных дозах и при достаточном времени наблюдения все НПВП (селективные и неселективные) демонстрируют одинаковую эффективность [28].
Основной принцип действия НПВП заключается в подавлении ЦОГ — фермента метаболизма арахидоновой кислоты в простагландины. Особое место среди НПВП занимает ацеклофенак (Аэртал), который обладает многокомпонентным действием на воспаление. Ацеклофенак ингибирует и ЦОГ-1 (синтез физиологических ПГ), и ЦОГ-2 (синтез провоспалительных ПГ), приближаясь к селективным НПВП, и поэтому является более безопасным в отношении ЖКТ. Препарат ингибирует синтез провоспалительного цитокина интерлейкина IL-1-бета, который подавляет пролиферацию хондроцитов и активизирует деградацию хряща. Важной способностью ацеклофенака является подавление синтеза фактора некроза опухоли альфа (ФНО-альфа), оксида азота. Кроме этого, препарат угнетает экспрессию молекул клеточной адгезии (L-селектин), подавляет адгезию нейтрофилов к эндотелию, что обеспечивает выраженный противовоспалительный эффект [14, 15]. В настоящее время особое внимание уделяется влиянию НПВП на метаболизм хрящевой ткани. Условно НПВП можно разделить на три группы: хондронегативные, нейтральные по отношению к хрящевой ткани и хондропротективные. Вопрос о негативном влиянии некоторых препаратов из этой группы на прогрессирование ОА широко обсуждается [11–13]. Так, в исследованиях in vitro было показано, что индометацин и салицилаты ингибируют синтез компонентов матрикса хряща, способствуя прогрессированию заболевания, а индометацин оказывает прямое негативное действие, снижая содержание протеогликанов в гиалиновом хряще и повышая потерю вновь образованных протеогликанов. В то же время некоторые НПВП повышают синтез компонентов матрикса и тормозят апоптоз хондроцитов. Ацеклофенак в эксперименте продемонстрировал способность повышать синтез протеогликанов и гиалуроновой кислоты в культуре клеток хряща больных ОА, а также снижать продукцию металлопротеиназ, вызывающих деструкцию костной и хрящевой ткани [14, 15]. Blot L. и соавт., изучая изменения в метаболизме протеогликанов и гиалуронана под влиянием ацеклофенака, диклофенака и мелоксикама в эксплантах хряща, полученных от больных среднетяжелым и тяжелым гонартрозом, показали, что при лечении диклофенаком метаболический баланс между содержанием протеогликанов и гиалуроновой кислоты в экстрацеллюлярном матриксе гиалинового хряща оставался без изменений. Ацеклофенак и мелоксикам, напротив, обладали дозозависимым эффектом и повышали синтез протеогликанов и гиалуроновой кислоты при среднетяжелом ОА [15].
Клиническая эффективность ацеклофенака доказана в 132 опубликованных клинических исследованиях. Переносимость и эффективность этого препарата изучалась в сравнительных исследованиях с различными анальгетиками и НПВП. Так, Battle-Gualda E. и соавт. в двойном слепом рандомизированном 6-недельном исследовании у 168 больных с ОА коленных суставов показали, что ацеклофенак в дозе 200 мг/сут был эффективнее в отношении купирования болевого синдрома при лучшей переносимости по сравнению с парацетамолом 3 г/сут [16]. В более длительном исследовании (период наблюдения составил 12 недель) у больных с гонартрозом, ацеклофенак 200 мг/сут сравнивали с напроксеном 1 г/сут. Оба препарата обладали равным анальгетическим эффектом, однако у ацеклофенака было отмечено значительно меньшее количество нежелательных явлений со стороны ЖКТ [17]. Результаты метаанализа 13 рандомизированных двойных слепых исследований у пациентов с РЗ показали, что при приеме ацеклофенака в течение длительного времени (3–6 месяцев) побочные реакции развивались в 1,38 раза реже, чем при приеме других НПВП [18]. Эффективность ацеклофенака оценивалась в рандомизированных исследованиях и при других РЗ: при РА ацеклофенак в дозе 200 мг/сут был сопоставим с диклофенаком в дозе 150 мг/сут, кетопрофеном в дозе 150 мг/сут, пироксикамом в дозе 20 мг/сут. Также было отмечено, что положительная динамика быстрее развивалась у больных, получавших ацеклофенак. У больных с анкилозирующим спондилоартритом (АС) в сравнительных исследованиях ацеклофенака 200 мг/сут, теноксикама 20 мг/сут, напроксена 1 г/сут и индометацина 100 мг/сут были получены сходные результаты [19].
Больные РЗ, как правило, вынуждены принимать НПВП длительное время, поэтому очень важна хорошая переносимость препарата. Результаты проспективного, открытого, многоцентрового 12-месячного исследования SAMM (Safety Assessment of Marketed Medicines), в котором оценивалась безопасность ацеклофенака и диклофенака у 10 142 больных, страдающих РА, ОА, АС, подтвердили хорошую переносимость ацеклофенака [20]. Ацеклофенак в дозе 200 мг/сут получали 7890 человек и диклофенак 150 мг/сут — 2252 пациента. Исследователями была проанализирована частота побочных реакций: нежелательные явления возникли у 22,4% больных, получавших ацеклофенак, и у 27,1% — принимавших диклофенак. Наиболее частыми из них были реакции со стороны ЖКТ (диспепсия, боли, диарея, тошнота) — в 10,6% и 15,2% (р 40 мм по ВАШ. По демографическим и клиническим параметрам группы были сопоставимы (табл. 1). Первая группа принимала ацеклофенак (Аэртал) 200 мг/сут, вторая — диклофенак 100 мг/сут. Длительность исследования составила 3 месяца. Оценивались: индекс WOMAC, тест «встань и иди», опросник EQ-5D, общий и биохимический анализы крови.
Результаты исследования и обсуждение
Достоверное уменьшение интенсивности боли и улучшение функции суставов, уменьшение суммарного индекса WOMAC отмечалось через месяц терапии в обеих группах больных и сохранялось весь период наблюдения (табл. 2). Более быстрое снижение скованности отмечалось у больных, принимавших ацеклофенак, когда уже на втором визите были получены статистически значимые показатели, к концу лечения отмечалось достоверное снижение скованности в обеих группах больных. Достоверное улучшение показателей общего состояния здоровья и EQ-5 D, а также уменьшение затрачиваемого времени при выполнении теста «встань и иди» наблюдалось в обеих группах со второго визита.
Через месяц «значительное улучшение» и «улучшение» чаще наблюдалось на фоне приема ацеклофенака (86,3%), чем на диклофенаке (66%), через 3 месяца терапии — у 95,8% и у 76,2% соответственно (р
Е. П. Шарапова*, кандидат медицинских наук
Е. А. Таскина*
Т. А. Раскина**, доктор медицинских наук
И. Б. Виноградова***, кандидат медицинских наук, доцент
О. Н. Иванова****, кандидат медицинских наук
Л. В. Меньшикова*****, доктор медицинских наук, профессор
Л. И. Алексеева*, доктор медицинских наук, профессор
*ФГБУ НИИ ревматологии РАМН, Москва
**ГБОУ ВПО КемГМА Минздравсоцразвития России, Кемерово
***ГУЗ ОКБ, Ульяновск
****ГУЗ ОКБ № 1, Воронеж
*****ГБОУ ДПО ИГМАПО Минздравсоцразвития России, Иркутск
Нестероидные противовоспалительные препараты: список и цены
Нестероидные противовоспалительные препараты используются достаточно широко для подавления воспалительных процессов в организме. НПВП доступны в различных формах выпуска: таблетки, капсулы, мази. Они обладают тремя основными свойствами: жаропонижающими, противовоспалительными и болеутоляющими.
Лучший нестероидный противовоспалительный препарат может подобрать только врач, отталкиваясь от индивидуальных особенностей пациента. Самолечение в данном случае может быть чревато развитие серьезных побочных реакций или же передозировки. Предлагаем ознакомиться со списком препаратов. Рейтинг разработан на основании соотношения цена-качество, отзывов пациентов и мнения специалистов.
Как работают НПВП?
Нестероиды ингибируют агрегацию тромбоцитов. Терапевтические свойства объясняются блокадой фермента циклооксигеназы (ЦОГ-2), а также снижением синтеза простагландина. По мнению специалистов они оказывают влияние на симптомы заболевания, но не устраняют причину его возникновения. Поэтому не следует забывать о средствах, с помощью которых должны быть устранены первичные механизмы развития патологии.
Если у пациента обнаружена непереносимость НПВП, тогда они заменяются лекарствами других категорий. Часто в таких случаях применяют комбинацию противовоспалительного и болеутоляющего средства.
Как показывает практика, нецелесообразно заменять одно лекарство другим той же группы, если при приеме обнаруживается недостаточный терапевтический эффект. Удвоение дозы может привести только к клинически незначительному увеличению воздействия.
Классификация НПВП
Нестероидные противовоспалительные средства классифицируются в зависимости от того, являются ли они селективными для ЦОГ-2 или нет. Таким образом, с одной стороны, есть неселективные НПВП, а с другой – селективные ЦОГ-2.
.gif)


